–Ю–±—Й–∞—П —Б—В—А—Г–Ї—В—Г—А–љ–∞—П —Д–Њ—А–Љ—Г–ї–∞ –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Р–ї—М–і–µ–≥–ЄћБ–і—Л (–Њ—В –ї–∞—В. al cohol dehyd rogenatus—Б–њ–Є—А—В , –ї–Є—И—С–љ–љ—Л–є –≤–Њ–і–Њ—А–Њ–і–∞ ) вАФ –Ї–ї–∞—Б—Б –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є , —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –∞–ї—М–і–µ–≥–Є–і–љ—Г—О –≥—А—Г–њ–њ—Г (-CHO)[ 1] –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ —Б–≤—П–Ј–∞–љ–∞ —Б –Њ–і–љ–Є–Љ –∞—В–Њ–Љ–Њ–Љ –≤–Њ–і–Њ—А–Њ–і–∞ –Є –Њ–і–љ–Њ–є –≥—А—Г–њ–њ–Њ–є R[ 2]
–°–ї–Њ–≤–Њ –∞–ї—М–і–µ–≥–Є–і –±—Л–ї–Њ –њ—А–Є–і—Г–Љ–∞–љ–Њ –Ѓ—Б—В—Г—Б–Њ–Љ —Д–Њ–љ –Ы–Є–±–Є—Е–Њ–Љ –Ї–∞–Ї —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –ї–∞—В–Є–љ—Б–Ї–Њ–≥–Њ alcohol dehydrogenatus вАФ –і–µ–≥–Є–і—А–Є—А–Њ–≤–∞–љ–љ—Л–є —Б–њ–Є—А—В[ 3] alcohol dehydrogenatum [ 1] —Д–Њ—А–Љ–Є–ї , –∞ —В–∞–Ї–ґ–µ –і—А—Г–≥–Є–µ –Њ–і–љ–Њ–Ї–Њ—А–µ–љ–љ—Л–µ —Б–ї–Њ–≤–∞ (—Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і , —Д–Њ—А–Љ–Є–∞—В—Л ), –њ—А–Њ–Є–Ј–Њ—И–ї–Є –Њ—В –ї–∞—В. formica вАФ –Љ—Г—А–∞–≤–µ–є [ 4]
–Т –њ–Њ–њ—Г–ї—П—А–љ–Њ–є –Є –љ–∞—Г—З–љ–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ –Љ–Њ–ґ–љ–Њ –љ–µ—А–µ–і–Ї–Њ –≤—Б—В—А–µ—В–Є—В—М –Є—Б—В–Њ—А–Є—З–µ—Б–Ї–Є–µ, –Є–ї–Є —В—А–Є–≤–Є–∞–ї—М–љ—Л–µ, –љ–∞–Ј–≤–∞–љ–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Б–ї–Њ–ґ–Є–≤—И–µ–є—Б—П —В—А–∞–і–Є—Ж–Є–Є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤–Љ–µ—Б—В–Њ —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –љ–∞–Ј–≤–∞–љ–Є–є. –Ґ—А–Є–≤–Є–∞–ї—М–љ—Л–µ –љ–∞–Ј–≤–∞–љ–Є—П –Њ–±—Л—З–љ–Њ –њ—А–Њ–Є—Б—Е–Њ–і—П—В –Њ—В –љ–∞–Ј–≤–∞–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В , –∞ —В–∞–Ї–ґ–µ –Њ—В –љ–∞–Ј–≤–∞–љ–Є—П –Є—Б—В–Њ—З–љ–Є–Ї–∞, –Є–Ј –Ї–Њ—В–Њ—А–Њ–≥–Њ –±—Л–ї –≤—Л–і–µ–ї–µ–љ —В–Њ—В –Є–ї–Є –Є–љ–Њ–є –∞–ї—М–і–µ–≥–Є–і. –Ґ–∞–Ї, –љ–∞–њ—А–Є–Љ–µ—А, –Љ–µ—В–∞–љ–∞–ї—М –љ–∞–Ј—Л–≤–∞—О—В –Љ—Г—А–∞–≤—М–Є–љ—Л–Љ –∞–ї—М–і–µ–≥–Є–і–Њ–Љ, —Н—В–∞–љ–∞–ї—М вАФ —Г–Ї—Б—Г—Б–љ—Л–Љ, –њ–µ–љ—В–∞–љ–∞–ї—М вАФ –≤–∞–ї–µ—А–Є–∞–љ–Њ–≤—Л–Љ –∞–ї—М–і–µ–≥–Є–і–Њ–Љ, —Ж–Є—В—А–Њ–љ–µ–ї–ї–∞–ї—М –њ–Њ–ї—Г—З–Є–ї —Б–≤–Њ—С –љ–∞–Ј–≤–∞–љ–Є–µ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –±—Л–ї –≤—Л–і–µ–ї–µ–љ –Є–Ј –Љ–∞—Б–ї–∞ —Ж–Є—В—А—Г—Б–Њ–≤—Л—Е .
–Ш—Б—В–Њ—А–Є—З–µ—Б–Ї–Є —Б–ї–Њ–ґ–Є–ї–Њ—Б—М, —З—В–Њ –њ–∞—А—Д—О–Љ–µ—А—Л –љ–∞–Ј—Л–≤–∞—О—В –Љ–љ–Њ–≥–Є–µ –њ–∞—Е—Г—З–Є–µ –≤–µ—Й–µ—Б—В–≤–∞ –∞–ї—М–і–µ–≥–Є–і–∞–Љ–Є, –і–∞–ґ–µ —В–µ, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –Є–Љ–µ—О—В –љ–Є—З–µ–≥–Њ –Њ–±—Й–µ–≥–Њ —Б –љ–Є–Љ–Є. –°—А–µ–і–Є —В–∞–Ї–Њ–≤—Л—Е, –љ–∞–њ—А–Є–Љ–µ—А, –њ–µ—А—Б–Є–Ї–Њ–≤—Л–є , –Ј–µ–Љ–ї—П–љ–Є—З–љ—Л–є –Є –Ї–Њ–Ї–Њ—Б–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і , –Ї–Њ—В–Њ—А—Л–µ —П–≤–ї—П—О—В—Б—П –љ–µ –∞–ї—М–і–µ–≥–Є–і–∞–Љ–Є, –∞ —Б–ї–Њ–ґ–љ—Л–Љ–Є —Н—Д–Є—А–∞–Љ–Є –Є–ї–Є –ї–∞–Ї—В–Њ–љ–∞–Љ–Є . –Ґ–∞–Ї–ґ–µ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –∞–ї—М–і–µ–≥–Є–і—Л —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ –љ–∞–Ј—Л–≤–∞—О—В—Б—П –њ–Њ —З–Є—Б–ї—Г –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞, —Е–Њ—В—П, –љ–∞–њ—А–Є–Љ–µ—А, –њ–µ—А—Б–Є–Ї–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і, –Њ–±–Њ–Ј–љ–∞—З–∞–µ–Љ—Л–є –Ї–∞–Ї ¬Ђ–∞–ї—М–і–µ–≥–Є–і C14¬ї, –љ–∞ —Б–∞–Љ–Њ–Љ –і–µ–ї–µ –Є–Љ–µ–µ—В –ї–Є—И—М 11 –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞[ 5]
–Я–Њ –љ–Њ–Љ–µ–љ–Ї–ї–∞—В—Г—А–µ –Ш–Ѓ–Я–Р–Ъ –љ–∞–Ј–≤–∞–љ–Є—П –њ—А–Њ—Б—В—Л—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Њ–±—А–∞–Ј—Г—О—В—Б—П –Њ—В –љ–∞–Ј–≤–∞–љ–Є–є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –∞–ї–Ї–∞–љ–Њ–≤ —Б –і–Њ–±–∞–≤–ї–µ–љ–Є–µ–Љ —Б—Г—Д—Д–Є–Ї—Б–∞ -–∞–ї—М , –∞ –і–Є–∞–ї—М–і–µ–≥–Є–і–Њ–≤ вАФ —Б—Г—Д—Д–Є–Ї—Б–∞ -–і–Є–∞–ї—М (–≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ –∞—В–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ –∞–ї—М–і–µ–≥–Є–і–љ–Њ–є –≥—А—Г–њ–њ—Л —Г–ґ–µ –≤—Е–Њ–і–Є—В –≤ —Б–Њ—Б—В–∞–≤ —А–Њ–і–Њ–љ–∞—З–∞–ї—М–љ–Њ–≥–Њ –∞–ї–Ї–∞–љ–∞). –Я—А–Є —Н—В–Њ–Љ –≤ –љ–∞–Ј–≤–∞–љ–Є–Є –љ–Њ–Љ–µ—А –њ—А–Є –∞–ї—М–і–µ–≥–Є–і–љ–Њ–є –≥—А—Г–њ–њ–µ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ —Б—В–∞–≤—П—В, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–љ–∞ –≤—Б–µ–≥–і–∞ –Ј–∞–љ–Є–Љ–∞–µ—В –Ї—А–∞–є–љ–µ–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ. –Х—Б–ї–Є –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ –љ–µ –≤—Е–Њ–і–Є—В –≤ —А–Њ–і–Њ–љ–∞—З–∞–ї—М–љ—Г—О —Б—В—А—Г–Ї—В—Г—А—Г (–љ–∞–њ—А–Є–Љ–µ—А, –µ—Б–ї–Є —А–Њ–і–Њ–љ–∞—З–∞–ї—М–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А–Њ–є —П–≤–ї—П–µ—В—Б—П —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–є —Г–≥–ї–µ–≤–Њ–і–Њ—А–Њ–і –Є–ї–Є –≥–µ—В–µ—А–Њ—Ж–Є–Ї–ї ), —В–Њ –Ї –љ–∞–Ј–≤–∞–љ–Є—О –і–Њ–±–∞–≤–ї—П–µ—В—Б—П —Б—Г—Д—Д–Є–Ї—Б -–Ї–∞—А–±–∞–ї—М–і–µ–≥–Є–і [ 6] [ 7]
–Х—Б–ї–Є –≤ –і–∞–љ–љ–Њ–Љ —Б–Њ–µ–і–Є–љ–µ–љ–Є–Є –∞–ї—М–і–µ–≥–Є–і–љ–∞—П –≥—А—Г–њ–њ–∞ –љ–µ —П–≤–ї—П–µ—В—Б—П —Б—В–∞—А—И–µ–є, —В–Њ –≤ —В–∞–Ї–Є—Е —Б–ї—Г—З–∞—П—Е –µ—С –Њ–±–Њ–Ј–љ–∞—З–∞—О—В –Є—Б–њ–Њ–ї—М–Ј—Г—П –њ—А–Є—Б—В–∞–≤–Ї—Г —Д–Њ—А–Љ–Є–ї -, —Г–Ї–∞–Ј—Л–≤–∞—П –µ—С –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ[ 7]
–Т —Г—Б—В–∞—А–µ–≤—И–Є—Е –Ц–µ–љ–µ–≤—Б–Ї–Њ–є (1892) –Є –Ы—М–µ–ґ—Б–Ї–Њ–є (1930) –љ–Њ–Љ–µ–љ–Ї–ї–∞—В—Г—А–∞—Е, –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –Ј–∞–Љ–µ–љ—С–љ–љ—Л—Е —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–Њ–Љ–µ–љ–Ї–ї–∞—В—Г—А–Њ–є –Ш–Ѓ–Я–Р–Ъ , –∞–ї—М–і–µ–≥–Є–і—Л –Њ–±–Њ–Ј–љ–∞—З–∞–ї–Є—Б—М –њ—А–Є –њ–Њ–Љ–Њ—Й–Є —Б—Г—Д—Д–Є–Ї—Б–∞ -–∞–ї [ 8]
–Я—А–Є–Љ–µ—А—Л –љ–∞–Ј–≤–∞–љ–Є–є –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –њ–Њ —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–Њ–Љ–µ–љ–Ї–ї–∞—В—Г—А–µ
–Р–ї—М–і–µ–≥–Є–і—Л –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А—Г—О—В—Б—П —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ (–≤ —Б–Ї–Њ–±–Ї–∞—Е –њ—А–Є–≤–µ–і–µ–љ—Л –њ—А–Є–Љ–µ—А—Л)[ 9]
–Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –љ–∞—Б—Л—Й–µ–љ–љ–Њ—Б—В–Є —Г–≥–ї–µ–≤–Њ–і–Њ—А–Њ–і–љ–Њ–≥–Њ –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—П :
–Я–Њ —З–Є—Б–ї—Г –Ї–∞—А–±–Њ–љ–Є–ї—М–љ—Л—Е –≥—А—Г–њ–њ:
–°—В—А—Г–Ї—В—Г—А–љ–∞—П —Д–Њ—А–Љ—Г–ї–∞ —А–µ—В–Є–љ–∞–ї—П –Я–Є—А–Є–і–Њ–Ї—Б–∞–ї—М –Р–ї—М–і–µ–≥–Є–і–љ–∞—П –≥—А—Г–њ–њ–∞ —Б–Њ–і–µ—А–ґ–Є—В—Б—П –≤–Њ –Љ–љ–Њ–≥–Є—Е –њ—А–Є—А–Њ–і–љ—Л—Е –≤–µ—Й–µ—Б—В–≤–∞—Е, —В–∞–Ї–Є—Е, –Ї–∞–Ї —Г–≥–ї–µ–≤–Њ–і—Л (–∞–ї—М–і–Њ–Ј—Л ), –љ–µ–Ї–Њ—В–Њ—А—Л–µ –≤–Є—В–∞–Љ–Є–љ—Л (—А–µ—В–Є–љ–∞–ї—М , –њ–Є—А–Є–і–Њ–Ї—Б–∞–ї—М ). –Ш—Е —Б–ї–µ–і—Л —Б–Њ–і–µ—А–ґ–∞—В—Б—П –≤ —Н—Д–Є—А–љ—Л—Е –Љ–∞—Б–ї–∞—Е –Є —З–∞—Б—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –Є—Е –њ—А–Є—П—В–љ–Њ–Љ—Г –Ј–∞–њ–∞—Е—Г, –љ–∞–њ—А–Є–Љ–µ—А, –Ї–Њ—А–Є—З–љ—Л–є –∞–ї—М–і–µ–≥–Є–і (–≤ –Ї–∞—Б—Б–Є–µ–≤–Њ–Љ –Љ–∞—Б–ї–µ –µ–≥–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Њ 75 %, –∞ –≤ —Ж–µ–є–ї–Њ–љ—Б–Ї–Њ–Љ –Ї–Њ—А–Є—З–љ–Њ–Љ –Љ–∞—Б–ї–µ –і–∞–ґ–µ –і–Њ 90 %) –Є –≤–∞–љ–Є–ї–Є–љ .
–Р–ї–Є—Д–∞—В–Є—З–µ—Б–Ї–Є–є –∞–ї—М–і–µ–≥–Є–і –°–Э3 (–°–Э2 )7 –°(–Э)=–Ю (—В—А–Є–≤–Є–∞–ї—М–љ–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ вАФ –њ–µ–ї–∞—А–≥–Њ–љ–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і ) —Б–Њ–і–µ—А–ґ–Є—В—Б—П –≤ —Н—Д–Є—А–љ—Л—Е –Љ–∞—Б–ї–∞—Е —Ж–Є—В—А—Г—Б–Њ–≤—Л—Е —А–∞—Б—В–µ–љ–Є–є, –Њ–±–ї–∞–і–∞–µ—В –Ј–∞–њ–∞—Е–Њ–Љ –∞–њ–µ–ї—М—Б–Є–љ–∞, –µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –Ї–∞–Ї –њ–Є—Й–µ–≤–Њ–є –∞—А–Њ–Љ–∞—В–Є–Ј–∞—В–Њ—А[ 10]
–¶–Є—В—А–∞–ї—М —Б–Њ–і–µ—А–ґ–Є—В—Б—П –≤ –ї–µ–Љ–Њ–љ–≥—А–∞—Б—Б–Њ–≤–Њ–Љ –Є –Ї–Њ—А–Є–∞–љ–і—А–Њ–≤–Њ–Љ –Љ–∞—Б–ї–∞—Е (–і–Њ 80 %), —Ж–Є—В—А–Њ–љ–µ–ї–ї–∞–ї—М вАФ –≤ —Ж–Є—В—А–Њ–љ–µ–ї–ї–Њ–≤–Њ–Љ (–њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ 30 %) –Є —Н–≤–Ї–∞–ї–Є–њ—В–Њ–≤–Њ–Љ, –±–µ–љ–Ј–∞–ї—М–і–µ–≥–Є–і вАФ –≤ –Љ–∞—Б–ї–µ –≥–Њ—А—М–Ї–Њ–≥–Њ –Љ–Є–љ–і–∞–ї—П. –Ъ—Г–Љ–Є–љ–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і —Б–Њ–і–µ—А–ґ–Є—В—Б—П –≤ –Љ–∞—Б–ї–µ —В–Љ–Є–љ–∞ , –≥–µ–ї–Є–Њ—В—А–Њ–њ–Є–љ вАФ –≤ –Љ–∞—Б–ї–µ –≥–µ–ї–Є—В—А–Њ–њ–∞ –Є —Б–Є—А–µ–љ–Є, –∞–љ–Є—Б–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і –Є –ґ–∞—Б–Љ–Є–љ–∞–ї—М–і–µ–≥–Є–і –≤ –љ–µ–±–Њ–ї—М—И–Є—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞—Е —Б–Њ–і–µ—А–ґ–∞—В—Б—П –≤–Њ –Љ–љ–Њ–≥–Є—Е —Н—Д–Є—А–љ—Л—Е –Љ–∞—Б–ї–∞—Е[ 1] [ 5]
–Ф–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е —З–∞—Б—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П —А–µ–∞–Ї—Ж–Є—П –Њ–Ї–Є—Б–ї–µ–љ–Є—П –њ–µ—А–≤–Є—З–љ—Л—Е —Б–њ–Є—А—В–Њ–≤ —А–µ–∞–≥–µ–љ—В–∞–Љ–Є, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–Є–Љ–Є —Б–Њ–±–Њ–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –Њ–Ї—Б–Є–і–∞ —Е—А–Њ–Љ–∞(VI) —Б —В—А–µ—В–Є—З–љ—Л–Љ–Є –∞–Љ–Є–љ–∞–Љ–Є , –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –ї—Г—З—И–Є–Љ–Є —А–µ–∞–≥–µ–љ—В–∞–Љ–Є —П–≤–ї—П—О—В—Б—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б —Б –њ–Є—А–Є–і–Є–љ–Њ–Љ (CrO3 ¬Ј 2C5 H5 N, —А–µ–∞–≥–µ–љ—В –°–∞—А—А–µ—В–∞ вАФ –Ъ–Њ–ї–ї–Є–љ–Ј–∞) –Є —Е–ї–Њ—А—Е—А–Њ–Љ–∞—В –њ–Є—А–Є–і–Є–љ–Є—П (C5 H5 NH+ CrO3 Cl- , —А–µ–∞–≥–µ–љ—В –Ъ–Њ—А–Є , PCC). –Ф–∞–љ–љ—Л–µ —А–µ–∞–≥–µ–љ—В—Л –њ–Њ–Ј–≤–Њ–ї—П—О—В –њ–Њ–ї—Г—З–∞—В—М –∞–ї—М–і–µ–≥–Є–і—Л —Б –≤—Л—Б–Њ–Ї–Є–Љ –≤—Л—Е–Њ–і–Њ–Љ, –∞ —Е–ї–Њ—А—Е—А–Њ–Љ–∞—В –њ–Є—А–Є–і–Є–љ–Є—П —В–∞–Ї–ґ–µ –љ–µ –Ј–∞—В—А–∞–≥–Є–≤–∞–µ—В –і–≤–Њ–є–љ—Г—О —Б–≤—П–Ј—М . –Ф–ї—П —Н—В–Є—Е –ґ–µ —Ж–µ–ї–µ–є –њ—А–Є–Љ–µ–љ—П—О—В –Є –і—А—Г–≥–Є–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Њ–Ї–Є—Б–ї–Є—В–µ–ї–Є , –љ–∞–њ—А–Є–Љ–µ—А –Њ–Ї—Б–Є–і –Љ–∞—А–≥–∞–љ—Ж–∞(IV) MnO2 , –Ї–∞—А–±–Њ–љ–∞—В —Б–µ—А–µ–±—А–∞ –љ–∞ —Ж–µ–Њ–ї–Є—В–µ , –∞ —В–∞–Ї–ґ–µ –і–Є–Љ–µ—В–Є–ї—Б—Г–ї—М—Д–Њ–Ї—Б–Є–і –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Њ—Б–љ–Њ–≤–∞–љ–Є—П (–Њ–Ї–Є—Б–ї–µ–љ–Є–µ –њ–Њ –°–≤–µ—А–љ—Г [–∞–љ–≥–ї.] [ 11] –°—Е–µ–Љ–∞ –Њ–Ї–Є—Б–ї–µ–љ–Є—П —Ж–Є—В—А–Њ–љ–µ–ї–ї–Њ–ї–∞ —Е–ї–Њ—А—Е—А–Њ–Љ–∞—В–Њ–Љ –њ–Є—А–Є–і–Є–љ–Є—П –Я–µ—А–Є–Њ–і–Є–љ–∞–љ –Ф–µ—Б—Б–∞-–Ь–∞—А—В–Є–љ–∞ –†–µ–∞–Ї—Ж–Є—П –Њ–Ї–Є—Б–ї–µ–љ–Є—П –њ–µ—А–Є–Њ–і–Є–љ–∞–љ–Њ–Љ –Ф–µ—Б—Б–∞-–Ь–∞—А—В–Є–љ–∞. –Я–µ—А–≤–Є—З–љ—Л–µ —Б–њ–Є—А—В—Л –њ—А–Є —Н—В–Њ–Љ —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ –Њ–Ї–Є—Б–ї—П—О—В—Б—П –і–Њ –∞–ї—М–і–µ–≥–Є–і–Њ–≤.[ 12]
R
− вИТ -->
C
H
2
O
H
→
D
M
P
R
− вИТ -->
C
H
O
{\displaystyle {\mathsf {R{-}CH_{2}OH{\xrightarrow[{DMP}]{}}R{-}CHO}}}
–Ъ–∞–Ї –Љ–µ—В–Њ–і –њ–Њ–ї—Г—З–µ–љ–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ—Л–є –Њ–Ј–Њ–љ–Њ–ї–Є–Ј —Б–Є–Љ–Љ–µ—В—А–Є—З–љ—Л—Е –і–Є–Ј–∞–Љ–µ—Й—С–љ–љ—Л—Е –∞–ї–Ї–µ–љ–Њ–≤ –ї–Є–±–Њ —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є—Е –∞–ї–Ї–µ–љ–Њ–≤ (–≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ —А–µ–∞–Ї—Ж–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –і–Є–∞–ї—М–і–µ–≥–Є–і–∞). –Р–љ–∞–ї–Њ–≥–Є—З–љ–Њ–µ –њ—А–µ–≤—А–∞—Й–µ–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ —Б–Љ–µ—Б–Є OsO4 –Є NaIO4 [ 13] –Т–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ—Л–є –Њ–Ј–Њ–љ–Њ–ї–Є–Ј —Ж–Є–Ї–ї–Њ–≥–µ–Ї—Б–µ–љ–∞
C
H
2
(
O
H
)
− вИТ -->
C
H
2
(
O
H
)
→
H
I
O
4
2
C
H
2
O
{\displaystyle {\mathsf {CH_{2}(OH){-}CH_{2}(OH){\xrightarrow[{HIO_{4}}]{}}2CH_{2}O}}}
–У–Є–і—А–Њ–±–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ вАФ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –≥–µ–Ї—Б–Є–љ–∞-1
–†—П–і –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В (—Е–ї–Њ—А–∞–љ–≥–Є–і—А–Є–і—Л , —Б–ї–Њ–ґ–љ—Л–µ —Н—Д–Є—А—Л , –љ–Є—В—А–Є–ї—Л , –∞–Љ–Є–і—Л ) –Љ–Њ–≥—Г—В –±—Л—В—М –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –і–Њ –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї–µ–є[ 16]
–†–µ–∞–Ї—Ж–Є—П –†–Њ–Ј–µ–љ–Љ—Г–љ–і–∞
–Р—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л –Љ–Њ–≥—Г—В –±—Л—В—М —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ—Л –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –Њ—В–ї–Є—З–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ–Є –љ–∞ —А–µ–∞–Ї—Ж–Є—П—Е –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н–ї–µ–Ї—В—А–Њ—Д–Є–ї—М–љ–Њ–≥–Њ –Ј–∞–Љ–µ—Й–µ–љ–Є—П .
–°—Е–µ–Љ–∞ —А–µ–∞–Ї—Ж–Є–Є –У–∞—В—В–µ—А–Љ–∞–љ–∞ вАФ –Ъ–Њ—Е–∞ –°—Е–µ–Љ–∞ —А–µ–∞–Ї—Ж–Є–Є –Т–Є–ї—М—Б–Љ–µ–є–µ—А–∞ вАФ –•–∞–∞–Ї–∞ –°—Е–µ–Љ–∞ —А–µ–∞–Ї—Ж–Є–Є –°–Њ–Љ–Љ–ї–µ –Р—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л –Љ–Њ–ґ–љ–Њ –њ–Њ–ї—Г—З–∞—В—М –Є–Ј –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В –Њ–±—Й–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є, –Њ–і–љ–∞–Ї–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—В –Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–Ї—Ж–Є–Є. –Э–∞–њ—А–Є–Љ–µ—А, —А–µ–∞–Ї—Ж–Є—П –°—В–µ—Д–µ–љ–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—В—М –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –љ–Є—В—А–Є–ї—Л —Е–ї–Њ—А–Є–і–Њ–Љ –Њ–ї–Њ–≤–∞(II) SnCl2 —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –≥–Є–і—А–Њ–ї–Є–Ј–Њ–Љ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ—Г –∞–ї—М–і–µ–≥–Є–і—Г[ 20]
–Р–ї—М–і–µ–≥–Є–і—Л —В–∞–Ї–ґ–µ –Љ–Њ–ґ–љ–Њ –њ–Њ–ї—Г—З–∞—В—М —А–µ–∞–Ї—Ж–Є—П–Љ–Є –≥–Є–і—А–∞—В–∞—Ж–Є–Є –∞–ї–Ї–Є–љ–Њ–≤ (—А–µ–∞–Ї—Ж–Є—П –Ъ—Г—З–µ—А–Њ–≤–∞ ), –њ–Є—А–Њ–ї–Є–Ј–Њ–Љ –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В –Є –Є—Е —Б–Љ–µ—Б–µ–є –≤ –≤–Є–і–µ –њ–∞—А–Њ–≤ –љ–∞–і –Њ–Ї—Б–Є–і–∞–Љ–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Љ–µ—В–∞–ї–ї–Њ–≤ (ThO2 , MnO2 , CaO , ZnO ) –њ—А–Є 400вАФ500 ¬∞C, –≥–Є–і—А–Њ–ї–Є–Ј–Њ–Љ –≥–µ–Љ–Є–љ–∞–ї—М–љ—Л—Е –і–Є–≥–∞–ї–Њ–≥–µ–љ–Њ–њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е (–µ—Б–ї–Є –∞—В–Њ–Љ—Л –≥–∞–ї–Њ–≥–µ–љ–∞ –љ–∞—Е–Њ–і—П—В—Б—П —Г –Њ–і–љ–Њ–≥–Њ –Є–Ј –Ї—А–∞–є–љ–Є—Е –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞) –Є –і—А—Г–≥–Є–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є[ 9]
–Ш–Ј–≤–µ—Б—В–љ–Њ –Љ–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–Њ–≤ —Б–Є–љ—В–µ–Ј–∞ –∞–ї—М–і–µ–≥–Є–і–Њ–≤, –Њ–і–љ–∞–Ї–Њ –Є—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≤ –њ—А–Њ–Љ—Л—И–ї–µ–љ–љ–Њ—Б—В–Є –Ј–∞–≤–Є—Б–Є—В –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ—В –і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Б—Л—А—М—П. –Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–Њ–Љ—Л—И–ї–µ–љ–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –њ–Њ–ї—Г—З–µ–љ–Є—П –љ–∞—Б—Л—Й–µ–љ–љ—Л—Е –∞–ї–Є—Д–∞—В–Є—З–µ—Б–Ї–Є—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤ —П–≤–ї—П—О—В—Б—П[ 21]
–Ґ–∞–Ї–ґ–µ –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –љ–µ–Ї–Њ—В–Њ—А—Л–µ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ —Б–Є–љ—В–µ–Ј—Л –∞–ї—М–і–µ–≥–Є–і–Њ–≤, —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –≤ –њ–∞—А—Д—О–Љ–µ—А–љ–Њ–є –њ—А–Њ–Љ—Л—И–ї–µ–љ–љ–Њ—Б—В–Є [ 21]
–Ю–Ї—Б–Њ—Б–Є–љ—В–µ–Ј —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–Љ –њ—А–Њ—Ж–µ—Б—Б–Њ–Љ –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ —Б —В—А–µ–Љ—П –∞—В–Њ–Љ–∞–Љ–Є —Г–≥–ї–µ—А–Њ–і–∞ –Є –≤—Л—И–µ. –Т —Н—В–Њ–є —А–µ–∞–Ї—Ж–Є–Є –∞–ї–Ї–µ–љ—Л —А–µ–∞–≥–Є—А—Г—О—В —Б —Б–Є–љ—В–µ–Ј-–≥–∞–Ј–Њ–Љ (CO + H2 ) —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–ї—М–і–µ–≥–Є–і–∞, —Б–Њ–і–µ—А–ґ–∞—Й–µ–≥–Њ –љ–∞ –Њ–і–Є–љ –∞—В–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ –±–Њ–ї—М—И–µ, —З–µ–Љ –Є—Б—Е–Њ–і–љ—Л–є –∞–ї–Ї–µ–љ. –Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –љ–µ—Б–Є–Љ–Љ–µ—В—А–Є—З–љ—Л—Е –∞–ї–Ї–µ–љ–Њ–≤ –Њ–±—А–∞–Ј—Г–µ—В—Б—П —Б–Љ–µ—Б—М –њ—А–Њ–і—Г–Ї—В–Њ–≤, —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е –Љ–Њ–ґ–љ–Њ –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –њ—Г—В—С–Љ –њ–Њ–і–±–Њ—А–∞ –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–∞[ 21]
–У–Є–і—А–Њ—Д–Њ—А–Љ–Є–ї–Є—А–Њ–≤–∞–љ–Є–µ –њ—А–Њ–њ–µ–љ–∞ –°—А–µ–і–Є –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Њ—В—Й–µ–њ–ї–µ–љ–Є—П –≤–Њ–і–Њ—А–Њ–і–∞ –Њ—В –њ–µ—А–≤–Є—З–љ—Л—Е —Б–њ–Є—А—В–Њ–≤ —А–∞–Ј–ї–Є—З–∞—О—В –і–µ–≥–Є–і—А–Є—А–Њ–≤–∞–љ–Є–µ, –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –Є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–µ –і–µ–≥–Є–і—А–Є—А–Њ–≤–∞–љ–Є–µ. –Ф–µ–≥–Є–і—А–Є—А–Њ–≤–∞–љ–Є–µ —Б–њ–Є—А—В–Њ–≤ –њ—А–Њ–≤–Њ–і—П—В –њ—А–Є –∞—В–Љ–Њ—Б—Д–µ—А–љ–Њ–Љ –і–∞–≤–ї–µ–љ–Є–Є –Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ 250вАФ400 ¬∞–° –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Љ–µ–і–љ–Њ–≥–Њ –Є–ї–Є —Б–µ—А–µ–±—А—П–љ–Њ–≥–Њ –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–∞ . –Т —Е–Њ–і–µ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤—Л–і–µ–ї—П–µ—В—Б—П –≤–Њ–і–Њ—А–Њ–і , –Ї–Њ—В–Њ—А—Л–є –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –±–µ–Ј –Њ—З–Є—Б—В–Ї–Є –≤ –і—А—Г–≥–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е. –Ф–µ–≥–Є–і—А–Є—А–Њ–≤–∞–љ–Є–µ –Є–Љ–µ–µ—В –Ї–Њ–Љ–Љ–µ—А—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –њ–Њ–ї—Г—З–µ–љ–Є–Є —Г–Ї—Б—Г—Б–љ–Њ–≥–Њ –∞–ї—М–і–µ–≥–Є–і–∞ –Є–Ј —Н—В–∞–љ–Њ–ї–∞ : —А–µ–∞–Ї—Ж–Є—О –њ—А–Њ–≤–Њ–і—П—В –њ—А–Є 270вАФ300 ¬∞–° –љ–∞ –Љ–µ–і–љ–Њ–Љ –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–µ, –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —Ж–µ—А–Є–µ–Љ , –њ—А–Є —Н—В–Њ–Љ –Ј–∞ —Ж–Є–Ї–ї –њ—А–µ–≤—А–∞—Й–∞–µ—В—Б—П 25вАФ50 % —Н—В–∞–љ–Њ–ї–∞ —Б —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О 90вАФ95 %. –Я–Њ–±–Њ—З–љ—Л–Љ–Є –њ—А–Њ–і—Г–Ї—В–∞–Љ–Є —П–≤–ї—П—О—В—Б—П —Н—В–Є–ї–∞—Ж–µ—В–∞—В , —Н—В–Є–ї–µ–љ , –Ї—А–Њ—В–Њ–љ–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і –Є –≤—Л—Б—И–Є–µ —Б–њ–Є—А—В—Л. –Ю–Ї–Є—Б–ї–µ–љ–Є–µ —Б–њ–Є—А—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –≤ –Є–Ј–±—Л—В–Ї–µ –≤–Њ–Ј–і—Г—Е–∞ –Є–ї–Є –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –њ—А–Є 350вАФ450 ¬∞–° –љ–∞ –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–µ, —Б–Њ–і–µ—А–ґ–∞—Й–µ–Љ –Њ–Ї—Б–Є–і—Л –ґ–µ–ї–µ–Ј–∞ –Є –Љ–Њ–ї–Є–±–і–µ–љ–∞ . –Я—А–Њ—Ж–µ—Б—Б –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–µ —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–∞ . –Ф–∞–љ–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л —В–∞–Ї–ґ–µ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –≤ —Б–Є–љ—В–µ–Ј–µ –і—Г—И–Є—Б—В—Л—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤[ 21]
–Ю–Ї–Є—Б–ї–µ–љ–Є–µ –∞–ї–Ї–µ–љ–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ—А–Њ–Љ—Л—И–ї–µ–љ–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –њ–Њ–ї—Г—З–µ–љ–Є—П –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і–∞ –Є –∞–Ї—А–Њ–ї–µ–Є–љ–∞ . –Т –њ–µ—А–≤–Њ–Љ —Б–ї—Г—З–∞–µ –Њ–Ї–Є—Б–ї–µ–љ–Є—О –њ–Њ–і–≤–µ—А–≥–∞–µ—В—Б—П —Н—В–Є–ї–µ–љ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Е–ї–Њ—А–Є–і–Њ–≤ –њ–∞–ї–ї–∞–і–Є—П –Є –Љ–µ–і–Є –Т–∞–Ї–µ—А-–њ—А–Њ—Ж–µ—Б—Б [ 21] [ 9]
C
H
2
=
C
H
2
+
P
d
C
l
2
+
H
2
O
→ вЖТ -->
C
H
3
C
H
O
+
P
d
+
2
H
C
l
{\displaystyle {\mathsf {CH_{2}{\text{=}}CH_{2}+PdCl_{2}+H_{2}O\rightarrow CH_{3}CHO+Pd+2HCl}}}
P
d
+
2
C
u
C
l
2
→ вЖТ -->
P
d
C
l
2
+
2
C
u
C
l
{\displaystyle {\mathsf {Pd+2CuCl_{2}\rightarrow PdCl_{2}+2CuCl}}}
4
C
u
C
l
+
4
H
C
l
+
O
2
→ вЖТ -->
4
C
u
C
l
2
+
2
H
2
O
{\displaystyle {\mathsf {4CuCl+4HCl+O_{2}\rightarrow 4CuCl_{2}+2H_{2}O}}}
–Я—А–Њ—Ж–µ—Б—Б –њ–Њ–ї—Г—З–µ–љ–Є—П –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і–∞, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л–є –љ–∞ –≥–Є–і—А–∞—В–∞—Ж–Є–Є –∞—Ж–µ—В–Є–ї–µ–љ–∞ , –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –њ–Њ—В–µ—А—П–ї –±—Л–ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –Я–Њ—Б–ї–µ–і–љ–Є–µ —Д–∞–±—А–Є–Ї–Є –≤ –Ч–∞–њ–∞–і–љ–Њ–є –Х–≤—А–Њ–њ–µ, —Б–Є–љ—В–µ–Ј–Є—А—Г—О—Й–Є–µ –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і –њ–Њ –і–∞–љ–љ–Њ–є —Б—Е–µ–Љ–µ, –±—Л–ї–Є –Ј–∞–Ї—А—Л—В—Л –≤ 1980 –≥–Њ–і—Г. –Я—А–Є—З–Є–љ–Њ–є —Н—В–Њ–Љ—Г –њ–Њ—Б–ї—Г–ґ–Є–ї–∞ –±–ЊћБ–ї—М—И–∞—П –і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М —Н—В–Є–ї–µ–љ–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—Л—А—М—П, –∞ —В–∞–Ї–ґ–µ —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–∞ вАФ —Б—Г–ї—М—Д–∞—В–∞ —А—В—Г—В–Є [ 21]
–Х–ґ–µ–≥–Њ–і–љ–Њ–µ –Љ–Є—А–Њ–≤–Њ–µ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–Њ —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–∞ (–њ–Њ –і–∞–љ–љ—Л–Љ –љ–∞ 1996 –≥–Њ–і) —Б–Њ—Б—В–∞–≤–Є–ї–Њ 8,7¬Ј106 —В[ 22] 6 —В[ 23]
–Ю—Б–љ–Њ–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –њ–Њ–ї—Г—З–µ–љ–Є—П –±–µ–љ–Ј–∞–ї—М–і–µ–≥–Є–і–∞ —П–≤–ї—П–µ—В—Б—П –≥–Є–і—А–Њ–ї–Є–Ј –±–µ–љ–Ј–∞–ї—М—Е–ї–Њ—А–Є–і–∞ –≤ –Ї–Є—Б–ї–Њ–є –Є–ї–Є —Й–µ–ї–Њ—З–љ–Њ–є —Б—А–µ–і–∞—Е. –Т –Ї–∞—З–µ—Б—В–≤–µ –≥–Є–і—А–Њ–ї–Є–Ј—Г—О—Й–Є—Е –∞–≥–µ–љ—В–Њ–≤ –Љ–Њ–≥—Г—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –≥–Є–і—А–Њ–Ї—Б–Є–і –Ї–∞–ї—М—Ж–Є—П , –Ї–∞—А–±–Њ–љ–∞—В –Ї–∞–ї—М—Ж–Є—П , –≥–Є–і—А–Њ–Ї–∞—А–±–Њ–љ–∞—В –љ–∞—В—А–Є—П , –Ї–∞—А–±–Њ–љ–∞—В –љ–∞—В—А–Є—П , –∞ —В–∞–Ї–ґ–µ —А–∞–Ј–ї–Є—З–љ—Л–µ –Ї–Є—Б–ї–Њ—В—Л —Б –і–Њ–±–∞–≤–ї–µ–љ–Є–µ–Љ —Б–Њ–ї–µ–є –Љ–µ—В–∞–ї–ї–Њ–≤. –Ш—Б—Е–Њ–і–љ–Њ–µ —Б—Л—А—М—С, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –њ–Њ–ї—Г—З–∞—О—В –њ—А–Є —Е–ї–Њ—А–Є—А–Њ–≤–∞–љ–Є–Є —В–Њ–ї—Г–Њ–ї–∞ –≤ –±–Њ–Ї–Њ–≤—Г—О —Ж–µ–њ—М. –Ь–µ–љ–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—С–љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –Њ—Б–љ–Њ–≤–∞–љ –љ–∞ —З–∞—Б—В–Є—З–љ–Њ–Љ –Њ–Ї–Є—Б–ї–µ–љ–Є–Є —В–Њ–ї—Г–Њ–ї–∞[ 24]
–§–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –≥–∞–Ј–Њ–Њ–±—А–∞–Ј–љ–Њ–µ –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ –≤–µ—Й–µ—Б—В–≤–Њ. –Р–ї—М–і–µ–≥–Є–і—Л –і–Њ –°12 вАФ –ґ–Є–і–Ї–Њ—Б—В–Є, –∞ –∞–ї—М–і–µ–≥–Є–і—Л –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Б—В—А–Њ–µ–љ–Є—П —Б –±–Њ–ї–µ–µ –і–ї–Є–љ–љ—Л–Љ –љ–µ—А–∞–Ј–≤–µ—В–≤–ї—С–љ–љ—Л–Љ —Г–≥–ї–µ—А–Њ–і–љ—Л–Љ —Б–Ї–µ–ї–µ—В–Њ–Љ —П–≤–ї—П—О—В—Б—П —В–≤—С—А–і—Л–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є.
–Ґ–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Ї–Є–њ–µ–љ–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ —Б –љ–µ—А–∞–Ј–≤–µ—В–≤–ї—С–љ–љ—Л–Љ —Б—В—А–Њ–µ–љ–Є–µ–Љ —Г–≥–ї–µ—А–Њ–і–љ–Њ–є —Ж–µ–њ–Є –≤—Л—И–µ, —З–µ–Љ —Г –Є—Е –Є–Ј–Њ–Љ–µ—А–Њ–≤. –Э–∞–њ—А–Є–Љ–µ—А, –≤–∞–ї–µ—А–Є–∞–љ–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і –Ї–Є–њ–Є—В –њ—А–Є 100,4 ¬∞C, –∞ –Є–Ј–Њ–≤–∞–ї–µ—А–Є–∞–љ–Њ–≤—Л–є вАФ –њ—А–Є 92,5 ¬∞C. –Ю–љ–Є –Ї–Є–њ—П—В –њ—А–Є –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є—Е —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞—Е, —З–µ–Љ —Б–њ–Є—А—В—Л —Б —В–µ–Љ –ґ–µ —З–Є—Б–ї–Њ–Љ —Г–≥–ї–µ—А–Њ–і–љ—Л—Е –∞—В–Њ–Љ–Њ–≤, –љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Њ–њ–Є–Њ–љ–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і –Ї–Є–њ–Є—В –њ—А–Є 48,8 ¬∞C, –∞ –њ—А–Њ–њ–∞–љ–Њ–ї-1 –њ—А–Є 97,8 ¬∞C. –≠—В–Њ –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –∞–ї—М–і–µ–≥–Є–і—Л, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В —Б–њ–Є—А—В–Њ–≤ , –љ–µ —П–≤–ї—П—О—В—Б—П —Б–Є–ї—М–љ–Њ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –ґ–Є–і–Ї–Њ—Б—В—П–Љ–Є[ 9] –њ–µ—А–µ–≥–Њ–љ–Ї–Њ–є [ 25] —Г–≥–ї–µ–≤–Њ–і–Њ—А–Њ–і–Њ–≤ —Б —В–Њ–є –ґ–µ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –Љ–∞—Б—Б–Њ–є, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Є—Е –≤—Л—Б–Њ–Ї–Њ–є –њ–Њ–ї—П—А–љ–Њ—Б—В—М—О[ 9]
–Т—П–Ј–Ї–Њ—Б—В—М , –њ–ї–Њ—В–љ–Њ—Б—В—М –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –њ—А–µ–ї–Њ–Љ–ї–µ–љ–Є—П –њ—А–Є 20 ¬∞C —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В—Б—П —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Љ–Њ–ї—П—А–љ–Њ–є –Љ–∞—Б—Б—Л –∞–ї—М–і–µ–≥–Є–і–Њ–≤. –Э–Є–Ј—И–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л —П–≤–ї—П—О—В—Б—П –њ–Њ–і–≤–Є–ґ–љ—Л–Љ–Є –ґ–Є–і–Ї–Њ—Б—В—П–Љ–Є, –∞ –∞–ї—М–і–µ–≥–Є–і—Л –Њ—В –≥–µ–њ—В–∞–љ–∞–ї—П –і–Њ —Г–љ–і–µ–Ї–∞–љ–∞–ї—П –Є–Љ–µ—О—В –Љ–∞—Б–ї–Њ–Њ–±—А–∞–Ј–љ—Г—О –Ї–Њ–љ—Б–Є—Б—В–µ–љ—Ж–Є—О[ 25]
–§–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і –Є –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ–Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ —Б–Љ–µ—И–Є–≤–∞—О—В—Б—П —Б –≤–Њ–і–Њ–є, –Њ–і–љ–∞–Ї–Њ, —Б —А–Њ—Б—В–Њ–Љ –і–ї–Є–љ—Л —Г–≥–ї–µ—А–Њ–і–љ–Њ–≥–Њ —Б–Ї–µ–ї–µ—В–∞, —А–∞—Б—В–≤–Њ—А–Є–Љ–Њ—Б—В—М –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –≤ –≤–Њ–і–µ —Б–Є–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П, –љ–∞–њ—А–Є–Љ–µ—А, —А–∞—Б—В–≤–Њ—А–Є–Љ–Њ—Б—В—М –≥–µ–Ї—Б–∞–љ–∞–ї—П –њ—А–Є 20 ¬∞–° —Б–Њ—Б—В–∞–≤–ї—П–µ—В –ї–Є—И—М 0,6 % –њ–Њ –Љ–∞—Б—Б–µ. –Р–ї–Є—Д–∞—В–Є—З–µ—Б–Ї–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л —А–∞—Б—В–≤–Њ—А–Є–Љ—Л –≤ —Б–њ–Є—А—В–∞—Е , –њ—А–Њ—Б—В—Л—Е —Н—Д–Є—А–∞—Е –Є –і—А—Г–≥–Є—Е —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—С–љ–љ—Л—Е –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—В–≤–Њ—А–Є—В–µ–ї—П—Е [ 25]
–Э–Є–Ј—И–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л –Є–Љ–µ—О—В —А–µ–Ј–Ї–Є–є –Ј–∞–њ–∞—Е, –∞ –≤—Л—Б—И–Є–µ –≥–Њ–Љ–Њ–ї–Њ–≥–Є (–°8 -–°13 ) —П–≤–ї—П—О—В—Б—П –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –Љ–љ–Њ–≥–Є—Е –њ–∞—А—Д—О–Љ–µ—А–љ—Л—Е –Є–Ј–і–µ–ї–Є–є[ 25]
–§–Є–Ј–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤ [ 26] [ 27]
–Э–∞–Ј–≤–∞–љ–Є–µ
–§–Њ—А–Љ—Г–ї–∞
–Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –њ–ї–∞–≤–ї–µ–љ–Є—П, ¬∞C
–Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –Ї–Є–њ–µ–љ–Є—П, ¬∞C
–Я–ї–Њ—В–љ–Њ—Б—В—М, –≥/—Б–Љ¬≥ (–њ—А–Є 20 ¬∞C)
–§–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і
HCHO
вИТ93
вИТ21
0,82 (–њ—А–Є вАУ20 ¬∞–°)
–Р—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і
CH3 CHO
вИТ123
21
0,778
–Я—А–Њ–њ–∞–љ–∞–ї—М
CH3 CH2 CHO
вИТ81
49
0,797
–С—Г—В–∞–љ–∞–ї—М
CH3 CH2 CH2 CHO
вИТ99
76
0,803
–Р–Ї—А–Њ–ї–µ–Є–љ
CH2 =CHвАУCHO
вИТ88
53
0,841
–Ъ—А–Њ—В–Њ–љ–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і
CH3 -CH=CHвАУCHO
вИТ74
104
0,852
–С–µ–љ–Ј–∞–ї—М–і–µ–≥–Є–і
C6 H5 CHO
вИТ56
179
1,05
–°–∞–ї–Є—Ж–Є–ї–Њ–≤—Л–є –∞–ї—М–і–µ–≥–Є–і
–Њ -HOвАУC6 H4 CHO
2
197
1,16
–Т–∞–љ–Є–ї–Є–љ
82
285
вАФ
–Р—В–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ –≤ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –љ–∞—Е–Њ–і–Є—В—Б—П –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є sp2 -–≥–Є–±—А–Є–і–Є–Ј–∞—Ж–Є–Є
–Ф–≤–Њ–є–љ–∞—П —Б–≤—П–Ј—М –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л —Б—Е–Њ–і–љ–∞ –њ–Њ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –њ—А–Є—А–Њ–і–µ —Б –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј—М—О –Љ–µ–ґ–і—Г —Г–≥–ї–µ—А–Њ–і–љ—Л–Љ–Є –∞—В–Њ–Љ–∞–Љ–Є, –Њ–і–љ–∞–Ї–Њ –≤ —В–Њ –ґ–µ –≤—А–µ–Љ—П —Н–љ–µ—А–≥–Є—П —Б–≤—П–Ј–Є –°=–Ю (749,4 –Ї–Ф–ґ /–Љ–Њ–ї—М ) –±–Њ–ї—М—И–µ, —З–µ–Љ —Н–љ–µ—А–≥–Є—П –і–≤—Г—Е –њ—А–Њ—Б—В—Л—Е —Б–≤—П–Ј–µ–є (2√Ч358 –Ї–Ф–ґ/–Љ–Њ–ї—М) C-O. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Ї–Є—Б–ї–Њ—А–Њ–і —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ —Н–ї–µ–Ї—В—А–Њ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–Љ —Н–ї–µ–Љ–µ–љ—В–Њ–Љ, —З–µ–Љ —Г–≥–ї–µ—А–Њ–і, –Є –њ–Њ—В–Њ–Љ—Г —Н–ї–µ–Ї—В—А–Њ–љ–љ–∞—П –њ–ї–Њ—В–љ–Њ—Б—В—М –≤–±–ї–Є–Ј–Є –∞—В–Њ–Љ–∞ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –±–Њ–ї—М—И–µ, —З–µ–Љ –≤–±–ї–Є–Ј–Є –∞—В–Њ–Љ–∞ —Г–≥–ї–µ—А–Њ–і–∞. –Ф–Є–њ–Њ–ї—М–љ—Л–є –Љ–Њ–Љ–µ–љ—В –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л —Б–Њ—Б—В–∞–≤–ї—П–µ—В ~9вЛЕ10вИТ30 –Ъ–ї¬Ј–Љ [ 9] [ 14]
–Я–Њ–ї—П—А–Є–Ј–∞—Ж–Є—П –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є ¬Ђ—Г–≥–ї–µ—А–Њ–і-–Ї–Є—Б–ї–Њ—А–Њ–і¬ї –њ–Њ –њ—А–Є–љ—Ж–Є–њ—Г –Љ–µ–Ј–Њ–Љ–µ—А–љ–Њ–≥–Њ —Б–Њ–њ—А—П–ґ–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Ј–∞–њ–Є—Б–∞—В—М —Б–ї–µ–і—Г—О—Й–Є–µ —А–µ–Ј–Њ–љ–∞–љ—Б–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л :
–†–µ–Ј–Њ–љ–∞–љ—Б–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л –і–ї—П –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л –Я–Њ–і–Њ–±–љ–Њ–µ —А–∞–Ј–і–µ–ї–µ–љ–Є–µ –Ј–∞—А—П–і–Њ–≤ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —Д–Є–Ј–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ–њ—А–µ–і–µ–ї—П–µ—В —А–µ–∞–Ї—Ж–Є–Њ–љ–љ—Г—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Ї–∞–Ї –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ—Д–Є–ї–Њ–≤ –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–Љ –≤—Б—В—Г–њ–∞—В—М –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –љ—Г–Ї–ї–µ–Њ—Д–Є–ї—М–љ–Њ–≥–Њ –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П [ 28]
–Т—Л—Б–Њ–Ї–∞—П —А–µ–∞–Ї—Ж–Є–Њ–љ–љ–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б–≤—П–Ј–∞–љ–∞ —Б –љ–∞–ї–Є—З–Є–µ–Љ –њ–Њ–ї—П—А–љ–Њ–є —Б–≤—П–Ј–Є –°=–Ю. –Р–ї—М–і–µ–≥–Є–і—Л —П–≤–ї—П—О—В—Б—П –ґ—С—Б—В–Ї–Є–Љ–Є –Њ—Б–љ–Њ–≤–∞–љ–Є—П–Љ–Є –Ы—М—О–Є—Б–∞ –Є, –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —Н—В–Є–Љ, –∞—В–Њ–Љ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –≤ –љ–Є—Е –Љ–Њ–ґ–µ—В –Ї–Њ–Њ—А–і–Є–љ–Є—А–Њ–≤–∞—В—М—Б—П —Б –ґ—С—Б—В–Ї–Є–Љ–Є –Ї–Є—Б–ї–Њ—В–∞–Љ–Є: H+ , ZnCl2 , BF3 , AlCl3 –Є —В. –і.[ 14] –Ї–µ—В–Њ–љ–∞–Љ , –Њ–і–љ–∞–Ї–Њ –∞–ї—М–і–µ–≥–Є–і—Л –њ—А–Њ—П–≤–ї—П—О—В –±–ЊћБ–ї—М—И—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї—М—И–µ–є –њ–Њ–ї—П—А–Є–Ј–∞—Ж–Є–µ–є —Б–≤—П–Ј–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –і–ї—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ —Е–∞—А–∞–Ї—В–µ—А–љ—Л —А–µ–∞–Ї—Ж–Є–Є, –љ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П –Ї–µ—В–Њ–љ–Њ–≤, –љ–∞–њ—А–Є–Љ–µ—А –≥–Є–і—А–∞—В–∞—Ж–Є—П –≤ –≤–Њ–і–љ–Њ–Љ —А–∞—Б—В–≤–Њ—А–µ.
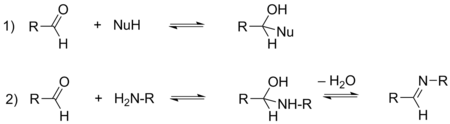
–Р–ї—М–і–µ–≥–Є–і—Л —Б–Њ–і–µ—А–ґ–∞—В –њ–Њ–ї—П—А–Є–Ј–Њ–≤–∞–љ–љ—Г—О –Ї–∞—А–±–Њ–љ–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г –Є —Б–Ї–ї–Њ–љ–љ—Л –њ—А–Є—Б–Њ–µ–і–Є–љ—П—В—М –љ—Г–Ї–ї–µ–Њ—Д–Є–ї—М–љ—Л–µ —А–µ–∞–≥–µ–љ—В—Л , –Ї–∞–Ї –љ–µ–є—В—А–∞–ї—М–љ—Л–µ (–∞–Љ–Љ–Є–∞–Ї , –∞–Љ–Є–љ—Л , –≤–Њ–і—Г , —Б–њ–Є—А—В—Л , —В–Є–Њ–ї—Л –Є –і—А.), —В–∞–Ї –Є –∞–љ–Є–Њ–љ–љ—Л–µ (—Ж–Є–∞–љ–Є–і-–Є–Њ–љ CN- , –∞–ї–Ї–Њ–≥–Њ–ї—П—В—Л , –≥–Є–і—А–Є–і-–Є–Њ–љ H- , –Ї–∞—А–±–∞–љ–Є–Њ–љ—Л –Є –і—А.). –Ч–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ —А–µ–∞–Ї—Ж–Є–є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –≥–Є–і—А–Є–і–∞–Љ–Є —В–Є–њ–∞ –∞–ї—О–Љ–Њ–≥–Є–і—А–Є–і–∞ –ї–Є—В–Є—П LiAlH4 , –∞ —В–∞–Ї–ґ–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б —А–µ–∞–Ї—В–Є–≤–∞–Љ–Є –У—А–Є–љ—М—П—А–∞, –і–∞–љ–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л —П–≤–ї—П—О—В—Б—П –Њ–±—А–∞—В–Є–Љ—Л–Љ–Є . –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —В–∞–Ї–ґ–µ —А–∞–Ј–ї–Є—З–∞—В—М –і–≤–∞ —В–Є–њ–∞ –Њ–±—А–∞—В–Є–Љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П: –њ–µ—А–≤—Л–є —В–Є–њ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О —В–µ—В—А–∞—Н–і—А–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞ –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П, –∞ –≤—В–Њ—А–Њ–є —В–Є–њ –≤–Ї–ї—О—З–∞–µ—В –≤ —Б–µ–±—П —В–∞–Ї–ґ–µ –њ–Њ—Б–ї–µ–і—Г—О—Й—Г—О —А–µ–∞–Ї—Ж–Є—О –і–µ–≥–Є–і—А–∞—В–∞—Ж–Є–Є , –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Ї–Њ—В–Њ—А–Њ–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г —Н–ї–µ–Ї—В—А–Њ—Д–Є–ї—М–љ—Л–Љ –∞—В–Њ–Љ–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ –Є –љ—Г–Ї–ї–µ–Њ—Д–Є–ї–Њ–Љ. –†–µ–∞–Ї—Ж–Є–Є –≤—В–Њ—А–Њ–≥–Њ —В–Є–њ–∞ —Е–∞—А–∞–Ї—В–µ—А–љ—Л, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ, –і–ї—П –∞–Ј–Њ—В—Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –љ—Г–Ї–ї–µ–Њ—Д–Є–ї–Њ–≤[ 29]
–Ю–±—Й–∞—П —Б—Е–µ–Љ–∞ –љ—Г–Ї–ї–µ–Њ—Д–Є–ї—М–љ–Њ–≥–Њ –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П –Ї –∞–ї—М–і–µ–≥–Є–і–∞–Љ –Т –і–∞–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є—П—Е –∞–ї—М–і–µ–≥–Є–і—Л —П–≤–ї—П—О—В—Б—П –±–Њ–ї–µ–µ —А–µ–∞–Ї—Ж–Є–Њ–љ–љ–Њ—Б–њ–Њ—Б–Њ–±–љ—Л–Љ–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–µ—В–Њ–љ–∞–Љ–Є. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї—М—И–µ–є —В–µ—А–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М—О –Ї–µ—В–Њ–љ–Њ–≤, –∞ —В–∞–Ї–ґ–µ –Љ–µ–љ—М—И–Є–Љ–Є –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ—Л–Љ–Є –Ј–∞—В—А—Г–і–љ–µ–љ–Є—П–Љ–Є –≤ —Б–ї—Г—З–∞–µ –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П –Ї –∞–ї—М–і–µ–≥–Є–і–∞–Љ[ 29]
–Я—А–Њ—Б—В–µ–є—И–µ–є –Љ–Њ–і–µ–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є –і–∞–љ–љ–Њ–≥–Њ —В–Є–њ–∞ —П–≤–ї—П–µ—В—Б—П —А–µ–∞–Ї—Ж–Є—П –≥–Є–і—А–∞—В–∞—Ж–Є–Є –∞–ї—М–і–µ–≥–Є–і–Њ–≤, –њ—А–Њ—В–µ–Ї–∞—О—Й–∞—П –≤ –Є—Е –≤–Њ–і–љ—Л—Е —А–∞—Б—В–≤–Њ—А–∞—Е. –°–Њ–≥–ї–∞—Б–љ–Њ –њ—А–∞–≤–Є–ї—Г –≠–ї—М—В–µ–Ї–Њ–≤–∞ вАФ –≠—А–ї–µ–љ–Љ–µ–є–µ—А–∞, –Њ–±—А–∞–Ј—Г—О—Й–Є–µ—Б—П –њ—А–Є —Н—В–Њ–Љ 1,1-–і–Є–Њ–ї—Л –љ–µ—Г—Б—В–Њ–є—З–Є–≤—Л –Є —Б –Њ—В—Й–µ–њ–ї–µ–љ–Є–µ–Љ –Љ–Њ–ї–µ–Ї—Г–ї—Л –≤–Њ–і—Л –њ—А–µ–≤—А–∞—Й–∞—О—В—Б—П –Њ–±—А–∞—В–љ–Њ –≤ –Є—Б—Е–Њ–і–љ—Л–µ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П. –У–Є–і—А–∞—В–∞—Ж–Є—П –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≤ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –ї–Є—И—М –і–ї—П –љ–Є–Ј—И–Є—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤. –Ґ–∞–Ї, —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і –≥–Є–і—А–∞—В–Є—А–Њ–≤–∞–љ –љ–∞ 99,999 %, –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і вАФ –љ–∞ 58 %. –Ъ–Њ–≥–і–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –Ј–∞—А—П–і –љ–∞ –∞—В–Њ–Љ–µ —Г–≥–ї–µ—А–Њ–і–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –≤ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –Ј–∞ —Б—З—С—В —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –љ–Є–Љ —А–∞–і–Є–Ї–∞–ї–Њ–≤, 1,1-–і–Є–Њ–ї—Л —Б—В–∞–љ–Њ–≤—П—В—Б—П —Г—Б—В–Њ–є—З–Є–≤—Л–Љ–Є –Є –Љ–Њ–≥—Г—В –±—Л—В—М –≤—Л–і–µ–ї–µ–љ—Л (–љ–∞–њ—А–Є–Љ–µ—А, —Е–ї–Њ—А–∞–ї—М –ї–µ–≥–Ї–Њ –њ—А–Є—Б–Њ–µ–і–Є–љ—П–µ—В –≤–Њ–і—Г —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ–≥–Њ –∞–і–і—Г–Ї—В–∞ вАФ —Е–ї–Њ—А–∞–ї—М–≥–Є–і—А–∞—В–∞ ). –†–µ–∞–Ї—Ж–Є—П –≥–Є–і—А–∞—В–∞—Ж–Є–Є –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г–µ—В—Б—П –Ї–∞–Ї –Ї–Є—Б–ї–Њ—В–∞–Љ–Є , —В–∞–Ї –Є –Њ—Б–љ–Њ–≤–∞–љ–Є—П–Љ–Є [ 14] [ 30]
–У–Є–і—А–∞—В–∞—Ж–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Я–Њ–і–Њ–±–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –њ—А–Њ—В–µ–Ї–∞–µ—В –Є —А–µ–∞–Ї—Ж–Є—П –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П —Б–њ–Є—А—В–Њ–≤ –њ–Њ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ, –Є–Љ–µ—О—Й–∞—П –≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–Љ —Б–Є–љ—В–µ–Ј–µ –і–ї—П –Ј–∞—Й–Є—В—Л –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л. –Я–µ—А–≤–Є—З–љ—Л–є –њ—А–Њ–і—Г–Ї—В –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П –љ–∞–Ј—Л–≤–∞–µ—В—Б—П –њ–Њ–ї—Г–∞—Ж–µ—В–∞–ї–µ–Љ , –і–∞–ї–µ–µ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Ї–Є—Б–ї–Њ—В—Л –Њ–љ –њ—А–µ–≤—А–∞—Й–∞–µ—В—Б—П –≤ –∞—Ж–µ—В–∞–ї—М . –Я—А–Є —Б—В–Њ—П–љ–Є–Є –∞–ї—М–і–µ–≥–Є–і—Л —В–∞–Ї–ґ–µ –Њ–±—А–∞–Ј—Г—О—В —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ –Є–ї–Є –њ–Њ–ї–Є–Љ–µ—А–љ—Л–µ –∞—Ж–µ—В–∞–ї–Є (–љ–∞–њ—А–Є–Љ–µ—А, —В—А–Є–Њ–Ї—Б–∞–љ –Є–ї–Є –њ–∞—А–∞—Д–Њ—А–Љ –і–ї—П —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–∞ –Є –њ–∞—А–∞–ї—М–і–µ–≥–Є–і –і–ї—П –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і–∞ ). –Я—А–Є –љ–∞–≥—А–µ–≤–∞–љ–Є–Є —Н—В–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є —Б–Њ —Б–ї–µ–і–Њ–≤—Л–Љ–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞–Љ–Є –Ї–Є—Б–ї–Њ—В –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –і–µ–њ–Њ–ї–Є–Љ–µ—А–Є–Ј–∞—Ж–Є—П –Є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—П –Є—Б—Е–Њ–і–љ—Л—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤[ 31]
–Я–Њ–ї—Г—З–µ–љ–Є–µ –∞—Ж–µ—В–∞–ї–µ–є –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –њ—А–µ–≤—А–∞—Й–µ–љ–Є—П –њ—А–Њ–Є—Б—Е–Њ–і—П—В —В–∞–Ї–ґ–µ —Б —Г—З–∞—Б—В–Є–µ–Љ —Б–µ—А–Њ—Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –∞–љ–∞–ї–Њ–≥–Њ–≤ —Б–њ–Є—А—В–Њ–≤ вАФ —В–Є–Њ–ї–Њ–≤ ; –Њ–љ–Є –њ—А–Є–≤–Њ–і—П—В, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Ї —В–Є–Њ–∞—Ж–µ—В–∞–ї—П–Љ , —В–∞–Ї–ґ–µ –Є–≥—А–∞—О—Й–Є–Љ –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —В–Њ–љ–Ї–Њ–Љ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–Љ —Б–Є–љ—В–µ–Ј–µ[ 31]
–Р–ї—М–і–µ–≥–Є–і—Л –Љ–Њ–≥—Г—В –њ—А–Є—Б–Њ–µ–і–Є–љ—П—В—М —Ж–Є–∞–љ–Њ–≤–Њ–і–Њ—А–Њ–і HCN —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —Ж–Є–∞–љ–≥–Є–і—А–Є–љ–Њ–≤ , –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –≤ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–Љ —Б–Є–љ—В–µ–Ј–µ –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П ќ±,ќ≤-–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є, ќ±-–≥–Є–і—А–Њ–Ї—Б–Є–Ї–Є—Б–ї–Њ—В, ќ±-–∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В . –Ф–∞–љ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П —В–∞–Ї–ґ–µ —П–≤–ї—П–µ—В—Б—П –Њ–±—А–∞—В–Є–Љ–Њ–є –Є –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г–µ—В—Б—П –Њ—Б–љ–Њ–≤–∞–љ–Є—П–Љ–Є. –Т –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е —Ж–Є–∞–љ–Њ–≤–Њ–і–Њ—А–Њ–і (—В. –Ї–Є–њ. 26 ¬∞C) –Њ–±—Л—З–љ–Њ –њ–Њ–ї—Г—З–∞—О—В –і–µ–є—Б—В–≤–Є–µ–Љ —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Љ–Є–љ–µ—А–∞–ї—М–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–∞ —Ж–Є–∞–љ–Є–і –љ–∞—В—А–Є—П –Є–ї–Є –Ї–∞–ї–Є—П [ 32]
–Я–Њ–ї—Г—З–µ–љ–Є–µ —Ж–Є–∞–љ–≥–Є–і—А–Є–љ–Њ–≤ –Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–±–Њ–ї—М—И–Є–µ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ—Л–µ –Ј–∞—В—А—Г–і–љ–µ–љ–Є—П –њ—А–Є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–Є –љ—Г–Ї–ї–µ–Њ—Д–Є–ї–Њ–≤ –Ї –∞–ї—М–і–µ–≥–Є–і–∞–Љ –њ–Њ–Ј–≤–Њ–ї—П—О—В –њ—А–µ–≤—А–∞—Й–∞—В—М –Є—Е –≤ –±–Є—Б—Г–ї—М—Д–Є—В–љ—Л–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –±–Њ–ї—М—И–Њ–≥–Њ –Є–Ј–±—Л—В–Ї–∞ –≥–Є–і—А–Њ—Б—Г–ї—М—Д–Є—В–∞ –љ–∞—В—А–Є—П NaHSO3 . –Ф–∞–љ–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–µ –≤–µ—Й–µ—Б—В–≤–∞ –Є —З–∞—Б—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –і–ї—П –≤—Л–і–µ–ї–µ–љ–Є—П, –Њ—З–Є—Б—В–Ї–Є –Є–ї–Є —Е—А–∞–љ–µ–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ–Њ—Б–ї–µ–і–љ–Є–µ –Љ–Њ–≥—Г—В –±—Л—В—М –ї–µ–≥–Ї–Њ –Є–Ј –љ–Є—Е —А–µ–≥–µ–љ–µ—А–Є—А–Њ–≤–∞–љ—Л –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Ї–Є—Б–ї–Њ—В—Л –Є–ї–Є –Њ—Б–љ–Њ–≤–∞–љ–Є—П[ 32]
–Я–Њ–ї—Г—З–µ–љ–Є–µ –±–Є—Б—Г–ї—М—Д–Є—В–љ—Л—Е –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –†–µ–∞–Ї—Ж–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ —Б –Љ–∞–≥–љ–Є–є - –Є –ї–Є—В–Є–є–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Њ–µ–і–Є–љ–µ–љ–Є—П–Љ–Є –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –≤—В–Њ—А–Є—З–љ—Л—Е —Б–њ–Є—А—В–Њ–≤ (–≤ —Б–ї—Г—З–∞–µ —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–∞ вАФ –њ–µ—А–≤–Є—З–љ—Л—Е). –Я—А–Њ—Ж–µ—Б—Б –Љ–Њ–ґ–µ—В –Њ—Б–ї–Њ–ґ–љ—П—В—М—Б—П –њ–Њ–±–Њ—З–љ—Л–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є –µ–љ–Њ–ї–Є–Ј–∞—Ж–Є–Є –Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–≥–Њ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–≤–Њ–і—П—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –≤—Л—Е–Њ–і–∞. –Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –ї–Є—В–Є–є–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є —Н—В–Є –њ–Њ–Љ–µ—Е–Є —Г–і–∞—С—В—Б—П —Г—Б—В—А–∞–љ–Є—В—М[ 33]
–†–µ–∞–Ї—Ж–Є—П —Б –Љ–∞–≥–љ–Є–є–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Њ–µ–і–Є–љ–µ–љ–Є—П–Љ–Є –†–µ–∞–Ї—Ж–Є—П —Б –Љ–∞–≥–љ–Є–є–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Њ–µ–і–Є–љ–µ–љ–Є—П–Љ–Є –Я—А–Є —А–µ–∞–Ї—Ж–Є–Є –∞–ї—М–і–µ–≥–Є–і–Њ–≤ —Б –њ–µ—А–≤–Є—З–љ—Л–Љ–Є –Є –≤—В–Њ—А–Є—З–љ—Л–Љ–Є –∞–Љ–Є–љ–∞–Љ–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Є–Љ–Є–љ–Њ–≤ –Є –µ–љ–∞–Љ–Є–љ–Њ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Т –Њ—Б–љ–Њ–≤–µ –Њ–±–µ–Є—Е —А–µ–∞–Ї—Ж–Є–є –ї–µ–ґ–Є—В –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –љ—Г–Ї–ї–µ–Њ—Д–Є–ї—М–љ—Л—Е —А–µ–∞–≥–µ–љ—В–Њ–≤ –њ–Њ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –Њ—В—Й–µ–њ–ї–µ–љ–Є–µ–Љ –≤–Њ–і—Л –Њ—В –њ–Њ–ї—Г—З–µ–љ–љ–Њ–≥–Њ —В–µ—В—А–∞—Н–і—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—В–µ—А–Љ–µ–і–Є–∞—В–∞. –†–µ–∞–Ї—Ж–Є—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Є–Љ–Є–љ–Њ–≤ —В—А–µ–±—Г–µ—В –Ї–Є—Б–ї–Њ—В–љ–Њ–≥–Њ –Ї–∞—В–∞–ї–Є–Ј–∞ –Є –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ—А–Њ—В–µ–Ї–∞–µ—В –≤ –Њ–±–ї–∞—Б—В–Є pH –Њ—В 3 –і–Њ 5. –Ф–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –µ–љ–∞–Љ–Є–љ–Њ–≤ —Б —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–Љ –≤—Л—Е–Њ–і–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –∞–Ј–µ–Њ—В—А–Њ–њ–љ—Г—О –Њ—В–≥–Њ–љ–Ї—Г –≤–Њ–і—Л, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–Љ–µ—Б—В–Є—В—М —А–∞–≤–љ–Њ–≤–µ—Б–Є–µ –≤ —Б—В–Њ—А–Њ–љ—Г –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ—А–Њ–і—Г–Ї—В–∞. –Ю–±—Л—З–љ–Њ –≤ –Ї–∞—З–µ—Б—В–≤–µ –≤—В–Њ—А–Є—З–љ—Л—Е –∞–Љ–Є–љ–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ –∞–Љ–Є–љ—Л (–њ–Є—А—А–Њ–ї–Є–і–Є–љ , –њ–Є–њ–µ—А–Є–і–Є–љ –Є–ї–Є –Љ–Њ—А—Д–Њ–ї–Є–љ )[ 34]
–Я–Њ–ї—Г—З–µ–љ–Є–µ –Є–Љ–Є–љ–Њ–≤ –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –∞–ї—М–і–µ–≥–Є–і—Л —А–µ–∞–≥–Є—А—Г—О—В —Б –≥–Є–і—А–Њ–Ї—Б–Є–ї–∞–Љ–Є–љ–Њ–Љ , –≥–Є–і—А–∞–Ј–Є–љ–Њ–Љ , 2,4-–і–Є–љ–Є—В—А–Њ—Д–µ–љ–Є–ї–≥–Є–і—А–∞–Ј–Є–љ–Њ–Љ , —Б–µ–Љ–Є–Ї–∞—А–±–∞–Ј–Є–і–Њ–Љ –Є –і—А—Г–≥–Є–Љ–Є –њ–Њ–і–Њ–±–љ—Л–Љ–Є —Б–Њ–µ–і–Є–љ–µ–љ–Є—П–Љ–Є. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ–Њ–ї—Г—З–∞–µ–Љ—Л—Е –њ—А–Є —Н—В–Њ–Љ —Б–Њ–µ–і–Є–љ–µ–љ–Є–є —П–≤–ї—П—О—В—Б—П –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–Љ–Є –Є –Љ–Њ–≥—Г—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –і–ї—П –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є–Є –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –њ–Њ —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ –њ–ї–∞–≤–ї–µ–љ–Є—П –Є –і—А—Г–≥–Є–Љ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞–Љ. –Ґ–∞–Ї–ґ–µ —Н—В–Є —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –љ–∞—Е–Њ–і—П—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–Љ —Б–Є–љ—В–µ–Ј–µ, –љ–∞–њ—А–Є–Љ–µ—А, –≥–Є–і—А–∞–Ј–Њ–љ—Л –Љ–Њ–≥—Г—В –±—Л—В—М –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –њ–Њ —А–µ–∞–Ї—Ж–Є–Є –Ъ–Є–ґ–љ–µ—А–∞ вАФ –Т–Њ–ї—М—Д–∞ [ 34]
–Я–Њ–ї—Г—З–µ–љ–Є–µ —Д—Г—А–∞—Ж–Є–ї–Є–љ–∞
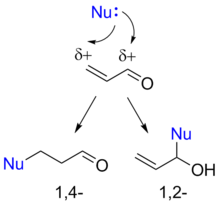
–Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –Ї ќ±,ќ≤-–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л–Љ –∞–ї—М–і–µ–≥–Є–і–∞–Љ –Љ–Њ–ґ–µ—В –њ—А–Њ—В–µ–Ї–∞—В—М —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ 1,2- –Є 1,4-–њ—А–Њ–і—Г–Ї—В–Њ–≤ –Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –љ—Г–Ї–ї–µ–Њ—Д–Є–ї—М–љ—Л—Е —А–µ–∞–≥–µ–љ—В–Њ–≤ –Ї ќ±,ќ≤-–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л–Љ –∞–ї—М–і–µ–≥–Є–і–∞–Љ –Љ–Њ–ґ–µ—В –њ—А–Њ—В–µ–Ї–∞—В—М –Ї–∞–Ї –њ–Њ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ, —В–∞–Ї –Є –њ–Њ ¬Ђ—З–µ—В–≤—С—А—В–Њ–Љ—Г¬ї –њ–Њ–ї–Њ–ґ–µ–љ–Є—О —Б–Њ–њ—А—П–ґ—С–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Я—А–Є—З–Є–љ–∞ —Н—В–Њ–≥–Њ –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ –і–≤–Њ–є–љ–∞—П —Г–≥–ї–µ—А–Њ–і-—Г–≥–ї–µ—А–Њ–і–љ–∞—П —Б–≤—П–Ј—М –њ–Њ–ї—П—А–Є–Ј—Г–µ—В—Б—П –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –њ–Њ–ї—П—А–љ–Њ–є –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л (–Љ–µ–Ј–Њ–Љ–µ—А–љ—Л–є —Н—Д—Д–µ–Ї—В ), –Є –і–∞–ї—М–љ–Є–є –Њ—В –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л –∞—В–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є –њ—А–Є–Њ–±—А–µ—В–∞–µ—В —З–∞—Б—В–Є—З–љ—Л–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –Ј–∞—А—П–і. –†–µ–∞–Ї—Ж–Є—П –љ—Г–Ї–ї–µ–Њ—Д–Є–ї–∞ —Б –і–∞–љ–љ—Л–Љ –∞—В–Њ–Љ–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ –љ–∞–Ј—Л–≤–∞–µ—В—Б—П —Б–Њ–њ—А—П–ґ—С–љ–љ—Л–Љ –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ–Љ, –Є–ї–Є 1,4-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ–Љ. –Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –Ї –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ –∞–љ–∞–ї–Њ–≥–Є–Є –љ–∞–Ј—Л–≤–∞—О—В 1,2-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ–Љ. –§–Њ—А–Љ–∞–ї—М–љ—Л–Љ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ 1,4-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –љ—Г–Ї–ї–µ–Њ—Д–Є–ї–∞ –њ–Њ —Г–≥–ї–µ—А–Њ–і-—Г–≥–ї–µ—А–Њ–і–љ–Њ–є –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є. –Т–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е 1,2- –Є 1,4-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ —П–≤–ї—П—О—В—Б—П –Ї–Њ–љ–Ї—Г—А–Є—А—Г—О—Й–Є–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є, –Њ–і–љ–∞–Ї–Њ –Є–љ–Њ–≥–і–∞ —Г–і–∞—С—В—Б—П –њ—А–Њ–≤–Њ–і–Є—В—М —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є —Б –њ–Њ–ї—Г—З–µ–љ–Є–µ–Љ –њ—А–Њ–і—Г–Ї—В–Њ–≤ 1,2- –ї–Є–±–Њ 1,4-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П[ 35]
–Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –њ–µ—А–≤–Є—З–љ—Л—Е –Є –≤—В–Њ—А–Є—З–љ—Л—Е –∞–Љ–Є–љ–Њ–≤ –Ї ќ±,ќ≤-–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л–Љ –∞–ї—М–і–µ–≥–Є–і–∞–Љ –њ—А–Њ—В–µ–Ї–∞–µ—В –≤ –Љ—П–≥–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –Є –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О 1,4-–њ—А–Њ–і—Г–Ї—В–∞. –Э–∞–њ—А–Њ—В–Є–≤, –≤ —Б–ї—Г—З–∞–µ —Ж–Є–∞–љ–Њ–≤–Њ–і–Њ—А–Њ–і–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Њ–±–Њ–Є—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –њ—А–Њ–і—Г–Ї—В–∞ 1,2-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П. –І—В–Њ–±—Л –≤ –і–∞–љ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –Є—Б–Ї–ї—О—З–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М 1,2-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П, –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–є —А–µ–∞–≥–µ–љ—В вАФ –і–Є—Н—В–Є–ї–∞–ї—О–Љ–Є–љ–Є–є—Ж–Є–∞–љ–Є–і (C2 H5 )2 AlCN[ 36]
–Ы–Є—В–Є–є–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –њ—А–Є—Б–Њ–µ–і–Є–љ—П—О—В—Б—П –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –њ–Њ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ, –і–∞–≤–∞—П –∞–ї–ї–Є–ї–Њ–≤—Л–µ —Б–њ–Є—А—В—Л. –°–Њ–њ—А—П–ґ—С–љ–љ–Њ–µ –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –њ—А–Њ–≤–Њ–і—П—В –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Љ–µ–і—М–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–≥–µ–љ—В–Њ–≤ вАФ –і–Є–∞–ї–Ї–Є–ї–Ї—Г–њ—А–∞—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –≤–≤–µ—Б—В–Є –≤ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –љ–µ —В–Њ–ї—М–Ї–Њ –њ–µ—А–≤–Є—З–љ—Г—О, –љ–Њ —В–∞–Ї–ґ–µ –≤—В–Њ—А–Є—З–љ—Г—О –Є–ї–Є —В—А–µ—В–Є—З–љ—Г—О –∞–ї–Ї–Є–ї—М–љ—Г—О , –∞–ї–Ї–µ–љ–Є–ї—М–љ—Г—О –Є–ї–Є –∞—А–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г. –Ь–∞–≥–љ–Є–є–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–≥–µ–љ—В—Л (—А–µ–∞–Ї—В–Є–≤—Л –У—А–Є–љ—М—П—А–∞ ), –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –Є–Ј –Љ–∞–≥–љ–Є—П —Б–≤–µ—А—Е–≤—Л—Б–Њ–Ї–Њ–є —З–Є—Б—В–Њ—В—Л, —В–∞–Ї–ґ–µ –њ—А–Є—Б–Њ–µ–і–Є–љ—П—О—В—Б—П —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ 1,2-–њ—А–Њ–і—Г–Ї—В–Њ–≤, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Њ–±—Л–Ї–љ–Њ–≤–µ–љ–љ—Л–µ —А–µ–∞–Ї—В–Є–≤—Л –У—А–Є–љ—М—П—А–∞, –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –Є–Ј-–Ј–∞ –њ—А–Є–Љ–µ—Б–µ–є –і—А—Г–≥–Є—Е –Љ–µ—В–∞–ї–ї–Њ–≤ (–љ–∞–њ—А–Є–Љ–µ—А, –Љ–µ–і–Є –Є –ґ–µ–ї–µ–Ј–∞ ) –≤—Б—В—Г–њ–∞—О—В –Є –≤ 1,2-, –Є –≤ 1,4-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ, —З—В–Њ —А–µ–≥—Г–ї–Є—А—Г–µ—В—Б—П –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Љ–∞–≥–љ–Є–є–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–≥–µ–љ—В—Л —Г—В—А–∞—В–Є–ї–Є —Б–≤–Њ—С –Ј–љ–∞—З–µ–љ–Є–µ –≤ –і–∞–љ–љ–Њ–є –Њ–±–ї–∞—Б—В–Є[ 37]
–С–Њ—А–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П (—В—А–Є–∞–ї–Ї–Є–ї–±–Њ—А–∞–љ—Л) —А–µ–∞–≥–Є—А—Г—О—В —Б –љ–µ–њ—А–µ–і–µ–ї—М–љ—Л–Љ–Є –∞–ї—М–і–µ–≥–Є–і–∞–Љ–Є, –і–∞–≤–∞—П –њ—А–Њ–і—Г–Ї—В—Л 1,4-–њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П[ 38]
–Р–ї—М–і–µ–≥–Є–і—Л –≤—Б—В—Г–њ–∞—О—В –≤ —А–µ–∞–Ї—Ж–Є—О —Б –≥–∞–ї–Њ–≥–µ–љ–∞–Љ–Є (—Е–ї–Њ—А–Њ–Љ , –±—А–Њ–Љ–Њ–Љ –Є–ї–Є –Є–Њ–і–Њ–Љ ), –Њ–±—А–∞–Ј—Г—П –≥–∞–ї–Њ–≥–µ–љ–њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ, –њ—А–Є —Н—В–Њ–Љ –≥–∞–ї–Њ–≥–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –≤ ќ±-–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ (–≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, —Б–Њ—Б–µ–і–љ–µ–µ —Б –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є)[ 39]
–Р–ї—М–і–µ–≥–Є–і—Л –њ—А–Њ—П–≤–ї—П—О—В —Б–≤–Њ–є—Б—В–≤–∞ —Б–ї–∞–±—Л—Е –Ї–Є—Б–ї–Њ—В: –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Њ—Б–љ–Њ–≤–∞–љ–Є–є –Њ–љ–Є —Б–њ–Њ—Б–Њ–±–љ—Л –Њ—В—Й–µ–њ–ї—П—В—М –њ—А–Њ—В–Њ–љ –Њ—В ќ±-–Љ–µ—В–Є–ї–µ–љ–Њ–≤–Њ–є –≥—А—Г–њ–њ—Л, –њ—А–µ–≤—А–∞—Й–∞—П—Б—М –≤ –µ–љ–Њ–ї—П—В-–Є–Њ–љ . –Ю–±—Л—З–љ–Њ –і–ї—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –њ–Њ–ї–љ–Њ–≥–Њ –і–µ–њ—А–Њ—В–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Б–Є–ї—М–љ—Л–µ –Њ—Б–љ–Њ–≤–∞–љ–Є—П (–≥–Є–і—А–Є–і –љ–∞—В—А–Є—П , –≥–Є–і—А–Є–і –Ї–∞–ї–Є—П , –і–Є–Є–Ј–Њ–њ—А–Њ–њ–Є–ї–∞–Љ–Є–і –ї–Є—В–Є—П –Є –і—А.) –≤ –∞–њ—А–Њ—В–Њ–љ–љ—Л—Е —А–∞—Б—В–≤–Њ—А–Є—В–µ–ї—П—Е (—В–µ—В—А–∞–≥–Є–і—А–Њ—Д—Г—А–∞–љ , –Ф–Ь–°–Ю ). –Я—А–µ–≤—А–∞—Й–µ–љ–Є–µ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –≤ –µ–љ–Њ–ї—М–љ—Г—О —Д–Њ—А–Љ—Г –њ—А–Њ—В–µ–Ї–∞–µ—В –Є –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–Є–ї—М–љ—Л—Е –Њ—Б–љ–Њ–≤–∞–љ–Є–є. –Ю–±—А–∞–Ј—Г—О—Й–Є–µ—Б—П –њ—А–Є —Н—В–Њ–Љ –µ–љ–Њ–ї—Л , –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–∞–Љ–љ–Њ–≥–Њ –Љ–µ–љ–µ–µ —Б—В–∞–±–Є–ї—М–љ—Л, —З–µ–Љ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–∞—П —Д–Њ—А–Љ–∞, –љ–∞–њ—А–Є–Љ–µ—А, –і–ї—П –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і–∞ –Ї–Њ–љ—Б—В–∞–љ—В–∞ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П вАФ —В–Њ–ї—М–Ї–Њ 6вЛЕ10вИТ5 –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ[ 40] –Ї–µ—В–Њ-–µ–љ–Њ–ї—М–љ–Њ–є —В–∞—Г—В–Њ–Љ–µ—А–Є–µ–є [ 41]
–Ъ–µ—В–Њ-–µ–љ–Њ–ї—М–љ–∞—П —В–∞—Г—В–Њ–Љ–µ—А–Є—П –С–ї–∞–≥–Њ–і–∞—А—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—В—М –µ–љ–Њ–ї—П—В-–Є–Њ–љ—Л –∞–ї—М–і–µ–≥–Є–і—Л –≤—Б—В—Г–њ–∞—О—В –≤ —А—П–і —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є, –≥–і–µ —Н—В–Є —З–∞—Б—В–Є—Ж—Л –≤—Л—Б—В—Г–њ–∞—О—В –Ї–∞–Ї –љ—Г–Ї–ї–µ–Њ—Д–Є–ї—Л . –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –і–ї—П –љ–Є—Е —Е–∞—А–∞–Ї—В–µ—А–љ—Л —А–µ–∞–Ї—Ж–Є–Є –Ї–Њ–љ–і–µ–љ—Б–∞—Ж–Є–Є. –Т —Б–ї–∞–±–Њ–Њ—Б–љ–Њ–≤–љ–Њ–є —Б—А–µ–і–µ (–≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –∞—Ж–µ—В–∞—В–∞ , –Ї–∞—А–±–Њ–љ–∞—В–∞ –Є–ї–Є —Б—Г–ї—М—Д–Є—В–∞ –Ї–∞–ї–Є—П ) –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –∞–ї—М–і–Њ–ї—М–љ–Њ–є –Ї–Њ–љ–і–µ–љ—Б–∞—Ж–Є–Є , –≤ —Е–Њ–і–µ –Ї–Њ—В–Њ—А–Њ–є —З–∞—Б—В—М –Љ–Њ–ї–µ–Ї—Г–ї –∞–ї—М–і–µ–≥–Є–і–∞ –≤—Л—Б—В—Г–њ–∞–µ—В –Ї–∞–Ї –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–∞—П –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ (—А–µ–∞–≥–Є—А—Г–µ—В –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є), –∞ —З–∞—Б—В—М –Љ–Њ–ї–µ–Ї—Г–ї –∞–ї—М–і–µ–≥–Є–і–∞ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Њ—Б–љ–Њ–≤–∞–љ–Є—П –њ—А–µ–≤—А–∞—Й–∞–µ—В—Б—П –≤ –µ–љ–Њ–ї—П—В-–Є–Њ–љ—Л –Є –≤—Л—Б—В—Г–њ–∞–µ—В –Ї–∞–Ї –Љ–µ—В–Є–ї–µ–љ–Њ–≤–∞—П –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ (–≤—Б—В—Г–њ–∞–µ—В –≤ —А–µ–∞–Ї—Ж–Є—О ќ±-–Љ–µ—В–Є–ї–µ–љ–Њ–≤—Л–Љ –Ј–≤–µ–љ–Њ–Љ). –Ю–±—А–∞–Ј—Г—О—Й–Є–є—Б—П –∞–ї—М–і–Њ–ї—М –њ—А–Є –љ–∞–≥—А–µ–≤–∞–љ–Є–Є –Њ—В—Й–µ–њ–ї—П–µ—В –≤–Њ–і—Г —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ ќ±,ќ≤-–љ–µ–њ—А–µ–і–µ–ї—М–љ–Њ–≥–Њ –∞–ї—М–і–µ–≥–Є–і–∞ (–њ–µ—А–µ—Е–Њ–і –Њ—В –њ—А–µ–і–µ–ї—М–љ–Њ–≥–Њ –∞–ї—М–і–µ–≥–Є–і–∞ –Ї –љ–µ–њ—А–µ–і–µ–ї—М–љ–Њ–Љ—Г —З–µ—А–µ–Ј –∞–ї—М–і–Њ–ї—М –љ–∞–Ј—Л–≤–∞–µ—В—Б—П –Ї—А–Њ—В–Њ–љ–Њ–≤–Њ–є –Ї–Њ–љ–і–µ–љ—Б–∞—Ж–Є–µ–є –Є–ї–Є –∞–ї—М–і–Њ–ї—М–љ–Њ-–Ї—А–Њ—В–Њ–љ–Њ–≤–Њ–є –Ї–Њ–љ–і–µ–љ—Б–∞—Ж–Є–µ–є )[ 9] [ 42]
–Р–ї—М–і–Њ–ї—М–љ–Њ-–Ї—А–Њ—В–Њ–љ–Њ–≤–∞—П –Ї–Њ–љ–і–µ–љ—Б–∞—Ж–Є—П –њ–µ–љ—В–∞–љ–∞–ї—П –Я—А–Є —А–µ–∞–Ї—Ж–Є–Є –Љ–µ–ґ–і—Г –і–≤—Г–Љ—П —А–∞–Ј–љ—Л–Љ–Є –∞–ї—М–і–µ–≥–Є–і–∞–Љ–Є –Њ–±—А–∞–Ј—Г–µ—В—Б—П —Б–Љ–µ—Б—М —З–µ—В—Л—А—С—Е —А–∞–Ј–ї–Є—З–љ—Л—Е –∞–ї—М–і–Њ–ї–µ–є. –Ш—Б–Ї–ї—О—З–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–ї—П—О—В —Б–ї—Г—З–∞–Є, –Ї–Њ–≥–і–∞ —А–∞–Ј–і–µ–ї–µ–љ–Є–µ —А–µ–∞–≥–µ–љ—В–Њ–≤ –љ–∞ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ—Г—О –Є –Љ–µ—В–Є–ї–µ–љ–Њ–≤—Г—О –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Г –Њ—З–µ–≤–Є–і–љ–Њ (–љ–∞–њ—А–Є–Љ–µ—А, –Њ–і–Є–љ –Є–Ј –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –љ–µ —Б–Њ–і–µ—А–ґ–Є—В ќ±-–Љ–µ—В–Є–ї–µ–љ–Њ–≤–Њ–≥–Њ –Ј–≤–µ–љ–∞ –Є –Љ–Њ–ґ–µ—В –≤—Л–њ–Њ–ї–љ—П—В—М —А–Њ–ї—М —В–Њ–ї—М–Ї–Њ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л). –†–∞–Ј—А–∞–±–Њ—В–∞–љ—Л —В–∞–Ї–ґ–µ –Љ–µ—В–Њ–і—Л –њ–Њ–≤—Л—И–µ–љ–Є—П —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ–і–Њ–±–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є. –Я–µ—А–µ–Ї—А—С—Б—В–љ–∞—П –Ї–Њ–љ–і–µ–љ—Б–∞—Ж–Є—П –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤ —Б –Ї–µ—В–Њ–љ–∞–Љ–Є, –њ–Њ–ї—Г—З–Є–ї–∞ –љ–∞–Ј–≤–∞–љ–Є–µ —А–µ–∞–Ї—Ж–Є–Є –Ъ–ї—П–є–Ј–µ–љ–∞ вАФ –®–Љ–Є–і—В–∞ [ 42] —А–µ–∞–Ї—Ж–Є—П –Ъ–љ—С–≤–µ–љ–∞–≥–µ–ї—П , —А–µ–∞–Ї—Ж–Є—П –Ґ–Є—Й–µ–љ–Ї–Њ , —А–µ–∞–Ї—Ж–Є—П –Я–µ—А–Ї–Є–љ–∞ , –±–µ–љ–Ј–Њ–Є–љ–Њ–≤–∞—П –Ї–Њ–љ–і–µ–љ—Б–∞—Ж–Є—П –Є –і—А—Г–≥–Є–µ[ 1]
–Ю–Ї–Є—Б–ї–µ–љ–Є–µ –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –і–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В –Ї–Є—Б–ї–Њ—А–Њ–і–Њ–Љ –њ—А–Њ—В–µ–Ї–∞–µ—В –њ–Њ —А–∞–і–Є–Ї–∞–ї—М–љ–Њ-—Ж–µ–њ–љ–Њ–Љ—Г –Љ–µ—Е–∞–љ–Є–Ј–Љ—Г (–∞–≤—В–Њ–Њ–Ї–Є—Б–ї–µ–љ–Є–µ ) —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ вАФ –њ–µ—А–Њ–Ї—Б–Њ–Ї–Є—Б–ї–Њ—В.
–Р–ї—М–і–µ–≥–Є–і—Л –ї–µ–≥–Ї–Њ –Њ–Ї–Є—Б–ї—П—О—В—Б—П –і–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л—Е –Њ–Ї–Є—Б–ї–Є—В–µ–ї–µ–є. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –њ–µ—А–Љ–∞–љ–≥–∞–љ–∞—В –Ї–∞–ї–Є—П , –∞ —В–∞–Ї–ґ–µ —А–µ–∞–≥–µ–љ—В –Ф–ґ–Њ–љ—Б–∞ (CrO3 + H2 SO4 ), –Ї–Њ—В–Њ—А—Л–є –і–∞—С—В –љ–∞–Є–ї—Г—З—И–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л (–≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –њ—А–Є –љ–Є–Ј–Ї–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –±–Њ–ї–µ–µ —З–µ–Љ 80%-—Л–є –≤—Л—Е–Њ–і –Ї–∞—А–±–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л). –†–µ–∞–≥–µ–љ—В –Ф–ґ–Њ–љ—Б–∞ —В–∞–Ї–ґ–µ –љ–µ –ї–Є—И—С–љ –љ–µ–і–Њ—Б—В–∞—В–Ї–Њ–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –Њ–љ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б–µ–ї–µ–Ї—В–Є–≤–µ–љ –Є –Њ–Ї–Є—Б–ї—П–µ—В –і—А—Г–≥–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –≥—А—Г–њ–њ—Л, –∞ –Ї–Є—Б–ї–∞—П —Б—А–µ–і–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ–є –Є–Ј–Њ–Љ–µ—А–Є–Ј–∞—Ж–Є–Є –Є–ї–Є —А–∞–Ј–ї–Њ–ґ–µ–љ–Є—О —Б—Г–±—Б—В—А–∞—В–∞[ 43]
–Ю–Ї–Є—Б–ї–µ–љ–Є–µ –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –њ–Њ –Ф–ґ–Њ–љ—Б—Г –Ш–Ј–±–µ–ґ–∞—В—М —Н—В–Є—Е –њ—А–Њ–±–ї–µ–Љ –Љ–Њ–ґ–љ–Њ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –±–Њ–ї–µ–µ –Љ—П–≥–Ї–Њ–≥–Њ –Њ–Ї–Є—Б–ї–Є—В–µ–ї—П вАФ —А–µ–∞–Ї—В–Є–≤–∞ –Ґ–Њ–ї–ї–µ–љ—Б–∞ (–∞–Љ–Љ–Є–∞—З–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ –Њ–Ї—Б–Є–і–∞ —Б–µ—А–µ–±—А–∞ ), –Ї–Њ—В–Њ—А—Л–є –љ–µ –Ј–∞—В—А–∞–≥–Є–≤–∞–µ—В –Ї—А–∞—В–љ—Л–µ —Б–≤—П–Ј–Є –Є –≥–Є–і—А–Њ–Ї—Б–Є–ї—М–љ—Л–µ –≥—А—Г–њ–њ—Л —Б–њ–Є—А—В–Њ–≤. –≠—В–∞ —А–µ–∞–Ї—Ж–Є—П —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –і–ї—П –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ (—А–µ–∞–Ї—Ж–Є—П ¬Ђ—Б–µ—А–µ–±—А—П–љ–Њ–≥–Њ –Ј–µ—А–Ї–∞–ї–∞¬ї)[ 43]
–Ю–Ї–Є—Б–ї–µ–љ–Є–µ —Д—Г—А—Д—Г—А–Њ–ї–∞ —А–µ–∞–Ї—В–Є–≤–Њ–Љ –Ґ–Њ–ї–ї–µ–љ—Б–∞ –Ю–Ї–Є—Б–ї–µ–љ–Є–µ –Љ–µ—В–Є–ї–µ–љ–Њ–≤—Л—Е –≥—А—Г–њ–њ –≤ ќ±-–њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –і–Є–Њ–Ї—Б–Є–і–Њ–Љ —Б–µ–ї–µ–љ–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О 1,2-–і–Є–Ї–∞—А–±–Њ–љ–Є–ї—М–љ—Л—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є[ 14] [ 43]
–Р–ї—М–і–µ–≥–Є–і—Л –Љ–µ–і–ї–µ–љ–љ–Њ –Њ–Ї–Є—Б–ї—П—О—В—Б—П –љ–∞ –≤–Њ–Ј–і—Г—Е–µ –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ. –≠—В–Њ—В —А–∞–і–Є–Ї–∞–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б —Г—Б–Ї–Њ—А—П–µ—В—Б—П –њ—А–Є –Њ–±–ї—Г—З–µ–љ–Є–Є –Є–ї–Є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Є–Њ–љ–Њ–≤ Fe2+ . –Р—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –Њ–Ї–Є—Б–ї–µ–љ–Є—О –ї–µ–≥—З–µ, —З–µ–Љ –∞–ї–Є—Д–∞—В–Є—З–µ—Б–Ї–Є–µ. –Ф–∞–љ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –љ–µ –Є–Љ–µ–µ—В —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П, –Њ–і–љ–∞–Ї–Њ –µ—С –њ—А–Њ—В–µ–Ї–∞–љ–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –њ—А–Є —Е—А–∞–љ–µ–љ–Є–Є –∞–ї—М–і–µ–≥–Є–і–Њ–≤: –ґ–µ–ї–∞—В–µ–ї—М–љ–Њ —Е—А–∞–љ–Є—В—М –Є—Е –≤ —В–µ–Љ–љ–Њ—В–µ –Є –Є–љ–µ—А—В–љ–Њ–є –∞—В–Љ–Њ—Б—Д–µ—А–µ[ 44]
–Р—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л —В–∞–Ї–ґ–µ –Њ–Ї–Є—Б–ї—П—О—В—Б—П –і–Њ –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В –Є–ї–Є —Б–ї–Њ–ґ–љ—Л—Е —Н—Д–Є—А–Њ–≤ —Д–µ–љ–Њ–ї–Њ–≤ (—А–µ–∞–Ї—Ж–Є—П –С–∞–є–µ—А–∞ вАФ –Т–Є–ї–ї–Є–≥–µ—А–∞ ) –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞–і–Ї–Є—Б–ї–Њ—В , –њ—А–Є—З—С–Љ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—В–Њ–≤ –Ј–∞–≤–Є—Б–Є—В –Ї–∞–Ї –Њ—В –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї–µ–є –≤ –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ —П–і—А–µ, —В–∞–Ї –Є –Њ—В –Ї–Є—Б–ї–Њ—В–љ–Њ—Б—В–Є —Б—А–µ–і—Л[ 44]
–Ю–Ї–Є—Б–ї–µ–љ–Є–µ –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –љ–∞–і–Ї–Є—Б–ї–Њ—В–∞–Љ–Є
–Р–ї—М–і–µ–≥–Є–і—Л –Љ–Њ–ґ–љ–Њ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—В—М –і–Њ –њ–µ—А–≤–Є—З–љ—Л—Е —Б–њ–Є—А—В–Њ–≤ . –Э–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—С–љ–љ—Л–µ –Љ–µ—В–Њ–і—Л –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –≤–Ї–ї—О—З–∞—О—В —А–µ–∞–Ї—Ж–Є–Є —Б –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ–Є –≥–Є–і—А–Є–і–∞–Љ–Є: –±–Њ—А–≥–Є–і—А–Є–і–Њ–Љ –љ–∞—В—А–Є—П NaBH4 , –±–Њ—А–≥–Є–і—А–Є–і–Њ–Љ –ї–Є—В–Є—П LiBH4 –Є –∞–ї—О–Љ–Њ–≥–Є–і—А–Є–і–Њ–Љ –ї–Є—В–Є—П LiAlH4 . –І—Г—В—М —А–µ–ґ–µ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –±–Њ—А–≥–Є–і—А–Є–і —Ж–Є–љ–Ї–∞ B2 H8 Zn.
–С–Њ—А–≥–Є–і—А–Є–і –љ–∞—В—А–Є—П —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ –Є–Ј–±–Є—А–∞—В–µ–ї—М–љ—Л–Љ —А–µ–∞–≥–µ–љ—В–Њ–Љ –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—В—М –Ї–∞—А–±–Њ–љ–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Є –Ї–µ—В–Њ–љ–Њ–≤, –љ–µ –Ј–∞—В—А–∞–≥–Є–≤–∞—П —Б–ї–Њ–ґ–љ–Њ—Н—Д–Є—А–љ—Л–µ , –љ–Є—В—А–Є–ї—М–љ—Л–µ , –∞–Љ–Є–і–љ—Л–µ , –ї–∞–Ї—В–Њ–љ–љ—Л–µ –Є –Њ–Ї—Б–Є—А–∞–љ–Њ–≤—Л–µ –≥—А—Г–њ–њ—Л. –Ю–љ —В–∞–Ї–ґ–µ –љ–µ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ—Г—О –і–≤–Њ–є–љ—Г—О —Г–≥–ї–µ—А–Њ–і-—Г–≥–ї–µ—А–Њ–і–љ—Г—О —Б–≤—П–Ј—М. –Р–ї—О–Љ–Њ–≥–Є–і—А–Є–і –ї–Є—В–Є—П –Љ–µ–љ–µ–µ —Б–µ–ї–µ–Ї—В–Є–≤–µ–љ –Є –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –≤—Л—И–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –≥—А—Г–њ–њ—Л, –њ–Њ—Н—В–Њ–Љ—Г –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –∞–ї—М–і–µ–≥–Є–і–Њ–≤ —Б –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —В–Њ–ї—М–Ї–Њ –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Н—В–Є—Е –≥—А—Г–њ–њ[ 45]
–Т–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –∞–ї—О–Љ–Њ–≥–Є–і—А–Є–і–Њ–Љ –ї–Є—В–Є—П –Ш—Б—В–Њ—А–Є—З–µ—Б–Ї—Г—О —А–Њ–ї—М –Є–≥—А–∞–µ—В —А–µ–∞–Ї—Ж–Є—П –Ь–µ–µ—А–≤–µ–є–љ–∞ вАФ –Я–Њ–љ–і–Њ—А—Д–∞ вАФ –Т–µ—А–ї–µ—П [–∞–љ–≥–ї.] –Є–Ј–Њ–њ—А–Њ–њ–Є–ї–∞—В –∞–ї—О–Љ–Є–љ–Є—П . –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Н—В–Њ—В –Љ–µ—В–Њ–і –≤—Л—В–µ—Б–љ–µ–љ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Є –Ї–µ—В–Њ–љ–Њ–≤ –Є–Ј–Њ–њ—А–Њ–њ–Є–ї–Њ–≤—Л–Љ —Б–њ–Є—А—В–Њ–Љ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Њ–Ї–Є—Б–Є –∞–ї—О–Љ–Є–љ–Є—П [ 45]
–Р–ї–Є—Д–∞—В–Є—З–µ—Б–Ї–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л –Њ–±—Л—З–љ–Њ –љ–µ –≥–Є–і—А–Є—А—Г—О—В –љ–∞ –њ–∞–ї–ї–∞–і–Є–µ–≤—Л—Е –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–∞—Е, –љ–Њ –і–ї—П —Н—В–Є—Е —Ж–µ–ї–µ–є –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —А—Г—В–µ–љ–Є–є –љ–∞ —Г–≥–ї–µ, –љ–Є–Ї–µ–ї—М –†–µ–љ–µ—П –Є–ї–Є –њ–ї–∞—В–Є–љ—Г [ 45]
–Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –љ–∞–ї–Є—З–Є–µ–Љ –љ–µ–њ–Њ–і–µ–ї—С–љ–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л—Е –њ–∞—А –∞—В–Њ–Љ–∞ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л –∞–ї—М–і–µ–≥–Є–і—Л —П–≤–ї—П—О—В—Б—П –ґ—С—Б—В–Ї–Є–Љ–Є –Њ—Б–љ–Њ–≤–∞–љ–Є—П–Љ–Є –Ы—М—О–Є—Б–∞ –Є, –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —Н—В–Є–Љ, –∞—В–Њ–Љ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –≤ –љ–Є—Е –Љ–Њ–ґ–µ—В –Ї–Њ–Њ—А–і–Є–љ–Є—А–Њ–≤–∞—В—М—Б—П —Б –ґ—С—Б—В–Ї–Є–Љ–Є –Ї–Є—Б–ї–Њ—В–∞–Љ–Є: H+ , ZnCl2 , BF3 , AlCl3 –Є —В. –і.[ 14] [ 46]
–Р–ї—М–і–µ–≥–Є–і—Л, –љ–µ –Є–Љ–µ—О—Й–Є–µ –∞—В–Њ–Љ–Њ–≤ –≤–Њ–і–Њ—А–Њ–і–∞ –њ—А–Є ќ±-—Г–≥–ї–µ—А–Њ–і–љ–Њ–Љ –∞—В–Њ–Љ–µ (—В–Њ –µ—Б—В—М –Є–Љ–µ—О—Й–Є–µ –Њ–±—Й—Г—О —Д–Њ—А–Љ—Г–ї—Г R3 CCHO) –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –≤–Њ–і–љ–Њ-—Б–њ–Є—А—В–Њ–≤–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ —Й—С–ї–Њ—З–Є –≤—Б—В—Г–њ–∞—О—В –≤ —А–µ–∞–Ї—Ж–Є—О –Ъ–∞–љ–љ–Є—Ж—Ж–∞—А–Њ , –≤ –Ї–Њ—В–Њ—А–Њ–є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –≤—Л—Б—В—Г–њ–∞—О—В –≤ —А–Њ–ї–Є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—П –Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—П . –°—Д–µ—А–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і–∞–љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ —А–∞—Б—И–Є—А—П–µ—В—Б—П –Ј–∞ —Б—З—С—В –њ–µ—А–µ–Ї—А—С—Б—В–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –Ъ–∞–љ–љ–Є—Ж—Ж–∞—А–Њ, –њ—А–Њ—В–µ–Ї–∞—О—Й–µ–є –Љ–µ–ґ–і—Г –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ –∞–ї—М–і–µ–≥–Є–і–Њ–Љ –Є —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–Њ–Љ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Й—С–ї–Њ—З–Є. –Я—А–Є —Н—В–Њ–Љ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї–µ–Љ —П–≤–ї—П–µ—В—Б—П —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і, –∞ –і—А—Г–≥–Њ–є –∞–ї—М–і–µ–≥–Є–і –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П –і–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ —Б–њ–Є—А—В–∞[ 47]
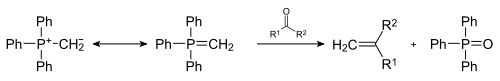
–Я–µ—А–µ–Ї—А—С—Б—В–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –Ъ–∞–љ–љ–Є—Ж—Ж–∞—А–Њ –Р–ї—М–і–µ–≥–Є–і—Л –Љ–Њ–≥—Г—В –≤—Б—В—Г–њ–∞—В—М –≤ —А–µ–∞–Ї—Ж–Є–Є —Б –Є–ї–Є–і–∞–Љ–Є —Д–Њ—Б—Д–Њ—А–∞ –њ–Њ —А–µ–∞–Ї—Ж–Є–Є –Т–Є—В—В–Є–≥–∞ , –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—П –∞–ї–Ї–µ–љ—Л —Б –Ј–∞–і–∞–љ–љ–Њ–є –Ї–Њ–љ—Д–Є–≥—Г—А–∞—Ж–Є–µ–є –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є (–Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Њ–±—А–∞–Ј—Г—О—В—Б—П Z -–∞–ї–Ї–µ–љ—Л, –љ–Њ —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –Є –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ –њ–Њ–ї—Г—З–∞—В—М E -–∞–ї–Ї–µ–љ—Л). –Т –і–∞–љ–љ–Њ–µ –≤—А–µ–Љ—П —Н—В–Њ –Њ–і–Є–љ –Є–Ј –ї—Г—З—И–Є—Е –Љ–µ—В–Њ–і–Њ–≤ —А–µ–≥–Є–Њ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ –∞–ї–Ї–µ–љ–Њ–≤[ 48]
–†–µ–∞–Ї—Ж–Є—П –Т–Є—В—В–Є–≥–∞ –Ґ–∞–Ї–ґ–µ –∞–ї—М–і–µ–≥–Є–і—Л –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤—Г—О—В —Б –Є–ї–Є–і–∞–Љ–Є —Б–µ—А—Л, –і–∞–≤–∞—П –Њ–Ї—Б–Є—А–∞–љ—Л (—А–µ–∞–Ї—Ж–Є—П –Ъ–Њ—А–Є вАФ –І–∞–є–Ї–Њ–≤—Б–Ї–Њ–≥–Њ [–∞–љ–≥–ї.] [ 49]
–Р–ї—М–і–µ–≥–Є–і—Л –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П —А–µ–∞–Ї—Ж–Є–Є –і–µ–Ї–∞—А–±–Њ–љ–Є–ї–Є—А–Њ–≤–∞–љ–Є—П –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–≤ –њ–µ—А–µ—Е–Њ–і–љ—Л—Е –Љ–µ—В–∞–ї–ї–Њ–≤, –љ–∞–њ—А–Є–Љ–µ—А, –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–∞ –£–Є–ї–Ї–Є–љ—Б–Њ–љ–∞ [ 50]
–Ґ–µ—Б—В –С—А–µ–і–Є вАФ 2,4-–і–Є–љ–Є—В—А–Њ—Д–µ–љ–Є–ї–≥–Є–і—А–∞–Ј–Є–љ —Б –∞–ї—М–і–µ–≥–Є–і–∞–Љ–Є –і–∞—С—В –ґ—С–ї—В—Л–є, –Њ—А–∞–љ–ґ–µ–≤—Л–є (–µ—Б–ї–Є –∞–ї—М–і–µ–≥–Є–і –∞–ї–Є—Д–∞—В–Є—З–µ—Б–Ї–Є–є) –Є–ї–Є –Ї—А–∞—Б–љ—Л–є (–µ—Б–ї–Є –∞–ї—М–і–µ–≥–Є–і –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є) –Њ—Б–∞–і–Њ–Ї:RCHO + C6 H3 (NO2 )2 NHNH2 вЖТ C6 H3 (NO2 )2 NHNCHR + H2 O RCHO + 2Cu(OH)2 вЖТ RCOOH + Cu2 O + 2H2 O –†–µ–∞–Ї—В–Є–≤ –®–Є—Д—Д–∞ (—Д—Г–Ї—Б–Є–љ—Б–µ—А–љ–Є—Б—В–∞—П –Ї–Є—Б–ї–Њ—В–∞) —А–µ–∞–≥–Є—А—Г–µ—В —Б –∞–ї—М–і–µ–≥–Є–і–∞–Љ–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —П—А–Ї–Њ–Њ–Ї—А–∞—И–µ–љ–љ–Њ–≥–Њ —Д–Є–Њ–ї–µ—В–Њ–≤–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞[ 53]
–Я—А–Є –і–µ–є—Б—В–≤–Є–Є —Е–ї–Њ—А–Є–і–∞ –≥–Є–і—А–Њ–Ї—Б–Є–ї–∞–Љ–Є–љ–Є—П –Њ–±—А–∞–Ј—Г–µ—В—Б—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–є –∞–ї—М–і–Њ–Ї—Б–Є–Љ –Є –≤—Л–і–µ–ї—П–µ—В—Б—П —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Е–ї–Њ—А–Є–і–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Т—Л–і–µ–ї–Є–≤—И—Г—О—Б—П –њ–Њ—Б–ї–µ —А–µ–∞–Ї—Ж–Є–Є –Ї–Є—Б–ї–Њ—В—Г —В–Є—В—А—Г—О—В —Й–µ–ї–Њ—З—М—О; –Є–љ–і–Є–Ї–∞—В–Њ—А вАФ —А–∞—Б—В–≤–Њ—А –±—А–Њ–Љ—Д–µ–љ–Њ–ї–Њ–≤–Њ–≥–Њ —Б–Є–љ–µ–≥–Њ (–Њ–Ї—А–∞—Б–Ї–∞ —А–∞—Б—В–≤–Њ—А–∞ –Є–Ј–Љ–µ–љ—П–µ—В—Б—П –Њ—В –ґ—С–ї—В–Њ-–Ј–µ–ї—С–љ–Њ–є –і–Њ —Д–Є–Њ–ї–µ—В–Њ–≤–Њ-—Б–Є–љ–µ–є)[ 54]
[
N
H
3
O
H
]
C
l
+
R
C
O
H
→ вЖТ -->
R
C
H
=
N
− вИТ -->
O
H
+
H
2
O
+
H
C
l
{\displaystyle {\mathsf {[NH_{3}OH]Cl+RCOH\rightarrow RCH{=}N{-}OH+H_{2}O+HCl}}}
–Т –∞–љ–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Є –Ї–µ—В–Њ–љ–Њ–≤ –є–Њ–і–Њ–Љ –≤ —Й–µ–ї–Њ—З–љ–Њ–є —Б—А–µ–і–µ. –Щ–Њ–і –і–Њ–±–∞–≤–ї—П—О—В –≤ –Є–Ј–±—Л—В–Ї–µ, –∞ –Ј–∞—В–µ–Љ –Є–Ј–±—Л—В–Њ–Ї –µ–≥–Њ –Њ—В—В–Є—В—А–Њ–≤—Л–≤–∞—О—В —В–Є–Њ—Б—Г–ї—М—Д–∞—В–Њ–Љ –љ–∞—В—А–Є—П[ 54]
R
C
H
O
+
I
2
+
3
N
a
O
H
→ вЖТ -->
R
C
O
O
N
a
+
2
N
a
I
+
2
H
2
O
{\displaystyle {\mathsf {RCHO+I_{2}+3NaOH\rightarrow RCOONa+2NaI+2H_{2}O}}}
I
2
+
2
N
a
2
S
2
O
3
→ вЖТ -->
2
N
a
I
+
N
a
2
S
4
O
6
{\displaystyle {\mathsf {I_{2}+2Na_{2}S_{2}O_{3}\rightarrow 2NaI+Na_{2}S_{4}O_{6}}}}
–Р–ї—М–і–µ–≥–Є–і—Л –ї–µ–≥–Ї–Њ –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –њ–Њ –Ш–Ъ-—Б–њ–µ–Ї—В—А—Г вАФ –Њ–љ —Б–Њ–і–µ—А–ґ–Є—В —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –њ–Њ–ї–Њ—Б—Л –њ–Њ–≥–ї–Њ—Й–µ–љ–Є—П, –Њ—В–љ–Њ—Б—П—Й–Є–µ—Б—П –Ї –≤–∞–ї–µ–љ—В–љ—Л–Љ –Ї–Њ–ї–µ–±–∞–љ–Є—П–Љ —Б–≤—П–Ј–Є C-H –≤ –∞–ї—М–і–µ–≥–Є–і–љ–Њ–є –≥—А—Г–њ–њ–µ: –і–≤–∞ –Њ—Б—В—А—Л—Е –њ–Є–Ї–∞, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–µ –і–∞–ї–µ–Ї–Њ –Ј–∞ –њ—А–µ–і–µ–ї–∞–Љ–Є –Њ–±–ї–∞—Б—В–Є –њ–Њ–≥–ї–Њ—Й–µ–љ–Є—П, —Е–∞—А–∞–Ї—В–µ—А–љ–Њ–є –і–ї—П —Б–≤—П–Ј–µ–є C-H –Њ–±—Л—З–љ–Њ–≥–Њ —В–Є–њ–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –Ш–Ъ-—Б–њ–µ–Ї—В—А–∞—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Њ–±—Л—З–љ–Њ –њ—А–Є—Б—Г—В—Б—В–≤—Г—О—В –њ–Њ–ї–Њ—Б—Л –њ–Њ–≥–ї–Њ—Й–µ–љ–Є—П, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–µ –≤–∞–ї–µ–љ—В–љ—Л–Љ–Є –Ї–Њ–ї–µ–±–∞–љ–Є—П–Љ–Є —Б–≤—П–Ј–µ–є –°=O –Є C-H: ќљ–°=O =1725-1685 —Б–ЉвИТ1 , ќљ–°-H =2850; 2750 —Б–ЉвИТ1 [ 14]
–Ь–∞—Б—Б-—Б–њ–µ–Ї—В—А—Л –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Є–Љ–µ—О—В –і–Њ–≤–Њ–ї—М–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–є –Є–Њ–љ, —Е–Њ—В—П –µ–≥–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Њ–≤–Њ–ї—М–љ–Њ –љ–Є–Ј–Ї–Є–Љ. –Я–Њ—В–µ—А—П –∞–ї–Ї–Є–ї—М–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –∞—Ж–Є–ї-–Ї–∞—В–Є–Њ–љ–Њ–≤. –Ф–ї—П –љ–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ —Е–∞—А–∞–Ї—В–µ—А–љ—Л ќ±- –Є ќ≤-—А–∞—Б—Й–µ–њ–ї–µ–љ–Є–µ –Є –њ–µ—А–µ–≥—А—Г–њ–њ–Є—А–Њ–≤–Ї–∞ –Ь–∞–Ї-–Ы–∞—Д—Д–µ—А—В–Є[ 55] [ 1] [ 56]
–Т 1 –Э –ѓ–Ь–†-—Б–њ–µ–Ї—В—А–µ –∞–ї—М–і–µ–≥–Є–і–∞ –љ–∞–Є–±–Њ–ї–µ–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є—З–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П —Б–Є–≥–љ–∞–ї —Д–Њ—А–Љ–Є–ї—М–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–љ–∞, –Њ–±—Л—З–љ–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–є –≤ –љ–∞–Є–±–Њ–ї–µ–µ —Б–ї–∞–±–Њ–Љ –њ–Њ–ї–µ –≤ –Њ–±–ї–∞—Б—В–Є ќі 9,4вАФ10,1 –Љ –і. (9,4-9,7 -–∞–ї–Є—Д–∞—В–Є—З–µ—Б–Ї–Є–µ, 9,6-10,1 -–∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ)[ 1] 13 C –ѓ–Ь–†-—Б–њ–µ–Ї—В—А–µ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ –≤ –Њ–±–ї–∞—Б—В–Є 182вАФ215 –Љ –і.[ 57]
–Ф–≤–∞ –Љ–∞–Ї—Б–Є–Љ—Г–Љ–∞ –њ–Њ–≥–ї–Њ—Й–µ–љ–Є—П –Њ—В —А –і–Њ —А* (<200 –љ–Љ) –Є –Њ—В n –і–Њ —А* (> 200 –љ–Љ)[ 57]
–≠–ї–µ–Ї—В—А–Њ–љ–љ—Л–µ —Б–њ–µ–Ї—В—А—Л —Б–Њ–і–µ—А–ґ–∞—В –њ–Њ–ї–Њ—Б—Л —Б ќї–Љ–∞–Ї—Б 290 –љ–Љ –і–ї—П RCHO (R=CH3 , C2 H5 , C3 H7 ), 345 –љ–Љ –і–ї—П –∞–Ї—А–Њ–ї–µ–Є–љ–∞ –Є 327 –і–ї—П –Ї—А–Њ—В–Њ–љ–Њ–≤–Њ–≥–Њ –∞–ї—М–і–µ–≥–Є–і–∞[ 1]
–Ґ–Њ–Ї—Б–Є—З–љ—Л. –°–њ–Њ—Б–Њ–±–љ—Л –љ–∞–Ї–∞–њ–ї–Є–≤–∞—В—М—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ. –Ъ—А–Њ–Љ–µ –Њ–±—Й–µ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ, –Њ–±–ї–∞–і–∞—О—В —А–∞–Ј–і—А–∞–ґ–∞—О—Й–Є–Љ –Є –љ–µ–є—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –≠—Д—Д–µ–Ї—В –Ј–∞–≤–Є—Б–Є—В –Њ—В –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –Љ–∞—Б—Б—Л: —З–µ–Љ –Њ–љ–∞ –±–Њ–ї—М—И–µ, —В–µ–Љ —Б–ї–∞–±–µ–µ —А–∞–Ј–і—А–∞–ґ–∞—О—Й–µ–µ, –љ–Њ —Б–Є–ї—М–љ–µ–µ –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –њ—А–Є—З—С–Љ –љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л–µ –∞–ї—М–і–µ–≥–Є–і—Л —В–Њ–Ї—Б–Є—З–љ–µ–µ –љ–∞—Б—Л—Й–µ–љ–љ—Л—Е. –Э–µ–Ї–Њ—В–Њ—А—Л–µ –Њ–±–ї–∞–і–∞—О—В –Ї–∞–љ—Ж–µ—А–Њ–≥–µ–љ–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є[ 58]
–Р–ї—М–і–µ–≥–Є–і—Л —А–∞–Ј–і—А–∞–ґ–∞—О—В —Б–ї–Є–Ј–Є—Б—В—Л–µ –Њ–±–Њ–ї–Њ—З–Ї–Є –≥–ї–∞–Ј –Є –≤–µ—А—Е–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, –≤—А–µ–і–љ–Њ –≤–ї–Є—П—О—В –љ–∞ –љ–µ—А–≤–љ—Г—О —Б–Є—Б—В–µ–Љ—Г. –° —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —З–Є—Б–ї–∞ –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞ –≤ –Љ–Њ–ї–µ–Ї—Г–ї–µ —А–∞–Ј–і—А–∞–ґ–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –Њ—Б–ї–∞–±–µ–≤–∞–µ—В. –Э–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л–µ –∞–ї—М–і–µ–≥–Є–і—Л –Њ–±–ї–∞–і–∞—О—В –±–Њ–ї–µ–µ —Б–Є–ї—М–љ—Л–Љ —А–∞–Ј–і—А–∞–ґ–∞—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, —З–µ–Љ –љ–∞—Б—Л—Й–µ–љ–љ—Л–µ.
–Р—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і –°–Э3 –°–Э–Ю –≤—Л–Ј—Л–≤–∞–µ—В –≤–Њ–Ј–±—Г–ґ–і–µ–љ–Є–µ, —Б–Љ–µ–љ—П—О—Й–µ–µ—Б—П –љ–∞—А–Ї–Њ–Ј–Њ–Љ. –Ю–љ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ—Л–Љ –њ—А–Њ–і—Г–Ї—В–Њ–Љ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ —Н—В–Є–ї–Њ–≤–Њ–≥–Њ —Б–њ–Є—А—В–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ. –Ф–µ–є—Б—В–≤–Є–µ —В—А–Є–Љ–µ—А–∞ —Н—В–Њ–≥–Њ –∞–ї—М–і–µ–≥–Є–і–∞ вАФ –њ–∞—А–∞–ї—М–і–µ–≥–Є–і–∞ (–°2 –Э4 O)3 вАФ —Б–Є–ї—М–љ–µ–µ –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–µ–µ, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —В–µ—В—А–∞–Љ–µ—А вАФ –Љ–µ—В–∞–ї—М–і–µ–≥–Є–і (–°2 –Э4 O)4 вАФ —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ —В–Њ–Ї—Б–Є—З–љ—Л–Љ. –£–і–ї–Є–љ–µ–љ–Є–µ –∞–ї–Ї–Є–ї—М–љ–Њ–≥–Њ —А–∞–і–Є–Ї–∞–ї–∞ –≤ –Љ–Њ–ї–µ–Ї—Г–ї–µ –∞–ї—М–і–µ–≥–Є–і–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г—Б–Є–ї–µ–љ–Є—О —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –љ–Њ –≤–Љ–µ—Б—В–µ —Б —Н—В–Є–Љ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –Є —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М[ 59]
–Т–≤–µ–і–µ–љ–Є–µ –≥–∞–ї–Њ–≥–µ–љ–∞ –≤ –Љ–Њ–ї–µ–Ї—Г–ї—Г –∞–ї—М–і–µ–≥–Є–і–∞ –њ–Њ–≤—Л—И–∞–µ—В –µ–≥–Њ –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Њ–µ (—Б–љ–Њ—В–≤–Њ—А–љ–Њ–µ) –і–µ–є—Б—В–≤–Є–µ. –Ґ–∞–Ї, –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ —Е–ї–Њ—А–∞–ї—П –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ—Л, —З–µ–Љ —Г –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і–∞. –Р–ї—М–і–µ–≥–Є–і–љ–∞—П –≥—А—Г–њ–њ–∞ —Г—Б–Є–ї–Є–≤–∞–µ—В —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М –≤–µ—Й–µ—Б—В–≤–∞, –љ–Њ –Њ–љ–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–µ–љ–∞ –њ—Г—В—С–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –≥–Є–і—А–∞—В–љ–Њ–є —Д–Њ—А–Љ—Л –∞–ї—М–і–µ–≥–Є–і–∞. –У–Є–і—А–∞—В–љ—Л–µ —Д–Њ—А–Љ—Л –Љ–∞–ї–Њ —В–Њ–Ї—Б–Є—З–љ—Л, –≤ —В–∞–Ї–Њ–є —Д–Њ—А–Љ–µ —Е–ї–Њ—А–∞–ї—М –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ –Љ–µ–і–Є—Ж–Є–љ–µ –њ–Њ–і –љ–∞–Ј–≤–∞–љ–Є–µ–Љ —Е–ї–Њ—А–∞–ї–≥–Є–і—А–∞—В–∞ , –њ—А–Њ—П–≤–ї—П—О—Й–µ–≥–Њ —Б–љ–Њ—В–≤–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Т–≤–µ–і–µ–љ–Є–µ –≥–Є–і—А–Њ–Ї—Б–Є–ї—М–љ—Л—Е –≥—А—Г–њ–њ –≤ –Љ–Њ–ї–µ–Ї—Г–ї—Г –∞–ї—М–і–µ–≥–Є–і–∞ –Є–ї–Є –Ї–Њ–љ–і–µ–љ—Б–∞—Ж–Є—П –Є—Е —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–ї—М–і–Њ–ї–µ–є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–ґ–∞–µ—В —А–µ–∞–Ї—Ж–Є–Њ–љ–љ—Г—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М, –∞ —В–∞–Ї–ґ–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Њ–µ–і–Є–љ–µ–љ–Є–є. –Ґ–∞–Ї, —Б–∞—Е–∞—А–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –Є–љ–µ—А—В–љ—Л–µ –≤–µ—Й–µ—Б—В–≤–∞. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –Є–Љ–µ–µ—В –љ–Є–Ј–Ї—Г—О —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М, —В–∞–Ї –Ї–∞–Ї –Њ–љ–Є –ї–µ–≥–Ї–Њ –Њ–Ї–Є—Б–ї—П—О—В—Б—П –і–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –Ї–Є—Б–ї–Њ—В, –Ї–Њ—В–Њ—А—Л–µ –Њ–±—Л—З–љ–Њ –і–Њ–≤–Њ–ї—М–љ–Њ –Є–љ–µ—А—В–љ—Л[ 59]
–Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –≤ –Љ–Њ–ї–µ–Ї—Г–ї–µ –∞–ї—М–і–µ–≥–Є–і–љ—Г—О –≥—А—Г–њ–њ—Г, –Є –Є—Е –Њ—Б–љ–Њ–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –Њ—А–≥–∞–љ–Є–Ј–Љ
–Т–∞–ґ–љ–µ–є—И–Є–µ –∞–ї—М–і–µ–≥–Є–і—Л –Є —А–Њ–і—Б—В–≤–µ–љ–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П. –Р–ї—М–і–µ–≥–Є–і–љ–∞—П (—Д–Њ—А–Љ–Є–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞) –Њ–±–Њ–Ј–љ–∞—З–µ–љ–∞ –Ї—А–∞—Б–љ—Л–Љ. –°–ї–µ–≤–∞ –љ–∞–њ—А–∞–≤–Њ: (1) —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і, (2) –µ–≥–Њ —В—А–Є–Љ–µ—А, (3) –∞—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і –Є (4) –µ–≥–Њ –µ–љ–Њ–ї –≤–Є–љ–Є–ї–Њ–≤—Л–є —Б–њ–Є—А—В, (5) –≥–ї—О–Ї–Њ–Ј–∞, (6) –∞—А–Њ–Љ–∞—В–Є–Ј–∞—В–Њ—А –Ї–Њ—А–Є—З–љ—Л–є –∞–ї—М–і–µ–≥–Є–і, (7) –њ–Є–≥–Љ–µ–љ—В —А–µ—В–Є–љ–∞–ї—М –Є (8) –≤–Є—В–∞–Љ–Є–љ –њ–Є—А–Є–і–Њ–Ї—Б–∞–ї—М –Ш–Ј –≤—Б–µ—Е –∞–ї—М–і–µ–≥–Є–і–Њ–≤ –±–Њ–ї—М—И–µ –≤—Б–µ–≥–Њ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—Б—П —Д–Њ—А–Љ–∞–ї—М–і–µ–≥–Є–і–∞ (–Њ–Ї–Њ–ї–Њ 6 –Љ–ї–љ —В–Њ–љ–љ/–≥–Њ–і). –Ю–љ, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ, –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–µ —Б–Љ–Њ–ї вАФ –±–∞–Ї–µ–ї–Є—В–∞, –≥–∞–ї–∞–ї–Є—В–∞ (–≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Љ–Њ—З–µ–≤–Є–љ–Њ–є , –Љ–µ–ї–∞–Љ–Є–љ–Њ–Љ –Є —Д–µ–љ–Њ–ї–Њ–Љ ), –і–ї—П –і—Г–±–ї–µ–љ–Є—П –Ї–Њ–ґ, –њ—А–Њ—В—А–∞–≤–ї–Є–≤–∞–љ–Є—П –Ј–µ—А–љ–∞. –Ґ–∞–Ї–ґ–µ –Є–Ј –љ–µ–≥–Њ —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ (—Г—А–Њ—В—А–Њ–њ–Є–љ ) –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –Ї–∞–Ї –Ї–Њ–љ—Б–µ—А–≤–∞–љ—В –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–±–ї–∞–≥–Њ–і–∞—А—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Б–≤–µ—А—В—Л–≤–∞—В—М –±–µ–ї–Њ–Ї). –Ю–љ —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–Њ–Љ –Љ–µ—В–Є–ї–µ–љ–і–Є—Д–µ–љ–Є–ї–і–Є–Є–Ј–Њ—Ж–Є–∞–љ–∞—В–∞ , –Є—Б–њ–Њ–ї—М–Ј—Г—О—Й–µ–≥–Њ—Б—П –≤ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–µ –њ–Њ–ї–Є—Г—А–µ—В–∞–љ–Њ–≤ –Є –≥–µ–Ї—Б–Њ–≥–µ–љ–∞ (–і–Њ–≤–Њ–ї—М–љ–Њ —Б–Є–ї—М–љ–Њ–є –≤–Ј—А—Л–≤—З–∞—В–Ї–Є).
–Т—В–Њ—А–Њ–є –њ–Њ –Љ–∞—Б—И—В–∞–±–∞–Љ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ –∞–ї—М–і–µ–≥–Є–і вАФ –Љ–∞—Б–ї—П–љ—Л–є –∞–ї—М–і–µ–≥–Є–і (–њ–Њ–ї—Г—З–∞—О—В –Њ–Ї–Њ–ї–Њ 2,5 –Љ–ї–љ —В–Њ–љ–љ/–≥–Њ–і –Љ–µ—В–Њ–і–Њ–Љ –≥–Є–і—А–Њ—Д–Њ—А–Љ–Є–ї–Є—А–Њ–≤–∞–љ–Є—П ). –Э–µ–Ї–Њ—В–Њ—А—Л–µ –∞–ї—М–і–µ–≥–Є–і—Л —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В —В–Њ–ї—М–Ї–Њ –≤ –љ–µ–±–Њ–ї—М—И–Є—Е –Љ–∞—Б—И—В–∞–±–∞—Е (–Љ–µ–љ–µ–µ 1000 —В–Њ–љ–љ / –≥–Њ–і) –Є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є–љ–≥—А–µ–і–Є–µ–љ—В–Њ–≤ –≤ –њ–∞—А—Д—О–Љ–µ—А–Є–Є –Є –∞—А–Њ–Љ–∞—В–Њ–≤ (–≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –∞–ї—М–і–µ–≥–Є–і—Л —Б —З–Є—Б–ї–Њ–Љ –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞ –Њ—В 8 –і–Њ 12)[ 1] –Ї–Њ—А–Є—З–љ—Л–є –∞–ї—М–і–µ–≥–Є–і –Є –µ–≥–Њ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ вАФ —Ж–Є—В—А–∞–ї—М –Є –ї–Є–ї–Є–∞–ї—М [ 60] –Љ–∞—Б–ї—П–љ—Л–є –∞–ї—М–і–µ–≥–Є–і (–њ–Њ–ї—Г—З–∞—О—В –Њ–Ї–Њ–ї–Њ 2,5 –Љ–ї–љ —В–Њ–љ–љ/–≥–Њ–і –Љ–µ—В–Њ–і–Њ–Љ –≥–Є–і—А–Њ—Д–Њ—А–Љ–Є–ї–Є—А–Њ–≤–∞–љ–Є—П ). –Э–µ–Ї–Њ—В–Њ—А—Л–µ –∞–ї—М–і–µ–≥–Є–і—Л —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В —В–Њ–ї—М–Ї–Њ –≤ –љ–µ–±–Њ–ї—М—И–Є—Е –Љ–∞—Б—И—В–∞–±–∞—Е (–Љ–µ–љ–µ–µ 1000 —В–Њ–љ–љ / –≥–Њ–і) –Є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є–љ–≥—А–µ–і–Є–µ–љ—В–Њ–≤ –≤ –њ–∞—А—Д—О–Љ–µ—А–Є–Є –Є –∞—А–Њ–Љ–∞—В–Њ–≤ (–≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –∞–ї—М–і–µ–≥–Є–і—Л —Б —З–Є—Б–ї–Њ–Љ –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞ –Њ—В 8 –і–Њ 12)[ 1] –Ї–Њ—А–Є—З–љ—Л–є –∞–ї—М–і–µ–≥–Є–і –Є –µ–≥–Њ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ вАФ —Ж–Є—В—А–∞–ї—М –Є –ї–Є–ї–Є–∞–ї—М [ 61]
–Р—Ж–µ—В–∞–ї—М–і–µ–≥–Є–і –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –і–ї—П —Б–Є–љ—В–µ–Ј–∞ —Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л , —Н—В–Є–ї–Њ–≤–Њ–≥–Њ —Б–њ–Є—А—В–∞, –±—Г—В–∞–і–Є–µ–љ–∞ –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –њ–Є—А–Є–і–Є–љ–∞ , –њ–µ–љ—В–∞—Н—А–Є—В—А–Є—В–∞ –Є –Ї—А–Њ—В–Њ–љ–Њ–≤–Њ–≥–Њ –∞–ї—М–і–µ–≥–Є–і–∞ , –∞ —В–∞–Ї–ґ–µ –њ—А–Є —Б–Є–љ—В–µ–Ј–µ –њ–Њ–ї–Є–≤–Є–љ–Є–ї–∞—Ж–µ—В–∞—В–∞ –Є –њ–ї–∞—Б—В–Љ–∞—Б—Б.
–Р–ї—М–і–µ–≥–Є–і—Л –њ—А–Є–Љ–µ–љ—П—О—В –і–ї—П —Б–Є–љ—В–µ–Ј–∞ —Б–њ–Є—А—В–Њ–≤ (–±—Г—В–Є–ї–Њ–≤—Л—Е, 2-—Н—В–Є–ї–≥–µ–Ї—Б–∞–љ–Њ–ї–∞, –њ–µ–љ—В–∞—Н—А–Є—В—А–Є—В–∞), –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В, –њ–Њ–ї–Є–Љ–µ—А–Њ–≤, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–Њ–≤, –њ–Є—А–Є–і–Є–љ–Њ–≤—Л—Е –Њ—Б–љ–Њ–≤–∞–љ–Є–є[ 1]
вЖС 1 2 3 4 5 6 7 8 9 10 –Ъ–љ—Г–љ—П–љ—Ж –Ш. –Ы. –Є –і—А. —В.1 –Р-–Ф–∞—А–Ј–∞–љ–∞ // –•–Є–Љ–Є—З–µ—Б–Ї–∞—П —Н–љ—Ж–Є–Ї–ї–Њ–њ–µ–і–Є—П. вАФ –Ь. : –°–Њ–≤–µ—В—Б–Ї–∞—П —Н–љ—Ж–Є–Ї–ї–Њ–њ–µ–і–Є—П, 1988. вАФ –°. 196-198. вАФ 623 —Б. вАФ 100 000 —Н–Ї–Ј. вЖС IUPAC Gold Book вАФ aldehydes (–љ–µ–Њ–њ—А.) . –Ф–∞—В–∞ –Њ–±—А–∞—Й–µ–љ–Є—П: 7 –Є—О–ї—П 2013. –Р—А—Е–Є–≤–Є—А–Њ–≤–∞–љ–Њ 9 –Є—О–ї—П 2013 –≥–Њ–і–∞.вЖС Liebig J. Sur les Produits de l'Oxidation de l'Alcool (—Д—А.) // Annales de chimie et de physique. вАФ 1835. вАФ Vol. 59 . вАФ P. 290 .вЖС Senning A. Elsevier's Dictionary of Chemoetymology. вАФ Elsevier, 2007. вАФ P. 151. вАФ ISBN 978-0-444-52239-9 .вЖС 1 2 –Ы–µ–µ–љ—Б–Њ–љ –Ш. –Р. –Ю—В–Ї—Г–і–∞ —В–≤–Њ—С –Є–Љ—П? –°—В–∞—В—М—П —И–µ—Б—В–∞—П. –Ю—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П (–љ–µ–Њ–њ—А.) . –Ф–∞—В–∞ –Њ–±—А–∞—Й–µ–љ–Є—П: 25 –Є—О–љ—П 2013. –Р—А—Е–Є–≤–Є—А–Њ–≤–∞–љ–Њ 29 –Є—О–љ—П 2013 –≥–Њ–і–∞.вЖС IUPAC Nomenclature of Organic Chemistry (–∞–љ–≥–ї.) . ACD/Labs. –Ф–∞—В–∞ –Њ–±—А–∞—Й–µ–љ–Є—П: 24 –∞–≤–≥—Г—Б—В–∞ 2009. –Р—А—Е–Є–≤–Є—А–Њ–≤–∞–љ–Њ 21 –∞–≤–≥—Г—Б—В–∞ 2011 –≥–Њ–і–∞.вЖС 1 2 –Ъ–∞–љ –†., –Ф–µ—А–Љ–µ—А –Ю. –Т–≤–µ–і–µ–љ–Є–µ –≤ —Е–Є–Љ–Є—З–µ—Б–Ї—Г—О –љ–Њ–Љ–µ–љ–Ї–ї–∞—В—Г—А—Г = Introduction to Chemical Nomenclature / –Я–µ—А. —Б –∞–љ–≥–ї. –Э. –Э. –©–µ—А–±–Є–љ–Њ–≤—Б–Ї–Њ–є, –њ–Њ–і —А–µ–і. –Т. –Ь. –Я–Њ—В–∞–њ–Њ–≤–∞, –†. –Р. –Ы–Є–і–Є–љ–∞. вАФ –Ь. : –•–Є–Љ–Є—П, 1983. вАФ –°. 139вАФ140.вЖС –°–њ—А–∞–≤–Њ—З–љ–Є–Ї —Е–Є–Љ–Є–Ї–∞ / –†–µ–і–Ї–Њ–ї–ї–µ–≥–Є—П: –Э–Є–Ї–Њ–ї—М—Б–Ї–Є–є –С. –Я. –Є –і—А.. вАФ 2-–µ –Є–Ј–і–∞–љ–Є–µ. вАФ –Ы–µ–љ–Є–љ–≥—А–∞–і, –Ь–Њ—Б–Ї–≤–∞: –•–Є–Љ–Є—П, 1964. вАФ –Ґ. 2. вАФ –°. 270, 285, 295. вЖС 1 2 3 4 5 6 7 –Я–µ—В—А–Њ–≤ –Р. –Р., –С–∞–ї—М—П–љ –•. –Т., –Ґ—А–Њ—Й–µ–љ–Ї–Њ –Р. –Ґ. –Ю—А–≥–∞–љ–Є—З–µ—Б–Ї–∞—П —Е–Є–Љ–Є—П. вАФ –Ш–≤–∞–љ –§–µ–і–Њ—А–Њ–≤, 1981. вАФ –Ґ. 1. вАФ –°. 165-184. вАФ 672 —Б. вАФ ISBN 5-81940-067-4 .вЖС –Э–µ—Б–Љ–µ—П–љ–Њ–≤ –Р. –Э., –Э–µ—Б–Љ–µ—П–љ–Њ–≤ –Э. –Р. –Э–∞—З–∞–ї–∞ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є —Е–Є–Љ–Є–Є. вАФ –Ь. : –•–Є–Љ–Є—П, 1974.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 2, —Б. 265вАФ273.вЖС –Ф–µ—Б—Б-–Ь–∞—А—В–Є–љ–∞ –†–µ–∞–≥–µ–љ—В (Dess Martin Periodinane) (–љ–µ–Њ–њ—А.) . www.khimia.ru. –Ф–∞—В–∞ –Њ–±—А–∞—Й–µ–љ–Є—П: 21 –Є—О–ї—П 2016. –Р—А—Е–Є–≤–Є—А–Њ–≤–∞–љ–Њ 22 –∞–≤–≥—Г—Б—В–∞ 2016 –≥–Њ–і–∞.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 12вАФ13.вЖС 1 2 3 4 5 6 7 –®–∞–±–∞—А–Њ–≤ –Ѓ.–°. –Ю—А–≥–∞–љ–Є—З–µ—Б–Ї–∞—П —Е–Є–Љ–Є—П. вАФ –Ы–∞–љ—М, 2011. вАФ –°. 218-221. вАФ 848 —Б.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 1, —Б. 480вАФ483.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 13вАФ14.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 203вАФ205.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 235.вЖС –Ь–∞—А—З –Ф–ґ. –Ю—А–≥–∞–љ–Є—З–µ—Б–Ї–∞—П —Е–Є–Љ–Є—П. вАФ –Ь. : –Ь–Є—А, 1987. вАФ –Ґ. –Ґ. 2. вАФ –°. 359вАФ363.вЖС 1 2 3 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 16вАФ20.вЖС 1 2 3 4 5 6 Kohlpaintner –Є –і—А., 2013 , p. 6вАФ8.вЖС Reuss G., Disteldorf W., Gamer A. O., Hilt A. Formaldehyde // Ullmann's Encyclopedia of Industrial Chemistry. вАФ Wiley, 2000. вАФ doi :10.1002/14356007.a11_619 .вЖС Eckert M., Fleischmann G., Jira R., Bolt H. M., Golka K. Acetaldehyde // Ullmann's Encyclopedia of Industrial Chemistry. вАФ Wiley, 2006. вАФ doi :10.1002/14356007.a01_031.pub2 .вЖС Br√Љhne F., Wright E. Benzaldehyde // Ullmann's Encyclopedia of Industrial Chemistry. вАФ Wiley, 2011. вАФ doi :10.1002/14356007.a03_463.pub2 .вЖС 1 2 3 4 Kohlpaintner –Є –і—А., 2013 , p. 2вАФ3.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 10вАФ11.вЖС Kohlpaintner –Є –і—А., 2013 , p. 3, 13.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 23.вЖС 1 2 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 23вАФ26.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 27вАФ28.вЖС 1 2 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 29вАФ37.вЖС 1 2 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 38вАФ39.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 40вАФ42.вЖС 1 2 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 44вАФ49.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 59вАФ60.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 60вАФ62.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 62вАФ64.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 64вАФ65.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 86.вЖС March, J. ¬ЂOrganic Chemistry: Reactions, Mechanisms, and Structures¬ї J. Wiley, New York: 1992. ISBN 0-471-58148-8 .
вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 95вАФ99.вЖС 1 2 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 124вАФ134.вЖС 1 2 3 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 75вАФ76.вЖС 1 2 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 79вАФ81.вЖС 1 2 3 –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 69вАФ75.вЖС –†–µ—Г—В–Њ–≤, 2004 .вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 82вАФ83.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 49вАФ57.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 57вАФ59.вЖС –†–µ—Г—В–Њ–≤, 2004 , —В. 3, —Б. 84вАФ85.вЖС –¶–≤–µ—В–Ї–Њ–≤ –Ы.–Р. ¬І 26. –Р–ї—М–і–µ–≥–Є–і—Л // –Ю—А–≥–∞–љ–Є—З–µ—Б–Ї–∞—П —Е–Є–Љ–Є—П. –£—З–µ–±–љ–Є–Ї –і–ї—П 10 –Ї–ї–∞—Б—Б–∞. вАФ 20-–µ –Є–Ј–і. вАФ –Ь. : –Я—А–Њ—Б–≤–µ—Й–µ–љ–Є–µ , 1981. вАФ –°. 120вАФ129.вЖС –Ъ–∞—З–µ—Б—В–≤–µ–љ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –љ–∞ –∞–ї—М–і–µ–≥–Є–і—Л —Б –≥–Є–і—А–Њ–Ї—Б–Є–і–Њ–Љ –Љ–µ–і–Є (II) –Р—А—Е–Є–≤–љ–∞—П –Ї–Њ–њ–Є—П –Њ—В 24 –і–µ–Ї–∞–±—А—П 2014 –љ–∞ Wayback Machine вАФ –≤–Є–і–µ–Њ–Њ–њ—Л—В –≤ –Х–і–Є–љ–Њ–є –Ї–Њ–ї–ї–µ–Ї—Ж–Є–Є —Ж–Є—Д—А–Њ–≤—Л—Е –Њ–±—А–∞–Ј–Њ–≤–∞—В–µ–ї—М–љ—Л—Е —А–µ—Б—Г—А—Б–Њ–≤вЖС –Ъ–∞—З–µ—Б—В–≤–µ–љ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –љ–∞ –∞–ї—М–і–µ–≥–Є–і—Л —Б —Д—Г–Ї—Б–Є–љ—Б–µ—А–љ–Є—Б—В–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є –Р—А—Е–Є–≤–Є—А–Њ–≤–∞–љ–Њ 24 –і–µ–Ї–∞–±—А—П 2014 –≥–Њ–і–∞.вЖС 1 2 –Я–∞—Б—Б–µ—В –С. –Т., –Р–љ—В–Є–њ–Њ–≤ –Ь. –Р. –Я—А–∞–Ї—В–Є–Ї—Г–Љ –њ–Њ —В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–Љ—Г –∞–љ–∞–ї–Є–Ј—Г –Є –Ї–Њ–љ—В—А–Њ–ї—О –≤ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–µ —Е–Є–Љ–Є–Ї–Њ-—Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. вАФ –Ь–µ–і–Є—Ж–Є–љ–∞, 1981. вАФ 272 —Б.вЖС Dr. Neil Glagovich. Fragmentation - Aldehydes (–љ–µ–Њ–њ—А.) . –Р—А—Е–Є–≤–Є—А–Њ–≤–∞–љ–Њ 6 –Є—О–ї—П 2013 –≥–Њ–і–∞.вЖС –Э.–°.–Т—Г–ї—М—Д—Б–Њ–љ, –Т.–У.–Ч–∞–Є–Ї–Є–љ,–Р.–Ш.–Ь–Є–Ї–∞—П. –Ь–∞—Б—Б-—Б–њ–µ–Ї—В—А–Њ—Б–Ї–Њ–њ–Є—П –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є. вАФ –•–Є–Љ–Є—П, 1986. вАФ –°. 197вАФ198.вЖС 1 2 Dr. Ian Hunt. Spectroscopic Analysis of Aldehydes (–∞–љ–≥–ї.) . Department of Chemistry University of Calgary . –Р—А—Е–Є–≤–Є—А–Њ–≤–∞–љ–Њ 6 –Є—О–ї—П 2013 –≥–Њ–і–∞.вЖС –Ю–±—Й–∞—П —В–Њ–Ї—Б–Є–Ї–Њ–ї–Њ–≥–Є—П / –њ–Њ–і —А–µ–і. –Р. –Ю. –Ы–Њ–є—В–∞. –°–Я–±.: –≠–Ы–С–Ш-–°–Я–±., 2006
вЖС 1 2 –Р–ї—М–і–µ–≥–Є–і—Л (–љ–µ–Њ–њ—А.) . –Ф–∞—В–∞ –Њ–±—А–∞—Й–µ–љ–Є—П: 27 –Є—О–љ—П 2013. –Р—А—Е–Є–≤–Є—А–Њ–≤–∞–љ–Њ –Є–Ј –Њ—А–Є–≥–Є–љ–∞–ї–∞ 29 –Є—О–љ—П 2013 –≥–Њ–і–∞.вЖС G. Reuss, W. Disteldorf, A. O. Gamer, A. Hilt. "Formaldehyde" in Ullmann's Encyclopedia of Industrial Chemistry (–∞–љ–≥–ї.) . вАФ 2005. вАФ doi :10.1002/14356007.a11 619 .вЖС G. Reuss, W. Disteldorf, A. O. Gamer, A. Hilt. "Formaldehyde" in Ullmann's Encyclopedia of Industrial Chemistry (–∞–љ–≥–ї.) . вАФ 2005. вАФ doi :10.1002/14356007.a11 619 .
–Ъ–љ—Г–љ—П–љ—Ж –Ш. –Ы. –Є –і—А. —В.1 –Р-–Ф–∞—А–Ј–∞–љ–∞ // –•–Є–Љ–Є—З–µ—Б–Ї–∞—П —Н–љ—Ж–Є–Ї–ї–Њ–њ–µ–і–Є—П. вАФ –Ь. : –°–Њ–≤–µ—В—Б–Ї–∞—П —Н–љ—Ж–Є–Ї–ї–Њ–њ–µ–і–Є—П, 1988. вАФ 623 —Б. вАФ 100 000 —Н–Ї–Ј. –†–µ—Г—В–Њ–≤ –Ю. –Р. –Є –і—А. –Ю—А–≥–∞–љ–Є—З–µ—Б–Ї–∞—П —Е–Є–Љ–Є—П. –Т 4 —З–∞—Б—В—П—Е. вАФ –Ь. : –С–Є–љ–Њ–Љ. –Ы–∞–±–Њ—А–∞—В–Њ—А–Є—П –Ј–љ–∞–љ–Є–є, 2004.Kohlpaintner C., Schulte M., Falbe J., Lappe P., Weber J., Frey G. D. Aldehydes, Araliphatic // Ullmann's Encyclopedia of Industrial Chemistry. вАФ Wiley, 2013. вАФ doi :10.1002/14356007.m01_m03.pub2 .Kohlpaintner C., Schulte M., Falbe J., Lappe P., Weber J., Frey G. D. Aldehydes, Aliphatic // Ullmann's Encyclopedia of Industrial Chemistry. вАФ Wiley, 2013. вАФ doi :10.1002/14356007.a01_321.pub3 .–°—Б—Л–ї–Ї–Є –љ–∞ –≤–љ–µ—И–љ–Є–µ —А–µ—Б—Г—А—Б—Л
–°–ї–Њ–≤–∞—А–Є –Є —Н–љ—Ж–Є–Ї–ї–Њ–њ–µ–і–Є–Є
–Т –±–Є–±–ї–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –Ї–∞—В–∞–ї–Њ–≥–∞—Е
–Я—А–µ–і–µ–ї—М–љ—Л–µ –Э–µ–њ—А–µ–і–µ–ї—М–љ—Л–µ –Р—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –У–µ—В–µ—А–Њ—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ


























![{\displaystyle {\mathsf {R{-}CH_{2}OH{\xrightarrow[{DMP}]{}}R{-}CHO}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f0b15841cd676b1573a947db0d7935b136295db0)

![{\displaystyle {\mathsf {CH_{2}(OH){-}CH_{2}(OH){\xrightarrow[{HIO_{4}}]{}}2CH_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f9d6919d90b037d655c0f4715fe8c3855c8c1732)

















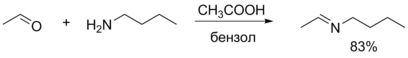
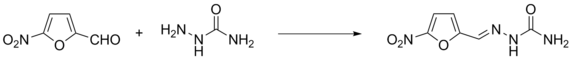








![{\displaystyle {\mathsf {[NH_{3}OH]Cl+RCOH\rightarrow RCH{=}N{-}OH+H_{2}O+HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/32eccdf5904f7cf37dee598b419a22c5ccb733be)





