–£—Ä–į—Ü–ł–Ľ

|
 –Ę–ĺ–Ņ—á–Ķ-–ł-—Ā—ā–į–Ņ—á–Ķ –ľ–ĺ–ī–Ķ–Ľ –Ĺ–į —É—Ä–į—Ü–ł–Ľ –Ę–ĺ–Ņ—á–Ķ-–ł-—Ā—ā–į–Ņ—á–Ķ –ľ–ĺ–ī–Ķ–Ľ –Ĺ–į —É—Ä–į—Ü–ł–Ľ
|
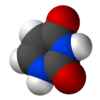 –ü—Ä–ĺ—Ā—ā–ĺ—Ä–Ķ–Ĺ –ľ–ĺ–ī–Ķ–Ľ –Ĺ–į —É—Ä–į—Ü–ł–Ľ –ü—Ä–ĺ—Ā—ā–ĺ—Ä–Ķ–Ĺ –ľ–ĺ–ī–Ķ–Ľ –Ĺ–į —É—Ä–į—Ü–ł–Ľ
|
|
–ü–ł—Ä–ł–ľ–ł–ī–ł–Ĺ-2,4(1H,3H)-–ī–ł–ĺ–Ĺ |
–Ē—Ä—É–≥–ł –Ĺ–į–∑–ł–≤–ł 2-–ĺ–ļ—Ā–ł-4-–ĺ–ļ—Ā–ł –Ņ–ł—Ä–ł–ľ–ł–ī–ł–Ĺ,
2,4(1H,3H)-–Ņ–ł—Ä–ł–ľ–ł–ī–ł–Ĺ–ī–ł–ĺ–Ĺ,
2,4-–ī–ł—Ö–ł–ī—Ä–ĺ—Ā–ļ–ł–Ņ–ł—Ä–ł–ľ–ł–ī–ł–Ĺ,
2,4-–Ņ–ł—Ä–ł–ľ–ł–ī–ł–Ĺ–ī–ł–ĺ–Ľ |
| –Ě–į–∑–Ĺ–į–ļ–ł
|
|
|
66-22-8 ![]() –ě–ļ –ě–ļ
|
| 3DMet
|
B00026
|
| –Ď–į—ė–Ľ—ą—ā–į—ė–Ĺ
|
606623
|
| ChEBI
|
CHEBI:17568  –Ě –Ě
|
| ChEMBL
|
ChEMBL566  –Ě –Ě
|
| ChemSpider
|
1141  –Ě –Ě
|
| DrugBank
|
DB03419
|
| EC-–Ī—Ä–ĺ—ė
|
200-621-9
|
|
|
2896
|
InChI=1S/C4H4N2O2/c7-3-1-2-5-4(8)6-3/h1-2H,(H2,5,6,7,8)  –Ě –Ě–ö–Ľ—É—á: ISAKRJDGNUQOIC-UHFFFAOYSA-N  –Ě –ĚInChI=1/C4H4N2O2/c7-3-1-2-5-4(8)6-3/h1-2H,(H2,5,6,7,8)
–ö–Ľ—É—á: ISAKRJDGNUQOIC-UHFFFAOYAV
|
IUPHAR/BPS
|
4560
|
| 3–Ē-–ľ–ĺ–ī–Ķ–Ľ (Jmol)
|
–°–Ľ–ł–ļ–į
|
| KEGG
|
C00106
|
| PubChem
|
1174
|
| RTECS-–Ī—Ä.
|
YQ8650000
|
|
|
| UNII
|
56HH86ZVCT  –Ě –Ě
|
| –°–≤–ĺ—ė—Ā—ā–≤–į
|
| –•–Ķ–ľ–ł—Ā–ļ–į —Ą–ĺ—Ä–ľ—É–Ľ–į
|
|
| –ú–ĺ–Ľ–į—Ä–Ĺ–į –ľ–į—Ā–į
|
0 g mol‚ąí1
|
| –ė–∑–≥–Ľ–Ķ–ī
|
–¶–≤—Ä—Ā—ā
|
| –ď—É—Ā—ā–ł–Ĺ–į
|
1.32 g/cm3
|
| –Ę–ĺ—á–ļ–į –Ĺ–į —ā–ĺ–Ņ–Ķ—ö–Ķ
|
|
| –Ę–ĺ—á–ļ–į –Ĺ–į –≤—Ä–ł–Ķ—ö–Ķ
|
|
|
|
–†–į—Ā—ā–≤–ĺ—Ä–Ľ–ł–≤
|
| –ě–Ņ–į—Ā–Ĺ–ĺ—Ā—ā
|
| –Ď–Ķ–∑–Ī–Ķ–ī–Ĺ–ĺ—Ā—ā –Ņ—Ä–ł —Ä–į–Ī–ĺ—ā–į:
|
–ď–Ľ–į–≤–Ĺ–ł –ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł
|
–ļ–į–Ĺ—Ü–Ķ—Ä–ĺ–≥–Ķ–Ĺ –ł —ā–Ķ—Ä–į—ā–ĺ–≥–Ķ–Ĺ —Ā–ĺ —Ö—Ä–ĺ–Ĺ–ł—á–Ĺ–ĺ –ł–∑–Ľ–ĺ–∂—É–≤–į—ö–Ķ
|
| GHS-–ĺ–∑–Ĺ–į–ļ–ł:
|
–ü–ł–ļ—ā–ĺ–≥—Ä–į–ľ–ł
|
 
|
–°–ł–≥–Ĺ–į–Ľ–Ĺ–ł –∑–Ī–ĺ—Ä–ĺ–≤–ł
|
–ě–Ņ–į—Ā–Ĺ–ĺ—Ā—ā
|
–ė–∑—ė–į–≤–ł –∑–į –ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā
|
H315, H319, H335, H361
|
–ė–∑—ė–į–≤–ł –∑–į –Ņ—Ä–Ķ—ā–Ņ–į–∑–Ľ–ł–≤–ĺ—Ā—ā
|
P201, P202, P261, P264, P271, P280, P281, P302+P352, P304+P340, P305+P351+P338, P308+P313, P312, P321, P332+P313, P337+P313, P362, P403+P233, P405, P501
|
| NFPA 704
|
|
| –Ę–Ķ–ľ–Ņ–Ķ—Ä–į—ā—É—Ä–į –Ĺ–į –∑–į–Ņ–į–Ľ—É–≤–į—ö–Ķ
|
–Ě–Ķ–∑–į–Ņ–į–Ľ–ł–≤
|
| –Ē–ĺ–Ņ–ĺ–Ľ–Ĺ–ł—ā–Ķ–Ľ–Ĺ–ł –Ņ–ĺ–ī–į—ā–ĺ—Ü–ł
|
|
|
 –ě–ļ(—ą—ā–ĺ –Ķ –ĺ–≤–į?) (–Ņ—Ä–ĺ–≤–Ķ—Ä–ł) –ě–ļ(—ą—ā–ĺ –Ķ –ĺ–≤–į?) (–Ņ—Ä–ĺ–≤–Ķ—Ä–ł)
–ě—Ā–≤–Ķ–Ĺ –į–ļ–ĺ –Ĺ–Ķ –Ķ –Ņ–ĺ–ł–Ĺ–į–ļ—É —É–ļ–į–∂–į–Ĺ–ĺ, –Ņ–ĺ–ī–į—ā–ĺ—Ü–ł—ā–Ķ —Ā–Ķ –ĺ–ī–Ĺ–Ķ—Ā—É–≤–į–į—ā –Ĺ–į –ľ–į—ā–Ķ—Ä–ł—ė–į–Ľ–ł—ā–Ķ –≤–ĺ –Ĺ–ł–≤–Ĺ–į—ā–į —Ā—ā–į–Ĺ–ī–į—Ä–ī–Ĺ–į —Ā–ĺ—Ā—ā–ĺ—ė–Ī–į (25 ¬įC, 100 kPa)
|
| –Ě–į–≤–ĺ–ī–ł
|
–£—Ä–į—Ü–ł–Ľ (U) –Ķ –Ķ–ī–Ĺ–į –ĺ–ī —á–Ķ—ā–ł—Ä–ł—ā–Ķ –į–∑–ĺ—ā–Ĺ–ł –Ī–į–∑–ł –ļ–ĺ–ł –≤–Ľ–Ķ–≥—É–≤–į–į—ā –≤–ĺ —Ā–ĺ—Ā—ā–į–≤–ĺ—ā –Ĺ–į –†–Ě–ö (–ĺ—Ā—ā–į–Ĺ–į—ā–ł—ā–Ķ —Ā–Ķ –į–ī–Ķ–Ĺ–ł–Ĺ, –≥–≤–į–Ĺ–ł–Ĺ –ł —Ü–ł—ā–ĺ–∑–ł–Ĺ). –í–ĺ –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ–į—ā–į –Ĺ–į –†–Ě–ö, —É—Ä–į—Ü–ł–Ľ —Ā–Ķ –≤—Ä–∑—É–≤–į —Ā–ĺ –į–ī–Ķ–Ĺ–ł–Ĺ –Ņ—Ä–Ķ–ļ—É –ī–≤–Ķ –≤–ĺ–ī–ĺ—Ä–ĺ–ī–Ĺ–ł –≤—Ä—Ā–ļ–ł. –í–ĺ –Ē–Ě–ö –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ–ł—ā–Ķ, —É—Ä–į—Ü–ł–Ľ–ĺ—ā —Ä–Ķ—ā–ļ–ĺ —Ā–Ķ —Ā—Ä–Ķ—ú–į–≤–į –ł –Ĺ–į—ė—á–Ķ—Ā—ā–ĺ –Ķ –∑–į–ľ–Ķ–Ĺ–Ķ—ā —Ā–ĺ –Ī–į–∑–į—ā–į —ā–ł–ľ–ł–Ĺ. –£—Ä–į—Ü–ł–Ľ–ĺ—ā –Ķ –≤—Ā—É—ą–Ĺ–ĺ—Ā—ā –ī–Ķ–ľ–Ķ—ā–ł–Ľ–ł—Ä–į–Ĺ–į —Ą–ĺ—Ä–ľ–į –Ĺ–į —ā–ł–ľ–ł–Ĺ–ĺ—ā.
–£—Ä–į—Ü–ł–Ľ–ĺ—ā –Ķ —á–Ķ—Ā—ā –Ņ—Ä–ł—Ä–ĺ–ī–Ķ–Ĺ –ī–Ķ—Ä–ł–≤–į—ā –Ĺ–į —Ö–Ķ—ā–Ķ—Ä–ĺ—Ü–ł–ļ–Ľ–ł—á–Ĺ–ĺ—ā–ĺ —Ā–ĺ–Ķ–ī–ł–Ĺ–Ķ–Ĺ–ł–Ķ –Ņ–ł—Ä–ł–ľ–ł–ī–ł–Ĺ. –ė–ľ–Ķ—ā–ĺ "—É—Ä–į—Ü–ł–Ľ" –≥–ĺ –ī–į–Ľ –≥–Ķ—Ä–ľ–į–Ĺ—Ā–ļ–ł–ĺ—ā —Ö–Ķ–ľ–ł—á–į—Ä –†–ĺ–Ī–Ķ—Ä—ā –Ď–Ķ—Ä–Ķ–Ĺ–ī, –≤–ĺ 1885 –≥–ĺ–ī–ł–Ĺ–į, –ļ–ĺ—ė —Ā–Ķ –ĺ–Ī–ł–ī—É–≤–į–Ľ –ī–į —Ā–ł–Ĺ—ā–Ķ—ā–ł–∑–ł—Ä–į –ī–Ķ—Ä–ł–≤–į—ā–ł –Ĺ–į –ľ–ĺ—á–Ĺ–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į.[1] –£—Ä–į—Ü–ł–Ľ–ĺ—ā –∑–į –Ņ—Ä–≤–Ņ–į—ā –Ī–ł–Ľ –ĺ—ā–ļ—Ä–ł–Ķ–Ĺ –≤–ĺ 1900 –≥–ĺ–ī–ł–Ĺ–į –ĺ–ī —Ā—ā—Ä–į–Ĺ–į –Ĺ–į –ź–Ľ–Ī–Ķ—Ä—ā–ĺ –ź—Ā–ļ–ĺ–Ľ–ł, –ļ–ĺ—ė –≥–ĺ –ł–∑–ĺ–Ľ–ł—Ä–į–Ľ —Ā–ĺ —Ö–ł–ī—Ä–ĺ–Ľ–ł–∑–į –Ĺ–į –Ĺ—É–ļ–Ľ–Ķ–ł–Ĺ—Ā–ļ–ł –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–ł –ĺ–ī –ļ–≤–į—Ā–Ķ—Ü.[2]
–í—Ä–∑ –ĺ—Ā–Ĺ–ĺ–≤–į –Ĺ–į –ĺ–ī–Ĺ–ĺ—Ā–ĺ—ā –ľ–Ķ—ď—É 12C/13C –ł–∑–ĺ—ā–ĺ–Ņ–ł—ā–Ķ –Ĺ–į –ĺ—Ä–≥–į–Ĺ—Ā–ļ–ł —Ā–ĺ–Ķ–ī–ł–Ĺ–Ķ–Ĺ–ł—ė–į –Ņ—Ä–ĺ–Ĺ–į—ė–ī–Ķ–Ĺ–ł –≤–ĺ –ú—É—Ä—á–ł—Ā–ĺ–Ĺ –ľ–Ķ—ā–Ķ–ĺ—Ä–ł—ā–ĺ—ā, –Ī–ł–Ľ–ĺ –∑–į–ļ–Ľ—É—á–Ķ–Ĺ–ĺ –ī–Ķ–ļ–į —Ā–ĺ–Ķ–ī–ł–Ĺ–Ķ–Ĺ–ł—ė–į –ļ–į–ļ–ĺ —É—Ä–į—Ü–ł–Ľ –ł –ļ—Ā–į–Ĺ—ā–ł–Ĺ –ľ–ĺ–∂–į—ā –ī–į —Ā–Ķ —Ą–ĺ—Ä–ľ–ł—Ä–į–į—ā –ł –≤–ĺ –≤–ĺ–Ĺ–∑–Ķ–ľ–Ĺ–ł —É—Ā–Ľ–ĺ–≤–ł.[3]
–í–ĺ 2012 –≥–ĺ–ī–ł–Ĺ–į, –į–Ĺ–į–Ľ–ł–∑–ł—ā–Ķ –Ĺ–į –Ņ–ĺ–ī–į—ā–ĺ—Ü–ł –ĺ–ī –ľ–ł—Ā–ł—ė–į—ā–į –ö–į—Ā–ł–Ĺ–ł –ļ–ĺ—ė–į –ĺ—Ä–Ī–ł—ā–ł—Ä–į –≤–ĺ —Ā–ł—Ā—ā–Ķ–ľ–ĺ—ā –Ĺ–į –Ņ–Ľ–į–Ĺ–Ķ—ā–į—ā–į –°–į—ā—É—Ä–Ĺ –Ņ–ĺ–ļ–į–∂–į–Ľ–Ķ –ī–Ķ–ļ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā –Ĺ–į—ė–≤–Ķ—Ä–ĺ—ė–į—ā–Ĺ–ĺ –≤–Ľ–Ķ–≥—É–≤–į –≤–ĺ –Ņ–ĺ–≤—Ä—ą–ł–Ĺ—Ā–ļ–ł–ĺ—ā —Ā–ĺ—Ā—ā–į–≤ –Ĺ–į –°–į—ā—É—Ä–Ĺ–ĺ–≤–ł–ĺ—ā —Ā–į—ā–Ķ–Ľ–ł—ā –Ę–ł—ā–į–Ĺ.[4]
–°–≤–ĺ—ė—Ā—ā–≤–į
–í–ĺ –†–Ě–ö, —É—Ä–į—Ü–ł–Ľ–ĺ—ā —Ā–Ķ –≤—Ä–∑—É–≤–į (—Ā–Ķ —Ā–Ņ–į—Ä—É–≤–į) –Ņ—Ä–Ķ–ļ—É –ī–≤–Ķ –≤–ĺ–ī–ĺ—Ä–ĺ–ī–Ĺ–ł –≤—Ä—Ā–ļ–ł –∑–į –į–ī–Ķ–Ĺ–ł–Ĺ–ĺ—ā –ł –≥–ĺ –∑–į–ľ–Ķ–Ĺ—É–≤–į —ā–ł–ľ–ł–Ĺ–ĺ—ā –∑–į –≤—Ä–Ķ–ľ–Ķ –Ĺ–į —ā—Ä–į–Ĺ—Ā–ļ—Ä–ł–Ņ—Ü–ł—ė–į—ā–į –Ĺ–į –Ē–Ě–ö. –ú–Ķ—ā–ł–Ľ–į—Ü–ł—ė–į—ā–į –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā –ī–į–≤–į —ā–ł–ľ–ł–Ĺ, —á–ł—ė –ī—Ä—É–≥ –Ĺ–į–∑–ł–≤ –Ķ 5-–ľ–Ķ—ā–ł–Ľ—É—Ä–į—Ü–ł–Ľ. –í–ĺ —ā–Ķ–ļ–ĺ—ā –Ĺ–į –Ķ–≤–ĺ–Ľ—É—Ü–ł—ė–į—ā–į –Ĺ–į –∂–ł–≤–ł–ĺ—ā —Ā–≤–Ķ—ā –Ĺ–į –ó–Ķ–ľ—ė–į—ā–į, –∑–į–ľ–Ķ–Ĺ–į—ā–į –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā —Ā–ĺ –Ņ–ĺ—Ā—ā–į–Ī–ł–Ľ–Ĺ–į—ā–į –Ī–į–∑–į —ā–ł–ľ–ł–Ĺ, –≤–ĺ —Ā–ĺ—Ā—ā–į–≤–ĺ—ā –Ĺ–į –Ē–Ě–ö, —ė–į –∑–≥–ĺ–Ľ–Ķ–ľ–ł–Ľ–į —Ā—ā–į–Ī–ł–Ľ–Ĺ–ĺ—Ā—ā–į –Ĺ–į –Ē–Ě–ö –ł –Ķ—Ą–ł–ļ–į—Ā–Ĺ–ĺ—Ā—ā–į –Ĺ–į –Ņ—Ä–ĺ—Ü–Ķ—Ā–ĺ—ā –Ĺ–į —Ä–Ķ–Ņ–Ľ–ł–ļ–į—Ü–ł—ė–į. –ü—Ä–ł –Ī–į–∑–Ĺ–ĺ—ā–ĺ —Ā–Ņ–į—Ä—É–≤–į—ö–Ķ —Ā–ĺ –į–ī–Ķ–Ĺ–ł–Ĺ, —É—Ä–į—Ü–ł–Ľ–ĺ—ā –ī–Ķ–Ľ—É–≤–į –ł –ļ–į–ļ–ĺ –į–ļ—Ü–Ķ–Ņ—ā–ĺ—Ä –ł –ļ–į–ļ–ĺ –ī–į—Ä–ł—ā–Ķ–Ľ –Ĺ–į –≤–ĺ–ī–ĺ—Ä–ĺ–ī–Ĺ–į –≤—Ä—Ā–ļ–į. –í–ĺ –†–Ě–ö, —É—Ä–į—Ü–ł–Ľ–ĺ—ā –ļ–ĺ–≤–į–Ľ–Ķ–Ĺ—ā–Ĺ–ĺ —Ā–Ķ –≤—Ä–∑—É–≤–į –∑–į —ą–Ķ—ú–Ķ—Ä–ĺ—ā —Ä–ł–Ī–ĺ–∑–į –∑–į –ī–į –≥–ĺ —Ą–ĺ—Ä–ľ–ł—Ä–į —Ä–ł–Ī–ĺ–Ĺ—É–ļ–Ľ–Ķ–ĺ–∑–ł–ī–ĺ—ā —É—Ä–ł–ī–ł–Ĺ. –°–ĺ –≤—Ä–∑—É–≤–į—ö–Ķ –Ĺ–į —Ą–ĺ—Ā—Ą–į—ā–Ĺ–į –≥—Ä—É–Ņ–į –∑–į —É—Ä–ł–ī–ł–Ĺ–ĺ—ā, —Ā–Ķ –ī–ĺ–Ī–ł–≤–į –Ĺ—É–ļ–Ľ–Ķ–ĺ—ā–ł–ī–ĺ—ā —É—Ä–ł–ī–ł–Ĺ 5'-–ľ–ĺ–Ĺ–ĺ—Ą–ĺ—Ā—Ą–į—ā.
–£—Ä–į—Ü–ł–Ľ –Ņ–ĺ–ī–Ľ–Ķ–≥–Ĺ—É–≤–į –Ĺ–į —ā–į–≤—ā–ĺ–ľ–Ķ—Ä–Ĺ–ł –Ņ—Ä–ĺ–ľ–Ķ–Ĺ–ł –Ĺ–į –į–ľ–ł–ī-–ł–ľ–ł–ī–Ĺ–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į, –Ī–ł–ī–Ķ—ė—ú–ł —Ā–Ķ–ļ–ĺ—ė–į —ė–į–ī—Ä–Ķ–Ĺ–į –Ĺ–Ķ—Ā—ā–į–Ī–ł–Ľ–Ĺ–ĺ—Ā—ā –ļ–ĺ—ė–į –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ–į—ā–į –ľ–ĺ–∂–Ķ –ī–į —ė–į –ł–ľ–į –Ņ–ĺ—Ä–į–ī–ł –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ–ļ–ĺ—ā –Ĺ–į —Ą–ĺ—Ä–ľ–į–Ľ–Ĺ–į –į—Ä–ĺ–ľ–į—ā–ł—á–Ĺ–ĺ—Ā—ā —Ā–Ķ –ļ–ĺ–ľ–Ņ–Ķ–Ĺ–∑–ł—Ä–į —Ā–ĺ —Ü–ł–ļ–Ľ–ł—á–Ĺ–ĺ-–į–ľ–ł–ī–Ĺ–į—ā–į —Ā—ā–į–Ī–ł–Ľ–Ĺ–ĺ—Ā—ā.[5] –ź–ľ–ł–ī–Ĺ–ł–ĺ—ā —ā–į–≤—ā–ĺ–ľ–Ķ—Ä —Ā–Ķ –Ĺ–į—Ä–Ķ–ļ—É–≤–į –Ľ–į–ļ—ā–į–ľ—Ā–ļ–į —Ā—ā—Ä—É–ļ—ā—É—Ä–į, –ī–ĺ–ī–Ķ–ļ–į —ā–į–≤—ā–ĺ–ľ–Ķ—Ä–ĺ—ā –Ĺ–į –ł–ľ–ł–ī–Ĺ–į—ā–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į —Ā–Ķ –Ĺ–į—Ä–Ķ–ļ—É–≤–į –Ľ–į–ļ—ā–ł–ľ—Ā–ļ–į —Ā—ā—Ä—É–ļ—ā—É—Ä–į. –ě–≤–ł–Ķ —ā–į–≤—ā–ĺ–ľ–Ķ—Ä–Ĺ–ł —Ą–ĺ—Ä–ľ–ł —Ā–Ķ –ī–ĺ–ľ–ł–Ĺ–į–Ĺ—ā–Ĺ–ł –Ņ—Ä–ł pH 7. –õ–į–ļ—ā–į–ľ—Ā–ļ–į—ā–į —Ā—ā—Ä—É–ļ—ā—É—Ä–į –Ķ –Ĺ–į—ė—á–Ķ—Ā—ā–į—ā–į —Ą–ĺ—Ä–ľ–į –Ĺ–į —É—Ä–į—Ü–ł–Ľ.
 –Ę–į–≤—ā–ĺ–ľ–Ķ—Ä–ł –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā: –į–ľ–ł–ī–Ĺ–į –ł–Ľ–ł –Ľ–į–ļ—ā–į–ľ—Ā–ļ–į —Ā—ā—Ä—É–ļ—ā—É—Ä–į (–Ľ–Ķ–≤–ĺ) –ł –ł–ľ–ł–ī–Ĺ–į –ł–Ľ–ł –Ľ–į–ļ—ā–ł–ľ—Ā–ļ–į —Ā—ā—Ä—É–ļ—ā—É—Ä–į (–ī–Ķ—Ā–Ĺ–ĺ).
–Ę–į–≤—ā–ĺ–ľ–Ķ—Ä–ł –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā: –į–ľ–ł–ī–Ĺ–į –ł–Ľ–ł –Ľ–į–ļ—ā–į–ľ—Ā–ļ–į —Ā—ā—Ä—É–ļ—ā—É—Ä–į (–Ľ–Ķ–≤–ĺ) –ł –ł–ľ–ł–ī–Ĺ–į –ł–Ľ–ł –Ľ–į–ļ—ā–ł–ľ—Ā–ļ–į —Ā—ā—Ä—É–ļ—ā—É—Ä–į (–ī–Ķ—Ā–Ĺ–ĺ).
–£—Ä–į—Ü–ł–Ľ–ĺ—ā, –ł—Ā—ā–ĺ —ā–į–ļ–į, —Ā–į–ľ–ł–ĺ—ā —Ā–Ķ —Ä–Ķ—Ü–ł–ļ–Ľ–ł—Ä–į –∑–į –ī–į —Ą–ĺ—Ä–ľ–ł—Ä–į –Ĺ—É–ļ–Ľ–Ķ–ĺ—ā–ł–ī–ł –Ņ—Ä–Ķ–ļ—É –Ĺ–į —Ā–Ķ—Ä–ł—ė–į –Ĺ–į —Ą–ĺ—Ā—Ą–ĺ—Ä–ł–Ī–ĺ–∑–ł–Ľ—ā—Ä–į–Ĺ—Ā—Ą–Ķ—Ä–į–∑–Ĺ–ł —Ä–Ķ–į–ļ—Ü–ł–ł. –†–į–∑–≥—Ä–į–ī—É–≤–į—ö–Ķ—ā–ĺ –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā –ī–į–≤–į –ļ–į–ļ–ĺ –Ņ—Ä–ĺ–ł–∑–≤–ĺ–ī–ł –į—Ā–Ņ–į—Ä–į–≥–ł–Ĺ—Ā–ļ–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į, —ė–į–≥–Ľ–Ķ—Ä–ĺ–ī –ī–ł–ĺ–ļ—Ā–ł–ī –ł –į–ľ–ĺ–Ĺ–ł—ė–į–ļ.
- C4H4N2O2 ‚Üí H3NCH2CH2COO‚ąí + NH4+ + CO2
–ě–ļ—Ā–ł–ī–į—ā–ł–≤–Ĺ–į—ā–į –ī–Ķ–≥—Ä–į–ī–į—Ü–ł—ė–į –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā –ī–į–≤–į –ļ–į–ļ–ĺ –Ņ—Ä–ĺ–ł–∑–≤–ĺ–ī–ł —É—Ä–Ķ–į –ł –ľ–į–Ľ–Ķ–ł–Ĺ—Ā–ļ–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į –≤–ĺ –Ņ—Ä–ł—Ā—É—Ā—ā–≤–ĺ –Ĺ–į H2O2 –ł Fe2+ –ł–Ľ–ł –≤–ĺ –Ņ—Ä–ł—Ā—É—Ā—ā–≤–ĺ –Ĺ–į –ļ–ł—Ā–Ľ–ĺ—Ä–ĺ–ī –ł Fe2+.
–£—Ä–į—Ü–ł–Ľ–ĺ—ā –Ķ —Ā–Ľ–į–Ī–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į. –ü—Ä–≤–į—ā–į –Ľ–ĺ–ļ–į—Ü–ł—ė–į –Ĺ–į —ė–ĺ–Ĺ–ł–∑–į—Ü–ł—ė–į –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā –Ĺ–Ķ –Ķ –Ņ–ĺ–∑–Ĺ–į—ā–į.[6] –Ě–Ķ–≥–į—ā–ł–≤–Ĺ–ł–ĺ—ā –Ņ–ĺ–Ľ–Ĺ–Ķ–∂ —Ā–Ķ —ė–į–≤—É–≤–į –Ĺ–į –ļ–ł—Ā–Ľ–ĺ—Ä–ĺ–ī–Ĺ–ł–ĺ—ā –į–Ĺ—ė–ĺ–Ĺ –ł –ī–į–≤–į pKa –≤—Ä–Ķ–ī–Ĺ–ĺ—Ā—ā –Ņ–ĺ–ľ–į–Ľ–į –ł–Ľ–ł –Ķ–ī–Ĺ–į–ļ–≤–į –Ĺ–į 12. –Ď–į–∑–Ĺ–į—ā–į pKa = -3.4, –ī–ĺ–ī–Ķ–ļ–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ—Ā–ļ–į—ā–į pKa = 9.389. –í–ĺ –≥–į—Ā–ĺ–≤–ł—ā–į —Ą–į–∑–į, —É—Ä–į—Ü–ł–Ľ–ĺ—ā –ł–ľ–į —á–Ķ—ā–ł—Ä–ł –ľ–Ķ—Ā—ā–į –ļ–ĺ–ł —Ā–Ķ –Ņ–ĺ–≤–Ķ—ú–Ķ –ļ–ł—Ā–Ķ–Ľ–ł –ĺ–ī –≤–ĺ–ī–į—ā–į.
–°–ł–Ĺ—ā–Ķ–∑–į
–ü–ĺ—Ā—ā–ĺ—ė–į—ā –ľ–Ĺ–ĺ–≥—É –Ĺ–į—á–ł–Ĺ–ł –∑–į –Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–ł—Ā–ļ–į —Ā–ł–Ĺ—ā–Ķ–∑–į –Ĺ–į —É—Ä–į—Ü–ł–Ľ. –Ě–į—ė–Ķ–ī–Ĺ–ĺ—Ā—ā–į–≤–Ĺ–į—ā–į —Ä–Ķ–į–ļ—Ü–ł—ė–į –Ķ –ī–ĺ–ī–į–≤–į—ö–Ķ –≤–ĺ–ī–į –Ĺ–į —Ü–ł—ā–ĺ–∑–ł–Ĺ –∑–į –ī–į —Ā–Ķ –ī–ĺ–Ī–ł–Ķ —É—Ä–į—Ü–ł–Ľ –ł –į–ľ–ĺ–Ĺ–ł—ė–į–ļ:
- C4H5N3O + H2O ‚Üí C4H4N2O2 + NH3
–Ě–į—ė—á–Ķ—Ā—ā–ł–ĺ—ā –Ĺ–į—á–ł–Ĺ –∑–į —Ā–ł–Ĺ—ā–Ķ–∑–į –Ĺ–į —É—Ä–į—Ü–ł–Ľ –Ķ –ļ–ĺ–Ĺ–ī–Ķ–Ĺ–∑–į—Ü–ł—ė–į –Ĺ–į —ė–į–Ī–ĺ–Ľ–ļ–ĺ–≤–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į —Ā–ĺ —É—Ä–Ķ–į –≤–ĺ –ī–ł–ľ–Ķ—á–ļ–į —Ā—É–Ľ—Ą—É—Ä–Ĺ–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į:[5]
- C4H4–ě4 + NH2CONH2 ‚Üí C4H4N2O2 + 2 H2O + C–ě
–£—Ä–į—Ü–ł–Ľ–ĺ—ā, –ł—Ā—ā–ĺ —ā–į–ļ–į, –ľ–ĺ–∂–Ķ –ī–į —Ā–Ķ —Ā–ł–Ĺ—ā–Ķ—ā–ł–∑–ł—Ä–į —Ā–ĺ –ī–≤–ĺ—ė–Ĺ–ĺ —Ä–į—Ā–Ņ–į—ď–į—ö–Ķ –Ĺ–į —ā–ł–ĺ—É—Ä–į—Ü–ł–Ľ –≤–ĺ –≤–ĺ–ī–Ķ–Ĺ–į —Ö–Ľ–ĺ—Ä–ĺ—Ü–Ķ—ā–Ĺ–į –ļ–ł—Ā–Ķ–Ľ–ł–Ĺ–į.[5]
–§–ĺ—ā–ĺ–ī–Ķ—Ö–ł–ī—Ä–ĺ–≥–Ķ–Ĺ–į—Ü–ł—ė–į—ā–į –Ĺ–į 5,6-–ī–ł—É—Ä–į—Ü–ł–Ľ–ĺ—ā, –ļ–ĺ—ė —Ā–Ķ —Ā–ł–Ĺ—ā–Ķ—ā–ł–∑–ł—Ä–į —Ā–ĺ —Ä–Ķ–į–ļ—Ü–ł—ė–į –ľ–Ķ—ď—É –Ī–Ķ—ā–į-–į–Ľ–į–Ĺ–ł–Ĺ –ł —É—Ä–Ķ–į, –ī–į–≤–į –ļ–į–ļ–ĺ –Ņ—Ä–ĺ–ł–∑–≤–ĺ–ī —É—Ä–į—Ü–ł–Ľ.
–†–Ķ–į–ļ—Ü–ł–ł
–£—Ä–į—Ü–ł–Ľ–ĺ—ā –Ľ–Ķ—Ā–Ĺ–ĺ —Ā—ā–į–Ņ—É–≤–į –≤–ĺ —Ä–Ķ–į–ļ—Ü–ł–ł –Ĺ–į –ĺ–ļ—Ā–ł–ī–į—Ü–ł—ė–į, –Ĺ–ł—ā—Ä–į—Ü–ł—ė–į –ł –į–Ľ–ļ–ł–Ľ–į—Ü–ł—ė–į. –í–ĺ –Ņ—Ä–ł—Ā—É—Ā—ā–≤–ĺ –Ĺ–į —Ą–Ķ–Ĺ–ĺ–Ľ (PhOH) –ł –Ĺ–į—ā—Ä–ł—É–ľ —Ö–ł–Ņ–ĺ—Ö–Ľ–ĺ—Ä–ł—ā (NaOCl), —É—Ä–į—Ü–ł–Ľ–ĺ—ā –ľ–ĺ–∂–Ķ –ī–į —Ā–Ķ –≤–ł–∑—É–Ķ–Ľ–ł–∑–ł—Ä–į –≤–ĺ —É–Ľ—ā—Ä–į–≤–ł–ĺ–Ľ–Ķ—ā–ĺ–≤–į —Ā–≤–Ķ—ā–Ľ–ł–Ĺ–į.[5] –£—Ä–į—Ü–ł–Ľ–ĺ—ā, –ł—Ā—ā–ĺ —ā–į–ļ–į, –ł–ľ–į —Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā –ī–į —Ä–Ķ–į–≥–ł—Ä–į —Ā–ĺ –Ķ–Ľ–Ķ–ľ–Ķ–Ĺ—ā–į—Ä–Ĺ–ł —Ö–į–Ľ–ĺ–≥–Ķ–Ĺ–ł –Ņ–ĺ—Ä–į–ī–ł –Ņ—Ä–ł—Ā—É—Ā—ā–≤–ĺ—ā–ĺ –Ĺ–į –Ņ–ĺ–≤–Ķ—ú–Ķ –ĺ–ī –Ķ–ī–Ĺ–į —Ā–ł–Ľ–Ĺ–į –Ķ–Ľ–Ķ–ļ—ā—Ä–ĺ–Ĺ-–ī–į—Ä–ł—ā–Ķ–Ľ—Ā–ļ–į –≥—Ä—É–Ņ–į.[5]
–ö–ĺ–≥–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā —Ä–Ķ–į–≥–ł—Ä–į —Ā–ĺ –Ī–Ķ–∑–≤–ĺ–ī–Ķ–Ĺ —Ö–ł–ī—Ä–į–∑–ł–Ĺ, –ļ–ł–Ĺ–Ķ—ā–ł–ļ–į—ā–į –Ĺ–į —Ä–Ķ–į–ļ—Ü–ł—ė–į—ā–į –Ķ –ĺ–ī –Ņ—Ä–≤ —Ä–Ķ–ī –ł —ā–Ķ—á–Ķ –ī–ĺ –ĺ—ā–≤–ĺ—Ä–į—ö–Ķ –Ĺ–į –Ņ—Ä—Ā—ā–Ķ–Ĺ–ĺ—ā –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā. –ź–ļ–ĺ —Ä–Ě –Ĺ–į —Ä–Ķ–į–ļ—Ü–ł—ė–į—ā–į —Ā–Ķ –∑–≥–ĺ–Ľ–Ķ–ľ–ł –Ĺ–į > 10.5, —Ā–Ķ —Ą–ĺ—Ä–ľ–ł—Ä–į –į–Ĺ—ė–ĺ–Ĺ –Ĺ–į —É—Ä–į—Ü–ł–Ľ, —ą—ā–ĺ –Ņ—Ä–Ķ–ī–ł–∑–≤–ł–ļ—É–≤–į –ľ–Ĺ–ĺ–≥—É –Ņ–ĺ–Ī–į–≤–Ĺ–ĺ —ā–Ķ—á–Ķ—ö–Ķ –Ĺ–į —Ä–Ķ–į–ļ—Ü–ł—ė–į—ā–į. –ė—Ā—ā–ĺ—ā–ĺ –∑–į–Ī–į–≤—É–≤–į—ö–Ķ –Ĺ–į —Ä–Ķ–į–ļ—Ü–ł—ė–į—ā–į —Ā–Ķ —ė–į–≤—É–≤–į –ł –į–ļ–ĺ pH —Ā–Ķ –Ĺ–į–ľ–į–Ľ—É–≤–į, –Ņ–ĺ—Ä–į–ī–ł –Ņ—Ä–ĺ—ā–ĺ–Ĺ–į—ā–į—Ü–ł—ė–į –Ĺ–į —Ö–ł–ī—Ä–į–∑–ł–Ĺ–ĺ—ā. –†–Ķ–į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–į –Ĺ–į —É—Ä–į—Ü–ł–Ľ–ĺ—ā –ĺ—Ā—ā–į–Ĺ—É–≤–į –Ĺ–Ķ–Ņ—Ä–ĺ–ľ–Ķ–Ĺ–Ķ—ā–į —Ā–ĺ –Ņ—Ä–ĺ–ľ–Ķ–Ĺ–į –Ĺ–į —ā–Ķ–ľ–Ņ–Ķ—Ä–į—ā—É—Ä–į—ā–į.
–Ě–į–≤–ĺ–ī–ł
- ‚ÜĎ Behrend, Robert (1885). ‚ÄěVersuche zur Synthese von K√∂rpern der Harns√§urereihe‚Äú. Justus Liebig's Annalen der Chemie (–į–Ĺ–≥–Ľ–ł—Ā–ļ–ł). 229 (1‚Äď2): 1‚Äď44. doi:10.1002/jlac.18852290102. ISSN 0075-4617.
- ‚ÜĎ ‚ÄěHoppe-Seyler's Zeitschrift F√ľr Physiologische Chemie - Google Books‚Äú. 2018-05-12. –ź—Ä—Ö–ł–≤–ł—Ä–į–Ĺ–ĺ –ĺ–ī –ł–∑–≤–ĺ—Ä–Ĺ–ł–ļ–ĺ—ā –Ĺ–į 2018-05-12. –ü–ĺ—Ā–Ķ—ā–Ķ–Ĺ–ĺ –Ĺ–į 2018-07-06.CS1-–ĺ–ī—Ä–∂—É–≤–į—ö–Ķ: –Ī–ĺ—ā: –Ĺ–Ķ–Ņ–ĺ–∑–Ĺ–į—ā —Ā—ā–į—ā—É—Ā –Ĺ–į –ł–∑–≤–ĺ—Ä–Ĺ–į—ā–į URL (link)
- ‚ÜĎ ‚ÄěExtraterrestrial nucleobases in the Murchison meteorite‚Äú. Earth and Planetary Science Letters (–į–Ĺ–≥–Ľ–ł—Ā–ļ–ł). 270 (1‚Äď2): 130‚Äď136. 2008-06-15. doi:10.1016/j.epsl.2008 –ľ–į—Ä—ā 026 . ISSN 0012-821X.
- ‚ÜĎ Nelson, Clark, Roger; N., Pearson; H., Brown, R.; P., Cruikshank, D.; J., Barnes; R., Jaumann; L., Soderblom; C., Griffith; P., Rannou (–ĺ–ļ—ā–ĺ–ľ–≤—Ä–ł 2012). ‚ÄěThe Surface Composition of Titan‚Äú (–į–Ĺ–≥–Ľ–ł—Ā–ļ–ł). 44.
- ‚ÜĎ 5,0 5,1 5,2 5,3 5,4 Brown, D. J. (1994). Chemistry of Heterocyclic Compounds (–į–Ĺ–≥–Ľ–ł—Ā–ļ–ł). Wiley-Interscience. ISBN 9780471506560.
- ‚ÜĎ Zorbach, W. Werner; Tipson, R. Stuart (1968). Synthetic Procedures in Nucleic Acid Chemistry: Physical and physicochemical aids in characterization and in determination of structure (–į–Ĺ–≥–Ľ–ł—Ā–ļ–ł). Interscience Publishers.
–Ě–į–ī–≤–ĺ—Ä–Ķ—ą–Ĺ–ł –≤—Ä—Ā–ļ–ł