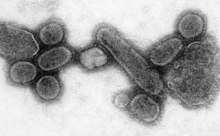
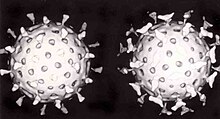
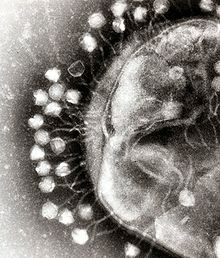
–Т—ЦћБ—А—Г—Б (–Т–Є–Љ–Њ–≤–∞ –ї–∞—В. virus вАФ –Њ—В—А—Г—В–∞) вАФ –љ–µ–Ї–ї—Ц—В–Є–љ–љ–Є–є —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є–є –∞–≥–µ–љ—В, —П–Ї–Є–є –Љ–Њ–ґ–µ –≤—Ц–і—В–≤–Њ—А—О–≤–∞—В–Є—Б—П –ї–Є—И–µ –≤—Б–µ—А–µ–і–Є–љ—Ц –ґ–Є–≤–Є—Е –Ї–ї—Ц—В–Є–љ . –Т—Ц—А—Г—Б–Є —Г—А–∞–ґ–∞—О—В—М –≤—Б—Ц —В–Є–њ–Є –Њ—А–≥–∞–љ—Ц–Ј–Љ—Ц–≤ , –≤—Ц–і —А–Њ—Б–ї–Є–љ —Ц —В–≤–∞—А–Є–љ –і–Њ –±–∞–Ї—В–µ—А—Ц–є —Ц –∞—А—Е–µ—Ч–≤ [ 1] –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥–∞–Љ–Є ). –Т–Є—П–≤–ї–µ–љ–Њ —В–∞–Ї–Њ–ґ –≤—Ц—А—Г—Б–Є, –Ј–і–∞—В–љ—Ц —А–µ–њ–ї—Ц–Ї—Г–≤–∞—В–Є—Б—П –ї–Є—И–µ –Ј–∞ –њ—А–Є—Б—Г—В–љ–Њ—Б—В—Ц —Ц–љ—И–Є—Е –≤—Ц—А—Г—Б—Ц–≤ (–≤—Ц—А—Г—Б–Є-—Б–∞—В–µ–ї—Ц—В–Є ).
–Т—Ц–і —З–∞—Б—Г –њ—Г–±–ї—Ц–Ї–∞—Ж—Ц—Ч 1892 —А–Њ–Ї—Г —Б—В–∞—В—В—Ц –Ф–Љ–Є—В—А–∞ –Ж–≤–∞–љ–Њ–≤—Б—М–Ї–Њ–≥–Њ , —П–Ї–Є–є –Њ–њ–Є—Б–∞–≤ –љ–µ–±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Є–є –њ–∞—В–Њ–≥–µ–љ —А–Њ—Б–ї–Є–љ —В—О—В—О–љ—Г , —Ц –≤—Ц–і–Ї—А–Є—В—В—П 1898 —А–Њ–Ї—Г –Ь–∞—А—В—Ц–љ–Њ–Љ –С–µ—Ф—А—Ц–љ–Ї–Њ–Љ –≤—Ц—А—Г—Б—Г —В—О—В—О–љ–Њ–≤–Њ—Ч –Љ–Њ–Ј–∞—Ч–Ї–Є –±—Г–ї–Њ –і–Њ–Ї–ї–∞–і–љ–Њ –Њ–њ–Є—Б–∞–љ–Њ –њ–Њ–љ–∞–і 6 —В–Є—Б—П—З –≤–Є–і—Ц–≤ –≤—Ц—А—Г—Б—Ц–≤. –Ю–і–љ–∞–Ї, –њ—А–Є–њ—Г—Б–Ї–∞—О—В—М, —Й–Њ —Ч—Е —Ц—Б–љ—Г—Ф –њ–Њ–љ–∞–і 100 –Љ—Ц–ї—М–є–Њ–љ—Ц–≤[ 4] –µ–Ї–Њ—Б–Є—Б—В–µ–Љ—Ц –љ–∞ –Ч–µ–Љ–ї—Ц . –Т–Њ–љ–Є —Ф –љ–∞–є—З–Є—Б–µ–ї—М–љ—Ц—И–Њ—О –±—Ц–Њ–ї–Њ–≥—Ц—З–љ–Њ—О —Д–Њ—А–Љ–Њ—О[ 5] [ 6] –≤—Ц—А—Г—Б–Њ–ї–Њ–≥—Ц—П , —А–Њ–Ј–і—Ц–ї –Љ—Ц–Ї—А–Њ–±—Ц–Њ–ї–Њ–≥—Ц—Ч .
–£ —В–≤–∞—А–Є–љ –≤—Ц—А—Г—Б–љ—Ц —Ц–љ—Д–µ–Ї—Ж—Ц—Ч —Б–њ—А–Є—З–Є–љ—О—О—В—М —Ц–Љ—Г–љ–љ—Г –≤—Ц–і–њ–Њ–≤—Ц–і—М , —П–Ї–∞ –љ–∞–є—З–∞—Б—В—Ц—И–µ –њ—А–Є–Ј–≤–Њ–і–Є—В—М –і–Њ –Ј–љ–Є—Й–µ–љ–љ—П –≤—Ц—А—Г—Б—Г. –Ж–Љ—Г–љ–љ—Г –≤—Ц–і–њ–Њ–≤—Ц–і—М —В–∞–Ї–Њ–ґ –Љ–Њ–ґ–љ–∞ —Б–њ—А–Є—З–Є–љ–Є—В–Є –≤–∞–Ї—Ж–Є–љ–∞–Љ–Є , —П–Ї—Ц –і–∞—О—В—М –∞–Ї—В–Є–≤–љ–Є–є –љ–∞–±—Г—В–Є–є —Ц–Љ—Г–љ—Ц—В–µ—В –њ—А–Њ—В–Є –њ–µ–≤–љ–Њ—Ч –≤—Ц—А—Г—Б–љ–Њ—Ч —Ц–љ—Д–µ–Ї—Ж—Ц—Ч. –Ю–і–љ–∞–Ї –і–µ—П–Ї–Є–Љ –≤—Ц—А—Г—Б–∞–Љ, –Ј–Њ–Ї—А–µ–Љ–∞ –≤—Ц—А—Г—Б—Г —Ц–Љ—Г–љ–Њ–і–µ—Д—Ц—Ж–Є—В—Г –ї—О–і–Є–љ–Є —Ц –Ј–±—Г–і–љ–Є–Ї–∞–Љ –≤—Ц—А—Г—Б–љ–Є—Е –≥–µ–њ–∞—В–Є—В—Ц–≤ , –≤–і–∞—Ф—В—М—Б—П –њ—А–Њ—Б–Ї–Њ—З–Є—В–Є –њ–Њ–≤–Ј —Ц–Љ—Г–љ–љ—Г –≤—Ц–і–њ–Њ–≤—Ц–і—М, —Б–њ—А–Є—З–Є–љ—О—О—З–Є —Е—А–Њ–љ—Ц—З–љ—Г —Е–≤–Њ—А–Њ–±—Г . –Р–љ—В–Є–±—Ц–Њ—В–Є–Ї–Є –љ–µ –і—Ц—О—В—М –љ–∞ –≤—Ц—А—Г—Б–Є, –њ—А–Њ—В–µ —А–Њ–Ј—А–Њ–±–ї–µ–љ–Њ –і–µ–Ї—Ц–ї—М–Ї–∞ –њ—А–Њ—В–Є–≤—Ц—А—Г—Б–љ–Є—Е –њ—А–µ–њ–∞—А–∞—В—Ц–≤ .
–°–ї–Њ–≤–Њ ¬Ђ–≤—Ц—А—Г—Б¬ї —Г—В–≤–Њ—А–µ–љ–µ –≤—Ц–і –ї–∞—В. virus вАФ ¬Ђ–Њ—В—А—Г—В–∞¬ї. –Р–±–Є –њ–Њ–Ј–љ–∞—З–Є—В–Є –∞–≥–µ–љ—В, –Ј–і–∞—В–љ–Є–є —Б–њ—А–Є—З–Є–љ–Є—В–Є —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ—Г —Е–≤–Њ—А–Њ–±—Г, –є–Њ–≥–Њ –≤–њ–µ—А—И–µ –Ј–∞—Б—В–Њ—Б–Њ–≤–∞–љ–Њ 1728 —А–Њ–Ї—Г[ 7] –Ф–Љ–Є—В—А–Њ–Љ –Ж–≤–∞–љ–Њ–≤—Б—М–Ї–Є–Љ ; –≤—Ц–љ –ґ–µ –≤–≤—Ц–≤ —В–µ—А–Љ—Ц–љ —Д—Ц–ї—М—В—А—Ц–≤–љ–Є–є –≤—Ц—А—Г—Б —П–Ї –њ–Њ–Ј–љ–∞—З–µ–љ–љ—П –љ–µ–±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Њ–≥–Њ —Е–≤–Њ—А–Њ–±–Њ—В–≤–Њ—А–љ–Њ–≥–Њ –∞–≥–µ–љ—В–∞, –Ј–і–∞—В–љ–Њ–≥–Њ –њ—А–Њ—Е–Њ–і–Є—В–Є –Ї—А—Ц–Ј—М –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ—Ц —Д—Ц–ї—М—В—А–Є вАФ —Д—Ц–ї—М—В—А—Г–≤–∞—В–Є—Б—П. –Ґ–µ—А–Љ—Ц–љ ¬Ђ–≤—Ц—А—Ц–Њ–љ¬ї , —Б—В–≤–Њ—А–µ–љ–љ—П —П–Ї–Њ–≥–Њ –њ—А–Є–њ–∞–і–∞—Ф –љ–∞ 1959 —А—Ц–Ї[ 8] [ 9]
–Ь–∞—А—В—Ц–љ –С–µ—Ф—А—Ц–љ–Ї —Г —Б–≤–Њ—Ч–є –ї–∞–±–Њ—А–∞—В–Њ—А—Ц—Ч 1921 —А–Њ–Ї—Г–Ы—Г—Ч –Я–∞—Б—В–µ—А –љ–µ –Ј–Љ—Ц–≥ –≤–Є—П–≤–Є—В–Є –Љ—Ц–Ї—А–Њ–Њ—А–≥–∞–љ—Ц–Ј–Љ, —П–Ї–Є–є —Б–њ—А–Є—З–Є–љ—О—Ф —Б–Ї–∞–Ј , —Ц –њ—А–Є–њ—Г—Б–Ї–∞–≤, —Й–Њ —Ж–µ–є –њ–∞—В–Њ–≥–µ–љ –Ј–∞–љ–∞–і—В–Њ –Љ–∞–ї–Є–є, —Й–Њ–± –њ–Њ–±–∞—З–Є—В–Є –є–Њ–≥–Њ –≤ –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ[ 10] –®–∞—А–ї—М –®–∞–Љ–±–µ—А–ї–∞–љ [en] —Д—Ц–ї—М—В—А –®–∞–Љ–±–µ—А–ї–∞–љ–∞ [en] —В–Њ–Ї—Б–Є–љ , —П–Ї–Є–є –≤–Є–і—Ц–ї—П—О—В—М –±–∞–Ї—В–µ—А—Ц—Ч, –Њ–і–љ–∞–Ї –≤—Ц–љ –љ–µ —А–Њ–Ј–≤–Є–љ—Г–≤ —Ж—О –і—Г–Љ–Ї—Г. –£ —В–Њ–є —З–∞—Б –≤–≤–∞–ґ–∞–ї–Є, —Й–Њ –±—Г–і—М-—П–Ї–Є–є —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є–є –∞–≥–µ–љ—В –Љ–Њ–ґ–љ–∞ –≤–Є–і—Ц–ї–Є—В–Є –љ–∞ —Д—Ц–ї—М—В—А—Ц –є –≤–Є—А–Њ—Й—Г–≤–∞—В–Є –≤ –ґ–Є–≤–Є–ї—М–љ–Њ–Љ—Г —Б–µ—А–µ–і–Њ–≤–Є—Й—Ц вАФ —Ж–µ –Њ–і–Є–љ –Ј –њ–Њ—Б—В—Г–ї–∞—В—Ц–≤ –Љ—Ц–Ї—А–Њ–±–љ–Њ—Ч —В–µ–Њ—А—Ц—Ч —Е–≤–Њ—А–Њ–±. –Ъ—А—Ц–Љ —В–Њ–≥–Њ, –Ж–≤–∞–љ–Њ–≤—Б—М–Ї–Є–є –≤ –Њ–њ—В–Є—З–љ–Њ–Љ—Г –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ—Ц —Б–њ–Њ—Б—В–µ—А—Ц–≥–∞–≤ —Г –Ј–∞—А–∞–ґ–µ–љ–Є—Е –Ї–ї—Ц—В–Є–љ–∞—Е —А–Њ—Б–ї–Є–љ –Ї—А–Є—Б—В–∞–ї–Њ–њ–Њ–і—Ц–±–љ—Ц —В—Ц–ї–∞, —П–Ї—Ц –≤ —Б—Г—З–∞—Б–љ–Њ–Љ—Г —А–Њ–Ј—Г–Љ—Ц–љ–љ—Ц –±—Г–ї–Є —Б–Ї—Г–њ—З–µ–љ–љ—П–Љ–Є –≤—Ц—А—Г—Б—Ц–≤, –Ј–≥–Њ–і–Њ–Љ —Ч—Е –љ–∞–Ј–≤–∞–љ–Њ ¬Ђ–Ї—А–Є—Б—В–∞–ї–∞–Љ–Є –Ж–≤–∞–љ–Њ–≤—Б—М–Ї–Њ–≥–Њ¬ї[ 13] –Ь–∞—А—В—Ц–љ –С–µ—Ф—А—Ц–љ–Ї –њ–Њ–≤—В–Њ—А–Є–≤ –і–Њ—Б–ї—Ц–і–ґ–µ–љ–љ—П –Ж–≤–∞–љ–Њ–≤—Б—М–Ї–Њ–≥–Њ –є –Ј—А–Њ–±–Є–≤ –≤–Є—Б–љ–Њ–≤–Њ–Ї, —Й–Њ —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є–є –Љ–∞—В–µ—А—Ц–∞–ї, —П–Ї–Є–є –њ—А–Њ–є—И–Њ–≤ –Ї—А—Ц–Ј—М —Д—Ц–ї—М—В—А, —Ф –љ–µ —Й–Њ —Ц–љ—И–µ, —П–Ї –љ–Њ–≤–∞ —Д–Њ—А–Љ–∞ —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є—Е –∞–≥–µ–љ—В—Ц–≤. –Т—Ц–љ –њ–Њ–Љ—Ц—В–Є–≤, —Й–Њ –∞–≥–µ–љ—В —А–Њ–Ј–Љ–љ–Њ–ґ—Г—Ф—В—М—Б—П —В—Ц–ї—М–Ї–Є –≤ –Ї–ї—Ц—В–Є–љ–∞—Е –Ї–Њ—В—А—Ц –і—Ц–ї—П—В—М—Б—П, –Њ–і–љ–∞–Ї –є–Њ–≥–Њ –і–Њ—Б–ї—Ц–і–Є –љ–µ –≤–Є—П–≤–Є–ї–Є —В–Њ–≥–Њ, —Й–Њ —Б–∞–Љ–µ —П–≤–ї—П—О—В—М —Б–Њ–±–Њ—О —З–∞—Б—В–Є–љ–Ї–Є. –С–µ—Ф—А—Ц–љ–Ї –љ–∞–Ј–≤–∞–≤ –є–Њ–≥–Њ —А–Њ–Ј—З–Є–љ–љ–Є–є –ґ–Є–≤–Є–є –Ї–Њ–љ—В–∞–≥—Ц–є (–ї–∞—В. Contagium vivum fluidum ) —Ц –Ј–љ–Њ–≤—Г –≤–≤—Ц–≤ —Г –≤–ґ–Є—В–Њ–Ї —Б–ї–Њ–≤–Њ ¬Ђ–≤—Ц—А—Г—Б¬ї. –Т—Ц–љ —В–≤–µ—А–і–Є–≤, —Й–Њ –Ј–∞ —Б–≤–Њ—Ф—О –њ—А–Є—А–Њ–і–Њ—О –≤—Ц—А—Г—Б —А—Ц–і–Ї–Є–є. –Ч–≥–Њ–і–Њ–Љ —Ж—О —В–µ–Њ—А—Ц—О —Б–њ—А–Њ—Б—В—Г–≤–∞–≤ –Т–µ–љ–і–µ–ї–ї –°—В–µ–љ–ї—Ц , —П–Ї–Є–є –і–Њ–≤—Ц–≤, —Й–Њ –≤—Ц—А—Г—Б–Є —Ф —З–∞—Б—В–Є–љ–Ї–∞–Љ–Є. –Ґ–Њ–≥–Њ –ґ —А–Њ–Ї—Г –§—А—Ц–і—А—Ц—Е –Ы–µ—Д–ї–µ—А —Ц –Я–∞—Г–ї—М –§—А–Њ—И –≤–Є—П–≤–Є–ї–Є –њ–µ—А—И–Є–є –≤—Ц—А—Г—Б —В–≤–∞—А–Є–љ вАФ –Ј–±—Г–і–љ–Є–Ї —П—Й—Г—А—Г (–∞—Д—В–Њ–≤—Ц—А—Г—Б [en] [ 15]
–Э–∞ –њ–Њ—З–∞—В–Ї—Г XX —Б—В–Њ–ї—Ц—В—В—П –∞–љ–≥–ї—Ц–є—Б—М–Ї–Є–є –±–∞–Ї—В–µ—А—Ц–Њ–ї–Њ–≥ –§—А–µ–і–µ—А—Ц–Ї –Ґ–≤–Њ—А—В –≤—Ц–і–Ї—А–Є–≤ –≥—А—Г–њ—Г –≤—Ц—А—Г—Б—Ц–≤, –Ї–Њ—В—А—Ц —Ц–љ—Д—Ц–Ї—Г—О—В—М –±–∞–Ї—В–µ—А—Ц—Ч (–љ–Є–љ—Ц –≤–Њ–љ–Є –≤—Ц–і–Њ–Љ—Ц —П–Ї –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥–Є –∞–±–Њ –њ—А–Њ—Б—В–Њ —Д–∞–≥–Є ), –∞ —Д—А–∞–љ–Ї–Њ-–Ї–∞–љ–∞–і—Б—М–Ї–Є–є –Љ—Ц–Ї—А–Њ–±—Ц–Њ–ї–Њ–≥ –§–µ–ї—Ц–Ї—Б –Ф'–Х—А–µ–ї–ї—М [en] –∞–≥–∞—А—Ц —Г—В–≤–Њ—А—О—О—В—М –љ–∞–≤–Ї–Њ–ї–Њ —Б–µ–±–µ –њ—А–Њ—Б—В—Ц—А –Ј –Љ–µ—А—В–≤–Є–Љ–Є –±–∞–Ї—В–µ—А—Ц—П–Љ–Є. –Ф'–Х—А–µ–ї–ї—М –Ј—А–Њ–±–Є–≤ —В–Њ—З–љ—Ц —А–Њ–Ј–≤–µ–і–µ–љ–љ—П —Б—Г—Б–њ–µ–љ–Ј—Ц—Ч —Ж–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Ц –≤—Б—В–∞–љ–Њ–≤–Є–≤ –љ–∞–є–±—Ц–ї—М—И–µ —А–Њ–Ј–≤–µ–і–µ–љ–љ—П (–љ–∞–є–Љ–µ–љ—И—Г –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж—Ц—О –≤—Ц—А—Г—Б—Ц–≤), –Ј–∞ —П–Ї–Њ–≥–Њ –љ–µ –≤—Б—Ц –±–∞–Ї—В–µ—А—Ц—Ч –≥–Є–љ—Г—В—М, –∞–ї–µ –≤–Њ–і–љ–Њ—З–∞—Б —Г—В–≤–Њ—А—О—О—В—М—Б—П –Њ–Ї—А–µ–Љ—Ц –і—Ц–ї—П–љ–Ї–Є –Ј –Љ–µ—А—В–≤–Є–Љ–Є –Ї–ї—Ц—В–Є–љ–∞–Љ–Є. –Я—Ц–і—А–∞—Е—Г–≤–∞–≤—И–Є –Ї—Ц–ї—М–Ї—Ц—Б—В—М —В–∞–Ї–Є—Е –і—Ц–ї—П–љ–Њ–Ї —В–∞ –≤—А–∞—Е–Њ–≤—Г—О—З–Є –Ї–Њ–µ—Д—Ц—Ж—Ц—Ф–љ—В —А–Њ–Ј–≤–µ–і–µ–љ–љ—П, –≤—Ц–љ –≤–Є–Ј–љ–∞—З–Є–≤ –Ї—Ц–ї—М–Ї—Ц—Б—В—М –≤—Ц—А—Г—Б–љ–Є—Е —З–∞—Б—В–Є–љ–Њ–Ї —Г –њ–Њ—З–∞—В–Ї–Њ–≤—Ц–є —Б—Г—Б–њ–µ–љ–Ј—Ц—Ч[ 17] —З–µ—А–µ–≤–љ–Є–є —В–Є—Д —Ц —Е–Њ–ї–µ—А–∞ , –њ—А–Њ—В–µ —Г–≤–∞–≥–∞ –і–Њ –љ–Є—Е –Ј–љ–Є–Ї–ї–∞ —З–µ—А–µ–Ј –≤—Ц–і–Ї—А–Є—В—В—П –±—Ц–ї—М—И –µ—Д–µ–Ї—В–Є–≤–љ–Є—Е –њ–µ–љ—Ц—Ж–Є–ї—Ц–љ—Г —В–∞ —Ц–љ—И–Є—Е –∞–љ—В–Є–±—Ц–Њ—В–Є–Ї—Ц–≤. –Т–Є–≤—З–µ–љ–љ—П —Д–∞–≥—Ц–≤ –і–∞–ї–Њ —А–Њ–Ј—Г–Љ—Ц–љ–љ—П –њ—А–Њ —П–≤–Є—Й–µ ¬Ђ–≤–Љ–Є–Ї–∞–љ–љ—П¬ї —Ц ¬Ђ–≤–Є–Љ–Є–Ї–∞–љ–љ—П¬ї –≥–µ–љ—Ц–≤, –∞ —В–∞–Ї–Њ–ґ –і–Њ–Ј–≤–Њ–ї–Є–ї–Њ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞—В–Є —Ч—Е –і–ї—П –≤–≤–µ–і–µ–љ–љ—П –≤ –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Є–є –≥–µ–љ–Њ–Љ —З—Г–ґ–Њ—А—Ц–і–љ–Є—Е –≥–µ–љ—Ц–≤.
–Э–∞–њ—А–Є–Ї—Ц–љ—Ж—Ц XIX —Б—В–Њ–ї—Ц—В—В—П –≤–ґ–µ –±—Г–ї–Њ –≤—Ц–і–Њ–Љ–Њ, —Й–Њ –≤—Ц—А—Г—Б–Є –Ј–і–∞—В–љ—Ц —Ц–љ—Д—Ц–Ї—Г–≤–∞—В–Є, –њ—А–Њ—Е–Њ–і—П—В—М –Ї—А—Ц–Ј—М —Д—Ц–ї—М—В—А–Є —Ц –њ–Њ—В—А–µ–±—Г—О—В—М –ґ–Є–≤–Њ–≥–Њ —Е–∞–Ј—П—Ч–љ–∞ –і–ї—П —А–Њ–Ј–Љ–љ–Њ–ґ–µ–љ–љ—П. –Ґ–Њ–і—Ц –≤—Ц—А—Г—Б–Є –Ј –і–Њ—Б–ї—Ц–і–љ–Є—Ж—М–Ї–Њ—О –Љ–µ—В–Њ—О –Ї—Г–ї—М—В–Є–≤—Г–≤–∞–ї–Є —В—Ц–ї—М–Ї–Є –≤ —А–Њ—Б–ї–Є–љ–∞—Е —Ц —В–≤–∞—А–Є–љ–∞—Е. 1906 —А–Њ–Ї—Г –†–Њ—Б—Б “Р—А–µ–љ–≤—Ц–ї–ї –У–∞—А—А—Ц—Б–Њ–љ –≤–Є–љ–∞–є—И–Њ–≤ —Б–њ–Њ—Б—Ц–± –≤–Є—А–Њ—Й—Г–≤–∞–љ–љ—П —В–Ї–∞–љ–Є–љ –≤ –ї—Ц–Љ—Д—Ц , —Ц 1913 —А–Њ–Ї—Г –®—В–µ–є–љ–∞—А–і, –Ж–Ј—А–∞–µ–ї—Ц —В–∞ –Ы–∞–Љ–±–µ—А—В –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞–ї–Є —Ж–µ–є –Љ–µ—В–Њ–і, –Ї–Њ–ї–Є –≤–Є—А–Њ—Й—Г–≤–∞–ї–Є –≤—Ц—А—Г—Б –Њ—Б–њ–Њ–≤–∞–Ї—Ж–Є–љ–Є –љ–∞ —Д—А–∞–≥–Љ–µ–љ—В–∞—Е —В–Ї–∞–љ–Є–љ–Є —А–Њ–≥—Ц–≤–Ї–Є –Љ–Њ—А—Б—М–Ї–Є—Е —Б–≤–Є–љ–Њ–Ї [ 18] –љ–Є—А–Њ–Ї . –¶–µ–є –Љ–µ—В–Њ–і –љ–µ –Ј–∞—Б—В–Њ—Б–Њ–≤—Г–≤–∞–ї–Є —И–Є—А–Њ–Ї–Њ –і–Њ –Ї—Ц–љ—Ж—П 1950-—Е —А–Њ–Ї—Ц–≤, –Ї–Њ–ї–Є —Г –≤–µ–ї–Є–Ї–Є—Е –Љ–∞—Б—И—В–∞–±–∞—Е —Б—В–∞–ї–Є –≤–Є—А–Њ—Й—Г–≤–∞—В–Є –њ–Њ–ї—Ц–Њ–≤—Ц—А—Г—Б –і–ї—П –≤–Є—А–Њ–±–љ–Є—Ж—В–≤–∞ –≤–∞–Ї—Ж–Є–љ–Є .
–Ж–љ—И–µ –≤–µ–ї–Є–Ї–µ –і–Њ—Б—П–≥–љ–µ–љ–љ—П –љ–∞–ї–µ–ґ–Є—В—М –∞–Љ–µ—А–Є–Ї–∞–љ—Б—М–Ї–Њ–Љ—Г –њ–∞—В–Њ–ї–Њ–≥—Г –Х—А–љ–µ—Б—В—Г –Т—Ц–ї—М—П–Љ—Г –У—Г–і–њ–∞—Б—З–µ—А—Г [en] –≥—А–Є–њ—Г —В–∞ –Ї—Ц–ї—М–Ї–∞ —Ц–љ—И–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Г –Ј–∞–њ–ї—Ц–і–љ–µ–љ–Є—Е –Ї—Г—А—П—З–Є—Е —П–є—Ж—П—Е[ 20] –Ф–ґ–Њ–љ –§—А–∞–љ–Ї–ї—Ц–љ –Х–љ–і–µ—А—Б , –Ґ–Њ–Љ–∞—Б –Т–µ–ї–ї–µ—А —Ц –§—А–µ–і–µ—А—Ц–Ї –†–Њ–±–±—Ц–љ—Б –≤–Є—А–Њ—Б—В–Є–ї–Є –њ–Њ–ї—Ц–Њ–≤—Ц—А—Г—Б –≤ –Ї—Г–ї—М—В—Г—А—Ц –Ї–ї—Ц—В–Є–љ –Ј–∞—А–Њ–і–Ї–∞ –ї—О–і–Є–љ–Є. –¶–µ –±—Г–≤ –њ–µ—А—И–Є–є –≤—Ц—А—Г—Б, –≤–Є—А–Њ—Й–µ–љ–Є–є –љ–µ –≤ —В–Ї–∞–љ–Є–љ–∞—Е —В–≤–∞—А–Є–љ –∞–±–Њ —П–є—Ж—П—Е. –¶—П —А–Њ–±–Њ—В–∞ –і–∞–ї–∞ –Љ–Њ–ґ–ї–Є–≤—Ц—Б—В—М –Ф–ґ–Њ–љ–∞—Б—Г –°–Њ–ї–Ї—Г —Б—В–≤–Њ—А–Є—В–Є –і—Ц—Ф–≤—Г –њ–Њ–ї—Ц–Њ–≤–∞–Ї—Ж–Є–љ—Г (–≤–∞–Ї—Ж–Є–љ—Г –њ—А–Њ—В–Є –њ–Њ–ї—Ц–Њ–Љ—Ц—Ф–ї—Ц—В—Г )[ 21]
–Я–µ—А—И—Ц –Ј–Њ–±—А–∞–ґ–µ–љ–љ—П –≤—Ц—А—Г—Б—Ц–≤ –Њ—В—А–Є–Љ–∞–ї–Є –њ—Ц—Б–ї—П —В–Њ–≥–Њ, —П–Ї 1931 —А–Њ–Ї—Г –љ—Ц–Љ–µ—Ж—М–Ї—Ц —Ц–љ–ґ–µ–љ–µ—А–Є –Х—А–љ—Б—В –†—Г—Б–Ї–∞ —Ц –Ь–∞–Ї—Б –Ъ–љ–Њ–ї–ї—М [en] –µ–ї–µ–Ї—В—А–Њ–љ–љ–Є–є –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ [ 22] –Т–µ–љ–і–µ–ї–ї –Ь–µ—А–µ–і—Ц—В –°—В–µ–љ–ї—Ц —А–µ—В–µ–ї—М–љ–Њ –≤–Є–≤—З–Є–≤ –≤—Ц—А—Г—Б —В—О—В—О–љ–Њ–≤–Њ—Ч –Љ–Њ–Ј–∞—Ч–Ї–Є –є –≤–Є—П–≤–Є–≤, —Й–Њ –≤—Ц–љ –Ј–і–µ–±—Ц–ї—М—И–Њ–≥–Њ —Б–Ї–ї–∞–і–∞—Ф—В—М—Б—П –Ј –±—Ц–ї–Ї–∞[ 23] –†–Э–Ъ -—Б–Ї–ї–∞–і–Њ–≤—Г[ 24] –Ї—А–Є—Б—В–∞–ї—Ц–Ј–Њ–≤–∞–љ–Њ –њ–µ—А—И–Є–Љ —Б–µ—А–µ–і –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –і–Њ–Ј–≤–Њ–ї–Є–ї–Њ –±–∞–≥–∞—В–Њ —З–Њ–≥–Њ –і—Ц–Ј–љ–∞—В–Є—Б—П –њ—А–Њ –є–Њ–≥–Њ —Б—В—А—Г–Ї—В—Г—А—Г. –Э–∞–њ—А–Є–Ї—Ц–љ—Ж—Ц 1930-—Е —А–Њ–Ї—Ц–≤ –С–µ—А–љ–∞–ї—М —Ц –§–µ–љ–Ї—Г—Е–µ–љ –Њ—В—А–Є–Љ–∞–ї–Є –њ–µ—А—И—Г —А–µ–љ—В–≥–µ–љ–Њ–≥—А–∞–Љ—Г –Ї—А–Є—Б—В–∞–ї—Ц–Ј–Њ–≤–∞–љ–Њ–≥–Њ –≤—Ц—А—Г—Б—Г. –Э–∞ –њ—Ц–і—Б—В–∞–≤—Ц –Ј—А–Њ–±–ї–µ–љ–Є—Е —Ж–Є–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –Ј–Њ–±—А–∞–ґ–µ–љ—М –†–Њ–Ј–∞–ї—Ц–љ–і –§—А–∞–љ–Ї–ї—Ц–љ 1955 —А–Њ–Ї—Г –≤–Є–Ј–љ–∞—З–Є–ї–∞ –њ–Њ–≤–љ—Г —Б—В—А—Г–Ї—В—Г—А—Г —Ж—М–Њ–≥–Њ –≤—Ц—А—Г—Б—Г[ 25] –•–µ–є–љ—Ж –Ы—О–і–≤—Ц–≥ –§—А–µ–љ–Ї–µ–ї—М-–Ъ–Њ–љ—А–∞—В —Ц –†–Њ–±–ї—Ц –Т—Ц–ї—М—П–Љ—Б [en]
–Ф—А—Г–≥–∞ –њ–Њ–ї–Њ–≤–Є–љ–∞ XX —Б—В–Њ–ї—Ц—В—В—П —Б—В–∞–ї–∞ –њ–µ—А—Ц–Њ–і–Њ–Љ —А–Њ–Ј–Ї–≤—Ц—В—Г –≤—Ц—А—Г—Б–Њ–ї–Њ–≥—Ц—Ч. –£ —В–Њ–є —З–∞—Б –±—Г–ї–Њ –≤—Ц–і–Ї—А–Є—В–Њ –њ–Њ–љ–∞–і 2000 –≤–Є–і—Ц–≤ –≤—Ц—А—Г—Б—Ц–≤ —В–≤–∞—А–Є–љ, —А–Њ—Б–ї–Є–љ —Ц –±–∞–Ї—В–µ—А—Ц–є[ 27] –∞—А—В–µ—А—Ц–≤—Ц—А—Г—Б [en] –≤—Ц—А—Г—Б–љ–Њ—Ч –і—Ц–∞—А–µ—Ч –Ї–Њ—А—Ц–≤ [en] –њ–µ—Б—В–Є–≤—Ц—А—Г—Б [en] –С–∞—А—Г—Е –С–ї–∞–Љ–±–µ—А–≥ –≤—Ц–і–Ї—А–Є–≤ –≤—Ц—А—Г—Б –≥–µ–њ–∞—В–Є—В—Г B , –∞ 1965 —А–Њ–Ї—Г –У–Њ–≤–∞—А–і –Ґ–µ–Љ—Ц–љ –Њ–њ–Є—Б–∞–≤ –њ–µ—А—И–Є–є —А–µ—В—А–Њ–≤—Ц—А—Г—Б . 1970 —А–Њ–Ї—Г –Ґ–µ–Љ—Ц–љ —Ц –Ф–µ–≤—Ц–і –С–∞–ї—В—Ц–Љ–Њ—А –љ–µ–Ј–∞–ї–µ–ґ–љ–Њ –Њ–і–Є–љ –≤—Ц–і –Њ–і–љ–Њ–≥–Њ –Њ–њ–Є—Б–∞–ї–Є –Ј–≤–Њ—А–Њ—В–љ—Г —В—А–∞–љ—Б–Ї—А–Є–њ—В–∞–Ј—Г , –Ї–ї—О—З–Њ–≤–Є–є —Д–µ—А–Љ–µ–љ—В , –Ј–∞ –і–Њ–њ–Њ–Љ–Њ–≥–Њ—О —П–Ї–Њ–≥–Њ —А–µ—В—А–Њ–≤—Ц—А—Г—Б–Є —Б–Є–љ—В–µ–Ј—Г—О—В—М –Ф–Э–Ъ -–Ї–Њ–њ—Ц—Ч —Б–≤–Њ—Ч—Е –†–Э–Ъ[ 29] –Ы—О–Ї–Њ–Љ –Ь–Њ–љ—В–∞–љ—М—Ф –Ј –Ж–љ—Б—В–Є—В—Г—В—Г –Я–∞—Б—В–µ—А–∞ —Г –§—А–∞–љ—Ж—Ц—Ч –≤–њ–µ—А—И–µ –≤–Є–і—Ц–ї–Є–ї–∞ —А–µ—В—А–Њ–≤—Ц—А—Г—Б, –≤—Ц–і–Њ–Љ–Є–є –љ–Є–љ—Ц —П–Ї –Т–Ж–Ы [ 30]
2002 —А–Њ–Ї—Г –≤ –Э—М—О-–Щ–Њ—А–Ї—Б—М–Ї–Њ–Љ—Г —Г–љ—Ц–≤–µ—А—Б–Є—В–µ—В—Ц —Б—В–≤–Њ—А–µ–љ–Њ –њ–µ—А—И–Є–є —Б–Є–љ—В–µ—В–Є—З–љ–Є–є –≤—Ц—А—Г—Б вАФ –њ–Њ–ї—Ц–Њ–≤—Ц—А—Г—Б [ 31]
–£ 2023 —А–Њ—Ж—Ц, —П–Ї –њ–Њ–≤—Ц–і–Њ–Љ–Є–≤ —А–µ—Б—Г—А—Б Sky News, —Г –≤–Њ–і–∞—Е –Ґ–Є—Е–Њ–≥–Њ –Њ–Ї–µ–∞–љ—Г –љ–∞ –≥–ї–Є–±–Є–љ—Ц 8900 –Љ–µ—В—А—Ц–≤ –≤ –Ь–∞—А—Ц–∞–љ—Б—М–Ї—Ц–є –Ј–∞–њ–∞–і–Є–љ—Ц –Ј–љ–∞–є—И–ї–Є –љ–µ–≤—Ц–і–Њ–Љ–Є–є –љ–∞—Г—Ж—Ц –≤—Ц—А—Г—Б, —П–Ї–Є–є –Њ—В—А–Є–Љ–∞–≤ –љ–∞–Ј–≤—Г vB_HmeY_H4907[ 32] [ 33]
–Т—Ц—А—Г—Б–Є –Ј–љ–∞–є–і–µ–љ–Њ —Б–Ї—А—Ц–Ј—М, –і–µ —Ф –ґ–Є—В—В—П, —Ц, –є–Љ–Њ–≤—Ц—А–љ–Њ, –≤–Њ–љ–Є —Ц—Б–љ—Г—О—В—М –≤—Ц–і –Љ–Є—В—Ц –њ–Њ—П–≤–Є –њ–µ—А—И–Є—Е –ґ–Є–≤–Є—Е –Ї–ї—Ц—В–Є–љ[ 34] –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ—Ч —Д—Ц–ї–Њ–≥–µ–љ–µ—В–Є–Ї–Є [ 35]
–Ч–≥—Ц–і–љ–Њ –Ј —Ж—Ц—Ф—О –≥—Ц–њ–Њ—В–µ–Ј–Њ—О, –≤—Ц—А—Г—Б–Є –Ї–Њ–ї–Є—Б—М –±—Г–ї–Є –і—А—Ц–±–љ–Є–Љ–Є –Ї–ї—Ц—В–Є–љ–∞–Љ–Є, —Й–Њ –њ–∞—А–∞–Ј–Є—В—Г—О—В—М —Г –±—Ц–ї—М—И–Є—Е –Ї–ї—Ц—В–Є–љ–∞—Е. –Ч –њ–ї–Є–љ–Њ–Љ —З–∞—Б—Г —Ж—Ц –Ї–ї—Ц—В–Є–љ–Є, –є–Љ–Њ–≤—Ц—А–љ–Њ, –≤—В—А–∞—В–Є–ї–Є –≥–µ–љ–Є, —П–Ї—Ц –±—Г–ї–Є ¬Ђ–Ј–∞–є–≤–Є–Љ–Є¬ї –Ј–∞ –њ–∞—А–∞–Ј–Є—В–Є—З–љ–Њ–≥–Њ —Б–њ–Њ—Б–Њ–±—Г –ґ–Є—В—В—П. –¶–µ –њ—А–Є–њ—Г—Й–µ–љ–љ—П “С—А—Г–љ—В—Г—Ф—В—М—Б—П –љ–∞ —Б–њ–Њ—Б—В–µ—А–µ–ґ–µ–љ–љ—Ц, —Й–Њ –і–µ—П–Ї—Ц –±–∞–Ї—В–µ—А—Ц—Ч, –∞ —Б–∞–Љ–µ —А–Є–Ї–µ—В—Б—Ц—Ч —В–∞ —Е–ї–∞–Љ—Ц–і—Ц—Ч , —Ф –Ї–ї—Ц—В–Є–љ–љ–Є–Љ–Є –Њ—А–≥–∞–љ—Ц–Ј–Љ–∞–Љ–Є, —П–Ї—Ц, –Њ–і–љ–∞–Ї, –њ–Њ–і—Ц–±–љ–Њ –і–Њ –≤—Ц—А—Г—Б—Ц–≤, –Љ–Њ–ґ—Г—В—М —А–Њ–Ј–Љ–љ–Њ–ґ—Г–≤–∞—В–Є—Б—П —В—Ц–ї—М–Ї–Є –≤—Б–µ—А–µ–і–Є–љ—Ц —Ц–љ—И–Њ—Ч –Ї–ї—Ц—В–Є–љ–Є. –¶—О –≥—Ц–њ–Њ—В–µ–Ј—Г —В–∞–Ї–Њ–ґ –љ–∞–Ј–Є–≤–∞—О—В—М –≥—Ц–њ–Њ—В–µ–Ј–Њ—О –і–µ–≥–µ–љ–µ—А–∞—Ж—Ц—Ч –∞–±–Њ –≥—Ц–њ–Њ—В–µ–Ј–Њ—О —А–µ–і—Г–Ї—Ж—Ц—Ч [ 40]
–Ф–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є –Љ–Њ–≥–ї–Є –Ј'—П–≤–Є—В–Є—Б—П –Ј —Д—А–∞–≥–Љ–µ–љ—В—Ц–≤ –Ф–Э–Ъ –∞–±–Њ –†–Э–Ъ, —Й–Њ ¬Ђ–≤—В–µ–Ї–ї–Є¬ї –Ј –≥–µ–љ–Њ–Љ—Г –±—Ц–ї—М—И–Њ–≥–Њ –Њ—А–≥–∞–љ—Ц–Ј–Љ—Г. –Ґ–∞–Ї—Ц —Д—А–∞–≥–Љ–µ–љ—В–Є –Љ–Њ–ґ—Г—В—М –њ–Њ—Е–Њ–і–Є—В–Є –≤—Ц–і –њ–ї–∞–Ј–Љ—Ц–і (–Љ–Њ–ї–µ–Ї—Г–ї –Ф–Э–Ъ, –Ј–і–∞—В–љ–Є—Е –њ–µ—А–µ–і–∞–≤–∞—В–Є—Б—П –≤—Ц–і –Ї–ї—Ц—В–Є–љ–Є –і–Њ –Ї–ї—Ц—В–Є–љ–Є) –∞–±–Њ –≤—Ц–і —В—А–∞–љ—Б–њ–Њ–Ј–Њ–љ—Ц–≤ (–Љ–Њ–ї–µ–Ї—Г–ї –Ф–Э–Ъ, —Й–Њ —А–µ–њ–ї—Ц–Ї—Г—О—В—М—Б—П —Ц –њ–µ—А–µ—Б—Г–≤–∞—О—В—М—Б—П –Ј –Љ—Ц—Б—Ж—П –љ–∞ –Љ—Ц—Б—Ж–µ –≤—Б–µ—А–µ–і–Є–љ—Ц –≥–µ–љ–Њ–Љ—Г). –Ґ—А–∞–љ—Б–њ–Њ–Ј–Њ–љ–Є, —Й–Њ —Ч—Е —А–∞–љ—Ц—И–µ –љ–∞–Ј–Є–≤–∞–ї–Є ¬Ђ–≥–µ–љ–∞–Љ–Є, —Й–Њ —Б—В—А–Є–±–∞—О—В—М¬ї, —Ф –њ—А–Є–Ї–ї–∞–і–∞–Љ–Є –Љ–Њ–±—Ц–ї—М–љ–Є—Е –µ–ї–µ–Љ–µ–љ—В—Ц–≤ –≥–µ–љ–Њ–Љ—Г , –Љ–Њ–ґ–ї–Є–≤–Њ, –≤—Ц–і –љ–Є—Е –Љ–Њ–≥–ї–Є –њ—Ц—В–Є –і–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є. –З—Е –≤—Ц–і–Ї—А–Є–ї–∞ –С–∞—А–±–∞—А–∞ –Ь–∞–Ї-–Ъ–ї—Ц–љ—В–Њ–Ї 1950 —А–Њ–Ї—Г –≤ –Ї—Г–Ї—Г—А—Г–і–Ј—Ц[ 42] –≥—Ц–њ–Њ—В–µ–Ј–Њ—О –Ї–Њ—З—Г–≤–∞–љ–љ—П –∞–±–Њ –≥—Ц–њ–Њ—В–µ–Ј–Њ—О –≤—В–µ—З—Ц [ 40]
–Ч–≥—Ц–і–љ–Њ –Ј —Ж—Ц—Ф—О –≥—Ц–њ–Њ—В–µ–Ј–Њ—О, –≤—Ц—А—Г—Б–Є –њ–Њ—Е–Њ–і—П—В—М –≤—Ц–і —Б–Ї–ї–∞–і–љ–Є—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б—Ц–≤ –±—Ц–ї–Ї—Ц–≤ —Ц –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Є—Е –Ї–Є—Б–ї–Њ—В –Њ–і–љ–Њ—З–∞—Б–љ–Њ –Ј –њ–µ—А—И–Є–Љ–Є –љ–∞ –Ч–µ–Љ–ї—Ц –ґ–Є–≤–Є–Љ–Є –Ї–ї—Ц—В–Є–љ–∞–Љ–Є, —Ц –Ј–∞–ї–µ–ґ–∞—В—М –≤—Ц–і –Ї–ї—Ц—В–Є–љ–љ–Њ–≥–Њ –ґ–Є—В—В—П –Њ—Б—М —Г–ґ–µ –Љ—Ц–ї—М—П—А–і–Є —А–Њ–Ї—Ц–≤. –Ъ—А—Ц–Љ –≤—Ц—А—Г—Б—Ц–≤, —Ц—Б–љ—Г—О—В—М —Ц —Ц–љ—И—Ц –љ–µ–Ї–ї—Ц—В–Є–љ–љ—Ц —Д–Њ—А–Љ–Є –ґ–Є—В—В—П. –Э–∞–њ—А–Є–Ї–ї–∞–і, –≤—Ц—А–Њ—Ч–і–Є вАФ —Ж–µ –Љ–Њ–ї–µ–Ї—Г–ї–Є –†–Э–Ъ, –Ї–Њ—В—А–Є—Е –љ–µ —А–Њ–Ј–≥–ї—П–і–∞—О—В—М —П–Ї –≤—Ц—А—Г—Б–Є, —З–µ—А–µ–Ј —В–µ —Й–Њ —Г –љ–Є—Е –љ–µ–Љ–∞—Ф –±—Ц–ї–Ї–Њ–≤–Њ—Ч –Њ–±–Њ–ї–Њ–љ–Ї–Є. –£—В—Ц–Љ, –љ–Є–Ј–Ї–∞ –≤–ї–∞—Б—В–Є–≤–Њ—Б—В–µ–є –Ј–±–ї–Є–ґ—Г—Ф —Ч—Е –Ј –і–µ—П–Ї–Є–Љ–Є –≤—Ц—А—Г—Б–∞–Љ–Є, –∞ —В–Њ–Љ—Г —Ч—Е –≤—Ц–і–љ–Њ—Б—П—В—М –і–Њ —Б—Г–±–≤—Ц—А—Г—Б–љ–Є—Е —З–∞—Б—В–Є–љ–Њ–Ї. –Т—Ц—А–Њ—Ч–і–Є —Ф –≤–∞–ґ–ї–Є–≤–Є–Љ–Є –њ–∞—В–Њ–≥–µ–љ–∞–Љ–Є —А–Њ—Б–ї–Є–љ. –Т–Њ–љ–Є –љ–µ –Ї–Њ–і—Г—О—В—М –≤–ї–∞—Б–љ—Ц –±—Ц–ї–Ї–Є, –Њ–і–љ–∞–Ї –≤–Ј–∞—Ф–Љ–Њ–і—Ц—О—В—М —Ц–Ј –Ї–ї—Ц—В–Є–љ–Њ—О-—Е–∞–Ј—П—Ч–љ–Њ–Љ —Ц –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М —Ч—Ч, –∞–±–Є —А–µ–њ–ї—Ц–Ї—Г–≤–∞—В–Є —Б–≤–Њ—О –†–Э–Ъ[ 46] –Т—Ц—А—Г—Б –≥–µ–њ–∞—В–Є—В—Г D –Љ–∞—Ф –†–Э–Ъ-–≥–µ–љ–Њ–Љ, –њ–Њ–і—Ц–±–љ–Є–є –і–Њ –≥–µ–љ–Њ–Љ—Г –≤—Ц—А–Њ—Ч–і—Ц–≤, –њ—А–Њ—В–µ —Б–∞–Љ –љ–µ –Ј–і–∞—В–љ–Є–є —Б–Є–љ—В–µ–Ј—Г–≤–∞—В–Є –±—Ц–ї–Њ–Ї –Њ–±–Њ–ї–Њ–љ–Ї–Є. –Ф–ї—П —Г—В–≤–Њ—А–µ–љ–љ—П –≤—Ц—А—Г—Б–љ–Є—Е —З–∞—Б—В–Є–љ–Њ–Ї –≤—Ц–љ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—Ф –±—Ц–ї–Њ–Ї –Ї–∞–њ—Б–Є–і—Г –≤—Ц—А—Г—Б—Г –≥–µ–њ–∞—В–Є—В—Г B —Ц –Љ–Њ–ґ–µ —А–Њ–Ј–Љ–љ–Њ–ґ—Г–≤–∞—В–Є—Б—П –ї–Є—И–µ –≤ –Ї–ї—Ц—В–Є–љ–∞—Е, –Ј–∞—А–∞–ґ–µ–љ–Є—Е —Ж–Є–Љ –≤—Ц—А—Г—Б–Њ–Љ. –Ю—В–ґ–µ, –≤—Ц—А—Г—Б –≥–µ–њ–∞—В–Є—В—Г D —Ф –і–µ—Д–µ–Ї—В–љ–Є–Љ –≤—Ц—А—Г—Б–Њ–Љ. –Я–Њ–і—Ц–±–љ–Њ –і–Њ —Ж—М–Њ–≥–Њ –≤—Ц—А–Њ—Д–∞–≥ –°—Г–њ—Г—В–љ–Є–Ї [en] –Љ—Ц–Љ—Ц–≤—Ц—А—Г—Б—Г , —П–Ї–Є–є —Г—А–∞–ґ–∞—Ф –љ–∞–є–њ—А–Њ—Б—В—Ц—И–µ Acanthamoeba castellanii [d] [ 48] –≤—Ц—А—Г—Б–∞–Љ–Є-—Б–∞—В–µ–ї—Ц—В–∞–Љ–Є . –Я–Њ–і—Ц–±–љ—Ц –≤—Ц—А—Г—Б–Є –і–µ–Љ–Њ–љ—Б—В—А—Г—О—В—М, —П–Ї –Љ–Њ–ґ–µ –≤–Є–≥–ї—П–і–∞—В–Є –њ—А–Њ–Љ—Ц–ґ–љ–∞ –ї–∞–љ–Ї–∞ –Љ—Ц–ґ –≤—Ц—А—Г—Б–∞–Љ–Є —Ц –≤—Ц—А–Њ—Ч–і–∞–Љ–Є.
–£ –Љ–Є–љ—Г–ї–Њ–Љ—Г –Ї–Њ–ґ–љ–∞ –Ј —Ж–Є—Е –≥—Ц–њ–Њ—В–µ–Ј –Љ–∞–ї–∞ —Б–≤–Њ—Ч —Б–ї–∞–±–Ї—Ц –Љ—Ц—Б—Ж—П: —А–µ–≥—А–µ—Б–Є–≤–љ–∞ –≥—Ц–њ–Њ—В–µ–Ј–∞ –љ–µ –њ–Њ—П—Б–љ—О–≤–∞–ї–∞, —З–Њ–Љ—Г –љ–∞–≤—Ц—В—М –љ–∞–є–і—А—Ц–±–љ—Ц—И—Ц –Ї–ї—Ц—В–Є–љ–љ—Ц –њ–∞—А–∞–Ј–Є—В–Є –љ—Ц—П–Ї –љ–µ —Б—Е–Њ–ґ—Ц –љ–∞ –≤—Ц—А—Г—Б–Є. –У—Ц–њ–Њ—В–µ–Ј–∞ –≤—В–µ—З—Ц –љ–µ –і–∞–≤–∞–ї–∞ –њ–Њ—П—Б–љ–µ–љ–љ—П –њ–Њ—П–≤–Є —Б–Ї–ї–∞–і–љ–Є—Е –Ї–∞–њ—Б–Є–і—Ц–≤ —В–∞ —Ц–љ—И–Є—Е —Б–Ї–ї–∞–і–љ–Є–Ї—Ц–≤ –≤—Ц—А—Г—Б–љ–Њ—Ч —З–∞—Б—В–Є–љ–Ї–Є. –У—Ц–њ–Њ—В–µ–Ј–∞ –Ї–Њ–µ–≤–Њ–ї—О—Ж—Ц—Ч —Б—Г–њ–µ—А–µ—З–Є–ї–∞ –≤–Є–Ј–љ–∞—З–µ–љ–љ—О –≤—Ц—А—Г—Б—Ц–≤ —П–Ї –љ–µ–Ї–ї—Ц—В–Є–љ–љ–Є—Е —З–∞—Б—В–Є–љ–Њ–Ї, –Ј–∞–ї–µ–ґ–љ–Є—Е –≤—Ц–і –Ї–ї—Ц—В–Є–љ-—Е–∞–Ј—П—Ч–≤[ 40] –і–Њ–Љ–µ–љ–Є . –¶–µ –≤—Ц–і–Ї—А–Є—В—В—П –і–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Б—Г—З–∞—Б–љ–Є–Љ –≤—Ц—А—Г—Б–Њ–ї–Њ–≥–∞–Љ –њ–µ—А–µ–≥–ї—П–љ—Г—В–Є —Ц –њ–µ—А–µ–Њ—Ж—Ц–љ–Є—В–Є —Ж—Ц —В—А–Є –Ї–ї–∞—Б–Є—З–љ—Ц –≥—Ц–њ–Њ—В–µ–Ј–Є[ 51]
–У—Ц–њ–Њ—В–µ–Ј–∞ —Б–≤—Ц—В—Г –†–Э–Ъ [ 52] –Ї–Њ–Љ–њ'—О—В–µ—А–љ–Є–є –∞–љ–∞–ї—Ц–Ј –њ–Њ—Б–ї—Ц–і–Њ–≤–љ–Њ—Б—В–µ–є –≤—Ц—А—Г—Б–љ–Њ—Ч –Ф–Э–Ъ —В–∞ –Ф–Э–Ъ —Е–∞–Ј—П—Ч–љ–∞ –і–∞—О—В—М –Ї—А–∞—Й–µ —А–Њ–Ј—Г–Љ—Ц–љ–љ—П –µ–≤–Њ–ї—О—Ж—Ц–є–љ–Є—Е –≤–Ј–∞—Ф–Љ–Є–љ –Љ—Ц–ґ —А—Ц–Ј–љ–Є–Љ–Є –≥—А—Г–њ–∞–Љ–Є –≤—Ц—А—Г—Б—Ц–≤ —Ц –Љ–Њ–ґ—Г—В—М –і–Њ–њ–Њ–Љ–Њ–≥—В–Є –≤–Є–Ј–љ–∞—З–Є—В–Є –њ—А–µ–і–Ї—Ц–≤ —Б—Г—З–∞—Б–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤. –Ф–Њ–њ–Њ–Ї–Є —Ж—Ц –і–Њ—Б–ї—Ц–і–ґ–µ–љ–љ—П –љ–µ –њ—А–Њ—П—Б–љ–Є–ї–Є, —П–Ї–∞ –Ј —В—А—М–Њ—Е –Њ—Б–љ–Њ–≤–љ–Є—Е –≥—Ц–њ–Њ—В–µ–Ј –њ—А–∞–≤–Є–ї—М–љ–∞. –Я—А–Њ—В–µ –Љ–∞–ї–Њ–є–Љ–Њ–≤—Ц—А–љ–Њ, —Й–Њ–±–Є –≤—Б—Ц —Б—Г—З–∞—Б–љ—Ц –≤—Ц—А—Г—Б–Є –Љ–∞–ї–Є —Б–њ—Ц–ї—М–љ–Њ–≥–Њ –њ—А–µ–і–Ї–∞, —Ц, –Љ–Њ–ґ–ї–Є–≤–Њ, –≤ –Љ–Є–љ—Г–ї–Њ–Љ—Г –≤—Ц—А—Г—Б–Є –љ–µ–Ј–∞–ї–µ–ґ–љ–Њ –≤–Є–љ–Є–Ї–∞–ї–Є –Ї—Ц–ї—М–Ї–∞ —А–∞–Ј—Ц–≤ –Ј–∞ –Њ–і–љ–Є–Љ –∞–±–Њ –Ї—Ц–ї—М–Ї–Њ–Љ–∞ –Љ–µ—Е–∞–љ—Ц–Ј–Љ–∞–Љ–Є, –±–Њ –Љ—Ц–ґ —А—Ц–Ј–љ–Є–Љ–Є –≥—А—Г–њ–∞–Љ–Є –≤—Ц—А—Г—Б—Ц–≤ —Ф –Ј–љ–∞—З–љ—Ц –≤—Ц–і–Љ—Ц–љ–љ–Њ—Б—В—Ц –≤ –Њ—А–≥–∞–љ—Ц–Ј–∞—Ж—Ц—Ч –≥–µ–љ–µ—В–Є—З–љ–Њ–≥–Њ –Љ–∞—В–µ—А—Ц–∞–ї—Г.
–Я—А–µ–њ–∞—А–∞—В –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–Ї—Г –Ї–Њ—А–Њ–≤–Є, —Г—А–∞–ґ–µ–љ–Њ—Ч –Ї–Њ—А–Њ–≤'—П—З–Є–Љ —Б–Ї–∞–Ј–Њ–Љ. –£ —Б—Ц—А—Ц–є —А–µ—З–Њ–≤–Є–љ—Ц —Г—В–≤–Њ—А—О—О—В—М—Б—П –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ—Ц—З–љ—Ц –њ–Њ—А–Њ–ґ–љ–Є–љ–Є, —П–Ї—Ц –љ–∞–і–∞—О—В—М —В–Ї–∞–љ–Є–љ—Ц –≤–Є–≥–ї—П–і—Г –≥—Г–±–Ї–Є –Я—А—Ц–Њ–љ–Є вАФ —Ж–µ —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ—Ц –±—Ц–ї–Ї–Њ–≤—Ц –Љ–Њ–ї–µ–Ї—Г–ї–Є, —П–Ї—Ц –љ–µ –Љ—Ц—Б—В—П—В—М –Ф–Э–Ъ –∞–±–Њ –†–Э–Ъ[ 54] —Б–Ї—А–µ–њ—Ц –≤ –Њ–≤–µ—З–Њ–Ї, –≥—Г–±—З–∞—Б—В–Њ–њ–Њ–і—Ц–±–љ–∞ –µ–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В—Ц—П –≤–µ–ї–Є–Ї–Њ—Ч —А–Њ–≥–∞—В–Њ—Ч —Е—Г–і–Њ–±–Є —В–∞ —Е—А–Њ–љ—Ц—З–љ–∞ —Б–ї–∞–±–Ї—Ц—Б—В—М (–∞–љ–≥–ї. chronic wasting disease ) —Г –Њ–ї–µ–љ–µ–≤–Є—Е. –Ф–Њ –њ—А—Ц–Њ–љ–Њ–≤–Є—Е —Е–≤–Њ—А–Њ–± –ї—О–і–Є–љ–Є –≤—Ц–і–љ–Њ—Б—П—В—М –Ї—Г—А—Г , —Е–≤–Њ—А–Њ–±—Г –Ъ—А–Њ–є—В—Ж—Д–µ–ї—М–і–∞ вАФ –ѓ–Ї–Њ–±–∞ —В–∞ —Б–Є–љ–і—А–Њ–Љ –У–µ—А—Б—В–Љ–∞–љ–∞ вАФ –®—В—А–Њ–є—Б–ї–µ—А–∞ вАФ –®–µ–є–љ–Ї–µ—А–∞ [ 55] –Я—А—Ц–Њ–љ–Њ–≤–Є–є –±—Ц–ї–Њ–Ї –Ј–і–∞—В–µ–љ —Ц—Б–љ—Г–≤–∞—В–Є —Г –і–≤–Њ—Е —Ц–Ј–Њ—Д–Њ—А–Љ–∞—Е : –љ–Њ—А–Љ–∞–ї—М–љ—Ц–є (PrPC ) —В–∞ –њ—А—Ц–Њ–љ–Њ–≤—Ц–є (PrPSc ). –Я—А—Ц–Њ–љ–Њ–≤–∞ —Д–Њ—А–Љ–∞, –≤–Ј–∞—Ф–Љ–Њ–і—Ц—О—З–Є –Ј –љ–Њ—А–Љ–∞–ї—М–љ–Є–Љ –±—Ц–ї–Ї–Њ–Љ, —Б–њ—А–Є—П—Ф –є–Њ–≥–Њ –њ–µ—А–µ—В–≤–Њ—А–µ–љ–љ—О –љ–∞ –њ—А—Ц–Њ–љ–Њ–≤—Г —Д–Њ—А–Љ—Г. –•–Њ—З–∞ –њ—А—Ц–Њ–љ–Є “С—А—Г–љ—В–Њ–≤–љ–Њ –≤—Ц–і—А—Ц–Ј–љ—П—О—В—М—Б—П –≤—Ц–і –≤—Ц—А—Г—Б—Ц–≤ —Ц –≤—Ц—А–Њ—Ч–і—Ц–≤, —Ч—Е –≤—Ц–і–Ї—А–Є—В—В—П –і–∞—Ф –±—Ц–ї—М—И–µ –њ—Ц–і—Б—В–∞–≤ –њ–Њ–≤—Ц—А–Є—В–Є –≤ —В–µ, —Й–Њ –≤—Ц—А—Г—Б–Є –Љ–Њ–≥–ї–Є –њ—Ц—В–Є –≤—Ц–і —Б–∞–Љ–Њ–≤—Ц–і—В–≤–Њ—А—О–≤–∞–љ–Є—Е –Љ–Њ–ї–µ–Ї—Г–ї[ 56]
–Я–Њ–Ї–Є –≤—Ц—А—Г—Б –њ–µ—А–µ–±—Г–≤–∞—Ф –≤ –њ–Њ–Ј–∞–Ї–ї—Ц—В–Є–љ–љ–Њ–Љ—Г —Б–µ—А–µ–і–Њ–≤–Є—Й—Ц –∞–±–Њ –≤ –њ—А–Њ—Ж–µ—Б—Ц –Ј–∞—А–∞–ґ–µ–љ–љ—П –Ї–ї—Ц—В–Є–љ–Є, –≤—Ц–љ —Ц—Б–љ—Г—Ф —Г –≤–Є–≥–ї—П–і—Ц –љ–µ–Ј–∞–ї–µ–ґ–љ–Њ—Ч —З–∞—Б—В–Є–љ–Ї–Є. –Т—Ц—А—Г—Б–љ—Ц —З–∞—Б—В–Є–љ–Ї–Є (–≤—Ц—А—Ц–Њ–љ–Є ) —Б–Ї–ї–∞–і–∞—О—В—М—Б—П –Ј –і–≤–Њ—Е —З–Є —В—А—М–Њ—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Ц–≤: –≥–µ–љ–µ—В–Є—З–љ–Њ–≥–Њ –Љ–∞—В–µ—А—Ц–∞–ї—Г —Г –≤–Є–≥–ї—П–і—Ц –Ф–Э–Ъ –∞–±–Њ –†–Э–Ъ (–і–µ—П–Ї—Ц, –љ–∞–њ—А–Є–Ї–ї–∞–і –Љ—Ц–Љ—Ц–≤—Ц—А—Г—Б–Є , –Љ–∞—О—В—М –Њ–±–Є–і–≤–∞ —В–Є–њ–Є –Љ–Њ–ї–µ–Ї—Г–ї); –±—Ц–ї–Ї–Њ–≤–Њ—Ч –Њ–±–Њ–ї–Њ–љ–Ї–Є (–Ї–∞–њ—Б–Є–і—Г ), —Й–Њ –Ј–∞—Е–Є—Й–∞—Ф —Ж—Ц –Љ–Њ–ї–µ–Ї—Г–ї–Є, —Ц, –≤ –і–µ—П–Ї–Є—Е –≤–Є–њ–∞–і–Ї–∞—Е, вАФ –і–Њ–і–∞—В–Ї–Њ–≤–Є—Е –ї—Ц–њ—Ц–і–љ–Є—Е –Њ–±–Њ–ї–Њ–љ–Њ–Ї. –Э–∞—П–≤–љ—Ц—Б—В—М –Ї–∞–њ—Б–Є–і—Г –≤—Ц–і—А—Ц–Ј–љ—П—Ф –≤—Ц—А—Г—Б–Є –≤—Ц–і –≤—Ц—А—Г—Б–Њ–њ–Њ–і—Ц–±–љ–Є—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є—Е –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Є—Е –Ї–Є—Б–ї–Њ—В вАФ –≤—Ц—А–Њ—Ч–і—Ц–≤ . –Ч–∞–ї–µ–ґ–љ–Њ –≤—Ц–і —В–Њ–≥–Њ, —П–Ї–Є–Љ —В–Є–њ–Њ–Љ –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –≥–µ–љ–µ—В–Є—З–љ–Є–є –Љ–∞—В–µ—А—Ц–∞–ї, –≤–Є–і—Ц–ї—П—О—В—М –Ф–Э–Ъ-–≤–Љ—Ц—Б–љ—Ц –≤—Ц—А—Г—Б–Є [en] –†–Э–Ъ-–≤–Љ—Ц—Б–љ—Ц –≤—Ц—А—Г—Б–Є [ru] –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—П –≤—Ц—А—Г—Б—Ц–≤ –Ј–∞ –С–∞–ї—В—Ц–Љ–Њ—А–Њ–Љ [en] –њ—А—Ц–Њ–љ–Є , –Њ–і–љ–∞–Ї –Ј–≥–Њ–і–Њ–Љ –≤–Є—П–≤–Є–ї–Њ—Б—П, —Й–Њ —Ж—Ц –Ј–±—Г–і–љ–Є–Ї–Є —Ф –Њ—Б–Њ–±–ї–Є–≤–Є–Љ–Є —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є–Љ–Є –±—Ц–ї–Ї–∞–Љ–Є —Ц –љ–µ –Љ—Ц—Б—В—П—В—М –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Є—Е –Ї–Є—Б–ї–Њ—В. –§–Њ—А–Љ–∞ –≤—Ц—А—Г—Б—Ц–≤ —А—Ц–Ј–љ–Є—В—М—Б—П –≤—Ц–і –њ—А–Њ—Б—В–Њ—Ч —Б–њ—Ц—А–∞–ї—М–љ–Њ—Ч —В–∞ —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ–Њ—Ч –і–Њ —Б–Ї–ї–∞–і–љ—Ц—И–Є—Е —Б—В—А—Г–Ї—В—Г—А. –†–Њ–Ј–Љ—Ц—А–Є —Б–µ—А–µ–і–љ—М–Њ–≥–Њ –≤—Ц—А—Г—Б—Г —Б—В–∞–љ–Њ–≤–ї—П—В—М –±–ї–Є–Ј—М–Ї–Њ –Њ–і–љ—Ц—Ф—Ч —Б–Њ—В–Њ—Ч —А–Њ–Ј–Љ—Ц—А—Г —Б–µ—А–µ–і–љ—М–Њ—Ч –±–∞–Ї—В–µ—А—Ц—Ч. –С—Ц–ї—М—И—Ц—Б—В—М –≤—Ц—А—Г—Б—Ц–≤ –Ј–∞–љ–∞–і—В–Њ –Љ–∞–ї—Ц, —Й–Њ–±–Є –±—Г—В–Є —З—Ц—В–Ї–Њ –њ–Њ–Љ—Ц—В–љ–Є–Љ–Є –њ—Ц–і –Њ–њ—В–Є—З–љ–Є–Љ –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ–Њ–Љ .
–Т—Ц—А—Г—Б–Є —Ф –Њ–±–ї—Ц–≥–∞—В–љ–Є–Љ–Є –њ–∞—А–∞–Ј–Є—В–∞–Љ–Є , —В–Њ–Љ—Г —Й–Њ –љ–µ –Ј–і–∞—В–љ—Ц —А–Њ–Ј–Љ–љ–Њ–ґ—Г–≤–∞—В–Є—Б—П –њ–Њ–Ј–∞ –Ї–ї—Ц—В–Є–љ–Њ—О. –Я–Њ–Ј–∞ –Ї–ї—Ц—В–Є–љ–Њ—О –≤—Ц—А—Г—Б–љ—Ц —З–∞—Б—В–Є–љ–Ї–Є –љ–µ –≤–Є—П–≤–ї—П—О—В—М –Њ–Ј–љ–∞–Ї –ґ–Є–≤–Њ–≥–Њ —Ц –њ–Њ–≤–Њ–і—П—В—М—Б—П —П–Ї —З–∞—Б—В–Є–љ–Ї–Є –±—Ц–Њ–њ–Њ–ї—Ц–Љ–µ—А—Ц–≤ . –Т—Ц–і –ґ–Є–≤–Є—Е –њ–∞—А–∞–Ј–Є—В–∞—А–љ–Є—Е –Њ—А–≥–∞–љ—Ц–Ј–Љ—Ц–≤ –≤—Ц—А—Г—Б–Є –≤—Ц–і—А—Ц–Ј–љ—П—О—В—М—Б—П –њ–Њ–≤–љ–Њ—О –≤—Ц–і—Б—Г—В–љ—Ц—Б—В—О –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –µ–љ–µ—А–≥–µ—В–Є—З–љ–Њ–≥–Њ –Њ–±–Љ—Ц–љ—Г —Ц –≤—Ц–і—Б—Г—В–љ—Ц—Б—В—О –љ–∞–є—Б–Ї–ї–∞–і–љ—Ц—И–Њ–≥–Њ –µ–ї–µ–Љ–µ–љ—В–∞ –ґ–Є–≤–Є—Е —Б–Є—Б—В–µ–Љ вАФ –∞–њ–∞—А–∞—В—Г —В—А–∞–љ—Б–ї—П—Ж—Ц—Ч (—Б–Є–љ—В–µ–Ј—Г –±—Ц–ї–Ї–∞), —Б–Ї–ї–∞–і–љ—Ц—Б—В—М —П–Ї–Њ–≥–Њ –њ–µ—А–µ–≤–Є—Й—Г—Ф —Б–Ї–ї–∞–і–љ—Ц—Б—В—М —Б–∞–Љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤.
–Ч–∞ –Њ–і–љ–Є–Љ —Ц–Ј –≤–Є–Ј–љ–∞—З–µ–љ—М –≤—Ц—А—Г—Б–Є —Ф —Д–Њ—А–Љ–Њ—О –ґ–Є—В—В—П, –Ј–∞ —Ц–љ—И–Є–Љ –≤—Ц—А—Г—Б–Є —Ф –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞–Љ–Є –Њ—А–≥–∞–љ—Ц—З–љ–Є—Е –Љ–Њ–ї–µ–Ї—Г–ї , —Й–Њ –≤–Ј–∞—Ф–Љ–Њ–і—Ц—О—В—М –Ј –ґ–Є–≤–Є–Љ–Є –Њ—А–≥–∞–љ—Ц–Ј–Љ–∞–Љ–Є. –Т—Ц—А—Г—Б–Є –≤–Є–Ј–љ–∞—З–∞—О—В—М —П–Ї ¬Ђ–Њ—А–≥–∞–љ—Ц–Ј–Љ–Є –љ–∞ –Љ–µ–ґ—Ц –ґ–Є–≤–Њ–≥–Њ¬ї[ 15] –µ–≤–Њ–ї—О—Ж—Ц—О—О—В—М —И–ї—П—Е–Њ–Љ –њ—А–Є—А–Њ–і–љ–Њ–≥–Њ –і–Њ–±–Њ—А—Г [ 57] –Њ–±–Љ—Ц–љ—Г —А–µ—З–Њ–≤–Є–љ , —Ц –і–ї—П —Б–Є–љ—В–µ–Ј—Г –≤–ї–∞—Б–љ–Є—Е –Љ–Њ–ї–µ–Ї—Г–ї –≤–Њ–љ–Є –њ–Њ—В—А–µ–±—Г—О—В—М –Ї–ї—Ц—В–Є–љ–Є-—Е–∞–Ј—П—Ч–љ–∞. –І–µ—А–µ–Ј —Ж–µ –≤–Њ–љ–Є –љ–µ –Ј–і–∞—В–љ—Ц —А–Њ–Ј–Љ–љ–Њ–ґ—Г–≤–∞—В–Є—Б—П –њ–Њ–Ј–∞ –Ї–ї—Ц—В–Є–љ–Њ—О[ 58] —А–Є–Ї–µ—В—Б—Ц—Ч —В–∞ —Е–ї–∞–Љ—Ц–і—Ц—Ч , –њ–Њ–њ—А–Є —В–µ, —Й–Њ –≤–Њ–љ–Є –љ–µ –Љ–Њ–ґ—Г—В—М —А–Њ–Ј–Љ–љ–Њ–ґ—Г–≤–∞—В–Є—Б—П –њ–Њ–Ј–∞ –Ї–ї—Ц—В–Є–љ–Њ—О —Е–∞–Ј—П—Ч–љ–∞, –≤–≤–∞–ґ–∞—О—В—М –ґ–Є–≤–Є–Љ–Є –Њ—А–≥–∞–љ—Ц–Ј–Љ–∞–Љ–Є[ 59] [ 60] –њ–Њ–і—Ц–ї–Њ–Љ –Ї–ї—Ц—В–Є–љ–Є , —В–Њ–і—Ц —П–Ї –≤—Ц—А—Г—Б–љ—Ц —З–∞—Б—В–Є–љ–Ї–Є –Љ–Є–Љ–Њ–≤—Ц–ї—М–љ–Њ –Ј–±–Є—А–∞—О—В—М—Б—П –≤ —Ц–љ—Д—Ц–Ї–Њ–≤–∞–љ—Ц–є –Ї–ї—Ц—В–Є–љ—Ц. –Т—Ц–і —А–Њ—Б—В—Г –Ї—А–Є—Б—В–∞–ї—Ц–≤ —А–Њ–Ј–Љ–љ–Њ–ґ–µ–љ–љ—П –≤—Ц—А—Г—Б—Ц–≤ –≤—Ц–і—А—Ц–Ј–љ—П—Ф—В—М—Б—П —В–Є–Љ, —Й–Њ –≤—Ц—А—Г—Б–Є —Г—Б–њ–∞–і–Ї–Њ–≤—Г—О—В—М –Љ—Г—В–∞—Ж—Ц—Ч —Ц –њ–µ—А–µ–±—Г–≤–∞—О—В—М –њ—Ц–і —В–Є—Б–Ї–Њ–Љ –њ—А–Є—А–Њ–і–љ–Њ–≥–Њ –і–Њ–±–Њ—А—Г. –°–∞–Љ–Њ—Б–Ї–ї–∞–і–∞–љ–љ—П –≤—Ц—А—Г—Б–љ–Є—Е —З–∞—Б—В–Є–љ–Њ–Ї —Г –Ї–ї—Ц—В–Є–љ—Ц –і–∞—Ф –і–Њ–і–∞—В–Ї–Њ–≤–µ –њ—Ц–і—В–≤–µ—А–і–ґ–µ–љ–љ—П –≥—Ц–њ–Њ—В–µ–Ј–Є, —Й–Њ –ґ–Є—В—В—П –Љ–Њ–≥–ї–Њ –Ј–∞—А–Њ–і–Є—В–Є—Б—П —Г –≤–Є–≥–ї—П–і—Ц –Њ—А–≥–∞–љ—Ц—З–љ–Є—Е –Љ–Њ–ї–µ–Ї—Г–ї, —Й–Њ —Б–∞–Љ–Њ—Б–Ї–ї–∞–і–∞—О—В—М—Б—П [en] [ 1] [ 61]
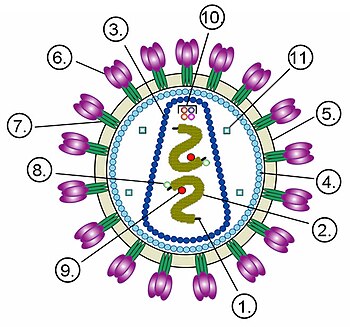
–С—Г–і–Њ–≤–∞ —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ–Є—Е –≤—Ц—А—Ц–Њ–љ—Ц–≤: –њ—Ц–Ї–Њ—А–љ–∞–≤—Ц—А—Г—Б ). –≥–µ—А–њ–µ—Б–≤—Ц—А—Г—Б ). –Я–∞–ї–Њ—З–Ї–Њ–њ–Њ–і—Ц–±–љ–Є–є –≤—Ц—А—Ц–Њ–љ –≤—Ц—А—Г—Б—Г —В—О—В—О–љ–Њ–≤–Њ—Ч –Љ–Њ–Ј–∞—Ч–Ї–Є . –¶–Є—Д—А–∞–Љ–Є –њ–Њ–Ј–љ–∞—З–µ–љ–Њ: (1) –†–Э–Ъ-–≥–µ–љ–Њ–Љ –≤—Ц—А—Г—Б—Г, (2) –Ї–∞–њ—Б–Њ–Љ–µ—А, —Й–Њ —Б–Ї–ї–∞–і–∞—Ф—В—М—Б—П –ї–Є—И–µ –Ј –Њ–і–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–Љ–µ—А–∞ , (3) –Ј—А—Ц–ї–∞ –і—Ц–ї—П–љ–Ї–∞ –Ї–∞–њ—Б–Є–і—Г –С—Г–і–Њ–≤–∞ –≤—Ц—А—Ц–Њ–љ–∞ –љ–µ—Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ–Њ–≥–Њ –Њ–±–Њ–ї–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –≤—Ц—А—Г—Б—Г –љ–∞ –њ—А–Є–Ї–ї–∞–і—Ц –Т–Ж–Ы . –¶–Є—Д—А–∞–Љ–Є –њ–Њ–Ј–љ–∞—З–µ–љ–Њ: (1) –†–Э–Ъ-–≥–µ–љ–Њ–Љ –≤—Ц—А—Г—Б—Г, (2) –љ—Г–Ї–ї–µ–Њ–Ї–∞–њ—Б–Є–і, (3) –Ї–∞–њ—Б–Є–і, (4) –±—Ц–ї–Ї–Њ–≤–Є–є –Љ–∞—В—А–Є–Ї—Б, —Й–Њ –њ—Ц–і—Б—В–Є–ї–∞—Ф (5) –ї—Ц–њ—Ц–і–љ—Г –Љ–µ–Љ–±—А–∞–љ—Г, (6) gp120 вАФ –≥–ї—Ц–Ї–Њ–њ—А–Њ—В–µ—Ч–љ, –Ј–∞ –і–Њ–њ–Њ–Љ–Њ–≥–Њ—О —П–Ї–Њ–≥–Њ –≤—Ц–і–±—Г–≤–∞—Ф—В—М—Б—П –Ј–≤'—П–Ј—Г–≤–∞–љ–љ—П –≤—Ц—А—Г—Б—Г –Ј –Ї–ї—Ц—В–Є–љ–љ–Њ—О –Љ–µ–Љ–±—А–∞–љ–Њ—О, (7) gp41 вАФ –≥–ї—Ц–Ї–Њ–њ—А–Њ—В–µ—Ч–љ.–Ј–≤–Њ—А–Њ—В–љ–∞ —В—А–∞–љ—Б–Ї—А–Є–њ—В–∞–Ј–∞ , (10) вАФ Vif, Vpr, Nef —Ц p7, (11) вАФ –њ—А–Њ—В–µ–∞–Ј–∞
–Т—Ц—А—Г—Б–Є –і—Г–ґ–µ —А—Ц–Ј–љ—П—В—М—Б—П –Ј–∞ —Д–Њ—А–Љ–Њ—О —В–∞ —А–Њ–Ј–Љ—Ц—А–Њ–Љ. –Ч–∞–Ј–≤–Є—З–∞–є, –≤–Њ–љ–Є –Ј–љ–∞—З–љ–Њ –і—А—Ц–±–љ—Ц—И—Ц –Ј–∞ –±–∞–Ї—В–µ—А—Ц—Ч. –С—Ц–ї—М—И—Ц—Б—В—М –≤–Є–≤—З–µ–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –Љ–∞—О—В—М –і—Ц–∞–Љ–µ—В—А —Г –Љ–µ–ґ–∞—Е –≤—Ц–і 20 –і–Њ 300 –љ–Љ . –Ф–µ—П–Ї—Ц —Д—Ц–ї–Њ–≤—Ц—А—Г—Б–Є –Ј–∞–≤–і–Њ–≤–ґ–Ї–Є –і–Њ 1400 –љ–Љ, –∞ —Ч—Е–љ—Ц–є –і—Ц–∞–Љ–µ—В—А —Б—В–∞–љ–Њ–≤–Є—В—М –ї–Є—И–µ 80 –љ–Љ. 2013 —А–Њ–Ї—Г –љ–∞–є–±—Ц–ї—М—И–Є–Љ –Ј –≤—Ц–і–Њ–Љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –≤–≤–∞–ґ–∞–ї–Є –њ–∞–љ–і–Њ—А–∞–≤—Ц—А—Г—Б 1 √Ч 0,5 –Љ–Ї–Љ , –Њ–і–љ–∞–Ї 2014 —А–Њ–Ї—Г –Ј –±–∞–≥–∞—В–Њ—А—Ц—З–љ–Њ—Ч –Љ–µ—А–Ј–ї–Њ—В–Є –Ј –°–Є–±—Ц—А—Г –Њ–њ–Є—Б–∞–љ–Њ Pithovirus [ 63] –Њ–њ—В–Є—З–љ–Є–є –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ , —В–Њ–Љ—Г –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М –µ–ї–µ–Ї—В—А–Њ–љ–љ—Ц вАФ —Ц —Б–Ї–∞–љ—Г–≤–∞–ї—М–љ—Ц , —Ц —В—А–∞–љ—Б–Љ—Ц—Б—Ц–є–љ—Ц . –Р–±–Є –≤—Ц—А—Г—Б–Є —А—Ц–Ј–Ї–Њ –≤–Є–і—Ц–ї—П–ї–Є—Б—П –љ–∞ –љ–∞–≤–Ї–Њ–ї–Є—И–љ—М–Њ–Љ—Г —В–ї—Ц, –Ј–∞—Б—В–Њ—Б–Њ–≤—Г—О—В—М –µ–ї–µ–Ї—В—А–Њ–љ–љ–Њ—Й—Ц–ї—М–љ—Ц ¬Ђ–±–∞—А–≤–љ–Є–Ї–Є¬ї. –Т–Њ–љ–Є —Ф —А–Њ–Ј—З–Є–љ–∞–Љ–Є —Б–Њ–ї–µ–є –≤–∞–ґ–Ї–Є—Е –Љ–µ—В–∞–ї—Ц–≤ , –љ–∞–њ—А–Є–Ї–ї–∞–і, –≤–Њ–ї—М—Д—А–∞–Љ—Г , —Й–Њ —А–Њ–Ј—Б—Ц—О—О—В—М –µ–ї–µ–Ї—В—А–Њ–љ–Є –љ–∞ –њ–Њ–Ї—А–Є—В—Ц–є –љ–Є–Љ–Є –њ–Њ–≤–µ—А—Е–љ—Ц. –Ю–і–љ–∞–Ї –Њ–±—А–Њ–±–Ї–∞ —В–∞–Ї–Є–Љ–Є —А–µ—З–Њ–≤–Є–љ–∞–Љ–Є –њ–Њ–≥—Ц—А—И—Г—Ф –≤–Є–і–Є–Љ—Ц—Б—В—М –і—А—Ц–±–љ–Є—Е –і–µ—В–∞–ї–µ–є. –¶—О –њ—А–Њ–±–ї–µ–Љ—Г –≤–Є—А—Ц—И—Г—Ф –љ–µ–≥–∞—В–Є–≤–љ–µ –Ї–Њ–љ—В—А–∞—Б—В—Г–≤–∞–љ–љ—П [en] [ 65]
–Ю–Ї—А–µ–Љ–∞ –≤—Ц—А—Г—Б–љ–∞ —З–∞—Б—В–Є–љ–Ї–∞, –≤—Ц–і–Њ–Љ–∞ —П–Ї –≤—Ц—А—Ц–Њ–љ, —Б–Ї–ї–∞–і–∞—Ф—В—М—Б—П –Ј –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є, –њ–Њ–Ї—А–Є—В–Њ—Ч –Ј–∞—Е–Є—Б–љ–Њ—О –±—Ц–ї–Ї–Њ–≤–Њ—О –Њ–±–Њ–ї–Њ–љ–Ї–Њ—О вАФ –Ї–∞–њ—Б–Є–і–Њ–Љ. –Ъ–∞–њ—Б–Є–і —Б–Ї–ї–∞–і–∞—Ф—В—М—Б—П –Ј –Њ–і–љ–∞–Ї–Њ–≤–Є—Е –±—Ц–ї–Ї–Њ–≤–Є—Е —Б—Г–±–Њ–і–Є–љ–Є—Ж—М, —П–Ї—Ц –љ–∞–Ј–Є–≤–∞—О—В—М—Б—П –Ї–∞–њ—Б–Њ–Љ–µ—А–∞–Љ–Є [en] [–і–ґ–µ—А–µ–ї–Њ? .
–Т—Ц—А—Г—Б–Є –Љ–Њ–ґ—Г—В—М —В–∞–Ї–Њ–ґ –Љ–∞—В–Є –ї—Ц–њ—Ц–і–љ—Г –Њ–±–Њ–ї–Њ–љ–Ї—Г –љ–∞–≤–Ї–Њ–ї–Њ –Ї–∞–њ—Б–Є–і—Г (—Б—Г–њ–µ—А–Ї–∞–њ—Б–Є–і –Љ–µ–Љ–±—А–∞–љ–Є –Ї–ї—Ц—В–Є–љ–Є-—Е–∞–Ј—П—Ч–љ–∞. –Ъ–∞–њ—Б–Є–і —Б–Ї–ї–∞–і–∞—Ф—В—М—Б—П –Ј –±—Ц–ї–Ї—Ц–≤, —Й–Њ –Ї–Њ–і—Г—О—В—М—Б—П –≤—Ц—А—Г—Б–љ–Є–Љ –≥–µ–љ–Њ–Љ–Њ–Љ, –∞ –є–Њ–≥–Њ —Д–Њ—А–Љ–∞ –ї–µ–ґ–Є—В—М –≤ –Њ—Б–љ–Њ–≤—Ц –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—Ч –≤—Ц—А—Г—Б—Ц–≤ –Ј–∞ –Љ–Њ—А—Д–Њ–ї–Њ–≥—Ц—З–љ–Њ—О –Њ–Ј–љ–∞–Ї–Њ—О[ 67] [ 68] –љ—Г–Ї–ї–µ–Њ–њ—А–Њ—В–µ—Ч–љ–Є –љ—Г–Ї–ї–µ–Њ–Ї–∞–њ—Б–Є–і–Њ–Љ . –§–Њ—А–Љ—Г –Ї–∞–њ—Б–Є–і—Г —Ц –≤—Ц—А—Ц–Њ–љ–∞ –≤ —Ж—Ц–ї–Њ–Љ—Г –Љ–Њ–ґ–љ–∞ –Љ–µ—Е–∞–љ—Ц—З–љ–Њ (—Д—Ц–Ј–Є—З–љ–Њ) –і–Њ—Б–ї—Ц–і–Є—В–Є –Ј–∞ –і–Њ–њ–Њ–Љ–Њ–≥–Њ—О –∞—В–Њ–Љ–љ–Њ-—Б–Є–ї–Њ–≤–Њ–≥–Њ –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ–∞ [ 69] [ 70] [–і–ґ–µ—А–µ–ї–Њ? .
–Ъ–ї–∞—Б–Є—Д—Ц–Ї—Г—О—В—М —З–Њ—В–Є—А–Є –Љ–Њ—А—Д–Њ–ї–Њ–≥—Ц—З–љ—Ц —В–Є–њ–Є –Ї–∞–њ—Б–Є–і—Ц–≤ –≤—Ц—А—Г—Б—Ц–≤: —Б–њ—Ц—А–∞–ї—М–љ–Є–є, —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ–Є–є, –і–Њ–≤–≥–∞—Б—В–Є–є —Ц –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Є–є.
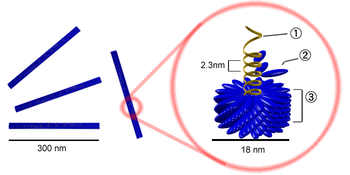
–¶—Ц –Ї–∞–њ—Б–Є–і–Є —Б–Ї–ї–∞–і–∞—О—В—М—Б—П –Ј –Њ–і–љ–Њ–≥–Њ —В–Є–њ—Г –Ї–∞–њ—Б–Њ–Љ–µ—А—Ц–≤, —Г–Ї–ї–∞–і–µ–љ–Є—Е —Б–њ—Ц—А–∞–ї–ї—О –љ–∞–≤–Ї–Њ–ї–Њ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ—Ч –Њ—Б—Ц. –£ —Ж–µ–љ—В—А—Ц —Ж—Ц—Ф—Ч —Б—В—А—Г–Ї—В—Г—А–Є –Љ–Њ–ґ–µ –±—Г—В–Є –њ–Њ—А–Њ–ґ–љ–Є–љ–∞ –∞–±–Њ –Ї–∞–љ–∞–ї. –Ґ–∞–Ї–∞ –Њ—А–≥–∞–љ—Ц–Ј–∞—Ж—Ц—П –Ї–∞–њ—Б–Њ–Љ–µ—А—Ц–≤ –њ—А–Є–Ј–≤–Њ–і–Є—В—М –і–Њ —Г—В–≤–Њ—А–µ–љ–љ—П –њ–∞–ї–Є—З–Ї–Њ–њ–Њ–і—Ц–±–љ–Є—Е —Ц –љ–Є—В–Ї–Њ–њ–Њ–і—Ц–±–љ–Є—Е –≤—Ц—А—Ц–Њ–љ—Ц–≤: –≤–Њ–љ–Є –Љ–Њ–ґ—Г—В—М –±—Г—В–Є –Ї–Њ—А–Њ—В–Ї–Є–Љ–Є —Ц –і—Г–ґ–µ –ґ–Њ—А—Б—В–Ї–Є–Љ–Є –∞–±–Њ –і–Њ–≤–≥–Є–Љ–Є —Ц –і—Г–ґ–µ –≥–љ—Г—З–Ї–Є–Љ–Є. –У–µ–љ–µ—В–Є—З–љ–Є–є –Љ–∞—В–µ—А—Ц–∞–ї, –Ј–∞–Ј–≤–Є—З–∞–є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Њ—О –†–Э–Ъ (—З–∞—Б–Њ–Љ –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Њ—О –Ф–Э–Ъ), —Г—В—А–Є–Љ—Г—Ф—В—М—Б—П –≤ –±—Ц–ї–Ї–Њ–≤—Ц–є —Б–њ—Ц—А–∞–ї—Ц —Ц–Њ–љ–љ–Є–Љ–Є –≤–Ј–∞—Ф–Љ–Њ–і—Ц—П–Љ–Є –Љ—Ц–ґ –љ–µ–≥–∞—В–Є–≤–љ–Є–Љ–Є –Ј–∞—А—П–і–∞–Љ–Є –љ–∞ –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Є—Е –Ї–Є—Б–ї–Њ—В–∞—Е —Ц –њ–Њ–Ј–Є—В–Є–≤–љ–Є–Љ–Є –Ј–∞—А—П–і–∞–Љ–Є –љ–∞ –±—Ц–ї–Ї–∞—Е. –Ч–∞–≥–∞–ї–Њ–Љ, –і–Њ–≤–ґ–Є–љ–∞ —Б–њ—Ц—А–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–њ—Б–Є–і—Г –Ј–∞–ї–µ–ґ–Є—В—М –≤—Ц–і –і–Њ–≤–ґ–Є–љ–Є –Њ—В–Њ—З–µ–љ–Њ—Ч –љ–Є–Љ –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є, –∞ –і—Ц–∞–Љ–µ—В—А –≤–Є–Ј–љ–∞—З–∞—Ф—В—М—Б—П —А–Њ–Ј–Љ—Ц—А–Њ–Љ —Ц —А–Њ–Ј—В–∞—И—Г–≤–∞–љ–љ—П–Љ –Ї–∞–њ—Б–Њ–Љ–µ—А—Ц–≤. –Я—А–Є–Ї–ї–∞–і–Њ–Љ —Б–њ—Ц—А–∞–ї—М–љ–Њ–≥–Њ –≤—Ц—А—Г—Б—Г —Ф –≤—Ц—А—Г—Б —В—О—В—О–љ–Њ–≤–Њ—Ч –Љ–Њ–Ј–∞—Ч–Ї–Є.
–Т—Ц—А—Г—Б –Ј –Ї–∞–њ—Б–Њ–Љ–µ—А–Њ–Љ —В–Є–њ—Г –≥–µ–Ї—Б–Њ–љ. –¶—П —Ц–ї—О—Б—В—А–∞—Ж—Ц—П –њ–Њ–Ї–∞–Ј—Г—Ф, —Й–Њ –≤—Ц—А—Г—Б–љ–Є–є –Ї–∞–њ—Б–Є–і –Љ–Њ–ґ–µ —Б–Ї–ї–∞–і–∞—В–Є—Б—М –Ј —З–Є—Б–ї–µ–љ–љ–Є—Е –Ї–Њ–њ—Ц–є –≤—Б—М–Њ–≥–Њ –ї–Є—И–µ –і–≤–Њ—Е –±—Ц–ї–Ї—Ц–≤
–С—Ц–ї—М—И—Ц—Б—В—М –≤—Ц—А—Г—Б—Ц–≤ —В–≤–∞—А–Є–љ –Љ–∞—О—В—М —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ—Г –∞–±–Њ –Љ–∞–є–ґ–µ –Ї—Г–ї—П—Б—В—Г —Д–Њ—А–Љ—Г –Ј —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ–Њ—О —Б–Є–Љ–µ—В—А—Ц—Ф—О . –Я—А–∞–≤–Є–ї—М–љ–Є–є —Ц–Ї–Њ—Б–∞–µ–і—А —Ф –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ—О —Д–Њ—А–Љ–Њ—О –і–ї—П –Ј–∞–Ї—А–Є—В–Њ–≥–Њ –Ї–∞–њ—Б–Є–і—Г, —Б–Ї–ї–∞–і–µ–љ–Њ–≥–Њ –Ј –Њ–і–љ–∞–Ї–Њ–≤–Є—Е —Б—Г–±–Њ–і–Є–љ–Є—Ж—М. –Ь—Ц–љ—Ц–Љ–∞–ї—М–љ–Њ –љ–µ–Њ–±—Е—Ц–і–љ–∞ –Ї—Ц–ї—М–Ї—Ц—Б—В—М –Њ–і–љ–∞–Ї–Њ–≤–Є—Е –Ї–∞–њ—Б–Њ–Љ–µ—А—Ц–≤ вАФ 12, –Ї–Њ–ґ–µ–љ –Ї–∞–њ—Б–Њ–Љ–µ—А —Б–Ї–ї–∞–і–∞—Ф—В—М—Б—П –Ј –њ'—П—В–Є —Ц–і–µ–љ—В–Є—З–љ–Є—Е —Б—Г–±–Њ–і–Є–љ–Є—Ж—М. –С–∞–≥–∞—В–Њ –≤—Ц—А—Г—Б—Ц–≤, —П–Ї-–Њ—В —А–Њ—В–∞–≤—Ц—А—Г—Б , –Љ–∞—О—В—М –њ–Њ–љ–∞–і –і–≤–∞–љ–∞–і—Ж—П—В—М –Ї–∞–њ—Б–Њ–Љ–µ—А—Ц–≤ —Ц –≤–Є–≥–ї—П–і–∞—О—В—М –Ї—А—Г–≥–ї–Є–Љ–Є, –∞–ї–µ –Ј–±–µ—А—Ц–≥–∞—О—В—М —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ—Г —Б–Є–Љ–µ—В—А—Ц—О. –Ъ–∞–њ—Б–Њ–Љ–µ—А–Є, —Й–Њ –ї–µ–ґ–∞—В—М —Г –≤–µ—А—И–Є–љ–∞—Е, –Њ—В–Њ—З–µ–љ—Ц –њ'—П—В—М–Љ–∞ —Ц–љ—И–Є–Љ–Є –Ї–∞–њ—Б–Њ–Љ–µ—А–∞–Љ–Є —Ц –љ–∞–Ј–Є–≤–∞—О—В—М—Б—П –њ–µ–љ—В–Њ–љ–∞–Љ–Є . –Ъ–∞–њ—Б–Њ–Љ–µ—А–Є —В—А–Є–Ї—Г—В–љ–Є—Е –≥—А–∞–љ–µ–є –Љ–∞—О—В—М 6 —Б—Г—Б—Ц–і—Ц–≤-–Ї–∞–њ—Б–Њ–Љ–µ—А—Ц–≤ —Ц –љ–∞–Ј–Є–≤–∞—О—В—М—Б—П –≥–µ–Ї—Б–Њ–љ–∞–Љ–Є . –У–µ–Ї—Б–Њ–љ–Є, –њ–Њ —Б—Г—В—Ц, —Ф –њ–ї–Њ—Б–Ї–Є–Љ–Є, –∞ –њ–µ–љ—В–Њ–љ–Є, —Й–Њ —Г—В–≤–Њ—А—О—О—В—М 12 –≤–µ—А—И–Є–љ, вАФ –ї–∞–Љ–∞–љ–Є–Љ–Є. –Ю–і–Є–љ —Ц —В–Њ–є —Б–∞–Љ–Є–є –±—Ц–ї–Њ–Ї –Љ–Њ–ґ–µ –±—Г—В–Є —Б—Г–±–Њ–і–Є–љ–Є—Ж–µ—О —Ц –њ–µ–љ—В–Њ–Љ–µ—А—Ц–≤, —Ц –≥–µ–Ї—Б–∞–Љ–µ—А—Ц–≤, –∞–±–Њ –ґ –≤–Њ–љ–Є –Љ–Њ–ґ—Г—В—М —Б–Ї–ї–∞–і–∞—В–Є—Б—П –Ј —А—Ц–Ј–љ–Є—Е –±—Ц–ї–Ї—Ц–≤.
–Ф–Њ–≤–≥–∞—Б—В–Є–Љ–Є –љ–∞–Ј–Є–≤–∞—О—В—М —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ—Ц –Ї–∞–њ—Б–Є–і–Є, –≤–Є—В—П–≥–љ—Г—В—Ц –≤–Ј–і–Њ–≤–ґ –Њ—Б—Ц —Б–Є–Љ–µ—В—А—Ц—Ч –њ'—П—В–Њ–≥–Њ –њ–Њ—А—П–і–Ї—Г. –Ґ–∞–Ї–∞ —Д–Њ—А–Љ–∞ —Е–∞—А–∞–Ї—В–µ—А–љ–∞ –і–ї—П –≥–Њ–ї–Њ–≤–Њ–Ї –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥—Ц–≤ [ 73]
–§–Њ—А–Љ–∞ —Ж–Є—Е –Ї–∞–њ—Б–Є–і—Ц–≤ –љ—Ц —Б—Г—В–Њ —Б–њ—Ц—А–∞–ї—М–љ–∞, –љ—Ц —Б—Г—В–Њ —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ–∞. –Т–Њ–љ–Є –Љ–Њ–ґ—Г—В—М –љ–µ—Б—В–Є –і–Њ–і–∞—В–Ї–Њ–≤—Ц –Ј–Њ–≤–љ—Ц—И–љ—Ц —Б—В—А—Г–Ї—В—Г—А–Є, –њ—А–Є–Љ—Ц—А–Њ–Љ, –±—Ц–ї–Ї–Њ–≤—Ц —Е–≤–Њ—Б—В–Є –∞–±–Њ —Б–Ї–ї–∞–і–љ—Ц –Ј–Њ–≤–љ—Ц—И–љ—Ц —Б—В—Ц–љ–Ї–Є. –Ф–µ—П–Ї—Ц –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥–Є, —П–Ї-–Њ—В —Д–∞–≥ –Ґ4 , –Љ–∞—О—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Є–є –Ї–∞–њ—Б–Є–і, —Й–Њ —Б–Ї–ї–∞–і–∞—Ф—В—М—Б—П –Ј —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ–Њ—Ч –≥–Њ–ї–Њ–≤–Ї–Є, –Ј'—Ф–і–љ–∞–љ–Њ—Ч –Ј—Ц —Б–њ—Ц—А–∞–ї—М–љ–Є–Љ —Е–≤–Њ—Б—В–Њ–Љ, —П–Ї–Є–є –Љ–Њ–ґ–µ –Љ–∞—В–Є —И–µ—Б—В–Є–≥—А–∞–љ–љ—Г –Њ—Б–љ–Њ–≤—Г –Ј —Е–≤–Њ—Б—В–Њ–≤–Є–Љ–Є –±—Ц–ї–Ї–Њ–≤–Є–Љ–Є –љ–Є—В–Ї–∞–Љ–Є, —Й–Њ –≤—Ц–і—Е–Њ–і—П—В—М –≤—Ц–і –љ–µ—Ч. –¶–µ–є —Е–≤—Ц—Б—В –і—Ц—Ф –љ–∞ –Ј—А–∞–Ј–Њ–Ї –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–≥–Њ —И–њ—А–Є—Ж–∞, –њ—А–Є–Ї—А—Ц–њ–ї—О—О—З–Є—Б—М –і–Њ –Ї–ї—Ц—В–Є–љ–Є-–≥–Њ—Б–њ–Њ–і–∞—А—П —Ц –њ–Њ—В—Ц–Љ –≤–њ–Њ—А—Б–Ї—Г—О—З–Є –≤ –љ–µ—Ч –≥–µ–љ–µ—В–Є—З–љ–Є–є –Љ–∞—В–µ—А—Ц–∞–ї –≤—Ц—А—Г—Б—Г[ 74]
–Т—Ц—А—Г—Б –≥–µ—А–њ–µ—Б—Г , –Њ—В–Њ—З–µ–љ–Є–є –ї—Ц–њ—Ц–і–љ–Њ—О –Њ–±–Њ–ї–Њ–љ–Ї–Њ—О (—Б—Г–њ–µ—А–Ї–∞–њ—Б–Є–і–Њ–Љ)
–Ф–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є –Њ—В–Њ—З—Г—О—В—М —Б–µ–±–µ –і–Њ–і–∞—В–Ї–Њ–≤–Њ—О –Њ–±–Њ–ї–Њ–љ–Ї–Њ—О –Ј –Љ–Њ–і–Є—Д—Ц–Ї–Њ–≤–∞–љ–Њ—Ч –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч –Љ–µ–Љ–±—А–∞–љ–Є (–њ–ї–∞–Ј–Љ–∞—В–Є—З–љ–Њ—Ч –∞–±–Њ –≤–љ—Г—В—А—Ц—И–љ—М–Њ—Ч, —П–Ї-–Њ—В —П–і–µ—А–љ–∞ –Љ–µ–Љ–±—А–∞–љ–∞ –∞–±–Њ –Љ–µ–Љ–±—А–∞–љ–∞ –µ–љ–і–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–љ–Њ–≥–Њ —А–µ—В–Є–Ї—Г–ї—Г–Љ—Г ). –¶–µ–є –і–Њ–і–∞—В–Ї–Њ–≤–Є–є –±—Ц–ї—Ц–њ—Ц–і–љ–Є–є —И–∞—А –љ–∞–Ј–Є–≤–∞—Ф—В—М—Б—П —Б—Г–њ–µ—А–Ї–∞–њ—Б–Є–і–Њ–Љ . –£ –ї—Ц–њ—Ц–і–љ—Ц–є –Њ–±–Њ–ї–Њ–љ—Ж—Ц –≤—Ц—А—Г—Б—Г —В–∞–Ї–Њ–ґ –Ј–љ–∞—Е–Њ–і—П—В—М—Б—П –±—Ц–ї–Ї–Є, –Ј–∞–Ї–Њ–і–Њ–≤–∞–љ—Ц –≤ –≤—Ц—А—Г—Б–љ–Њ–Љ—Г –≥–µ–љ–Њ–Љ—Ц —В–∞/—З–Є –≥–µ–љ–Њ–Љ—Ц —Е–∞–Ј—П—Ч–љ–∞. –°–∞–Љ–∞ –ґ –Љ–µ–Љ–±—А–∞–љ–∞, –∞ —В–∞–Ї–Њ–ґ –±—Г–і—М-—П–Ї—Ц —Ч—Ч –≤—Г–≥–ї–µ–≤–Њ–і–љ—Ц –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Є –њ–Њ—Е–Њ–і—П—В—М –≤–Є–љ—П—В–Ї–Њ–≤–Њ –≤—Ц–і –Ї–ї—Ц—В–Є–љ–Є-—Е–∞–Ј—П—Ч–љ–∞. –Ґ–∞–Ї–Є–Љ —З–Є–љ–Њ–Љ —Д–Њ—А–Љ—Г—О—В—М —Б–≤–Њ—О –Њ–±–Њ–ї–Њ–љ–Ї—Г –≤—Ц—А—Г—Б –≥—А–Є–њ—Г —Ц –Т–Ж–Ы . –Ж–љ—Д–µ–Ї—Ж—Ц–є–љ—Ц—Б—В—М –±—Ц–ї—М—И–Њ—Б—В—Ц –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –Љ–∞—О—В—М –Њ–±–Њ–ї–Њ–љ–Ї—Г, –Ј–∞–ї–µ–ґ–Є—В—М —Б–∞–Љ–µ –≤—Ц–і —Ж—Ц—Ф—Ч –Њ–±–Њ–ї–Њ–љ–Ї–Є.
–Ф–Њ –≤—Ц—А—Г—Б—Ц–≤ –Ј —Б—Г–њ–µ—А–Ї–∞–њ—Б–Є–і–Њ–Љ –љ–∞–ї–µ–ґ–∞—В—М –њ–Њ–Ї—Б–≤—Ц—А—Г—Б–Є, –Љ—Ц–Љ—Ц–≤—Ц—А—Г—Б–Є, –Љ–µ–≥–∞–≤—Ц—А—Г—Б —В–Њ—Й–Њ. –Я–Њ–Ї—Б–≤—Ц—А—Г—Б–Є вАФ —Ж–µ –≤–µ–ї–Є–Ї—Ц —Б–Ї–ї–∞–і–љ–Њ–Њ—А–≥–∞–љ—Ц–Ј–Њ–≤–∞–љ—Ц –≤—Ц—А—Г—Б–Є –Ј –љ–µ–Ј–≤–Є—З–∞–є–љ–Њ—О –Љ–Њ—А—Д–Њ–ї–Њ–≥—Ц—Ф—О. –Т—Б–µ—А–µ–і–Є–љ—Ц –≤—Ц—А—Ц–Њ–љ–∞ –Ј–љ–∞—Е–Њ–і–Є—В—М—Б—П –Ј–≤'—П–Ј–∞–љ–∞ –Ј –±—Ц–ї–Ї–∞–Љ–Є –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–∞ –Љ–Њ–ї–µ–Ї—Г–ї–∞ –Ф–Э–Ъ —Г –≤–Є–≥–ї—П–і—Ц –і–Є—Б–Ї–Њ–њ–Њ–і—Ц–±–љ–Њ—Ч —Б—В—А—Г–Ї—В—Г—А–Є вАФ –љ—Г–Ї–ї–µ–Њ—Ч–і–∞. –Э—Г–Ї–ї–µ–Њ—Ч–і –Њ—В–Њ—З–µ–љ–Є–є –ї—Ц–њ—Ц–і–љ–Њ—О –Љ–µ–Љ–±—А–∞–љ–Њ—О —В–∞ –і–≤–Њ–Љ–∞ –±–Њ–Ї–Њ–≤–Є–Љ–Є —В—Ц–ї—М—Ж—П–Љ–Є –љ–µ–≤—Ц–і–Њ–Љ–Њ—Ч —Д—Г–љ–Ї—Ж—Ц—Ч. –Т—Ц—А—Г—Б –Љ–∞—Ф —Б—Г–њ–µ—А–Ї–∞–њ—Б–Є–і –Ј –≤–µ–ї–Є–Ї–Њ—О –Ї—Ц–ї—М–Ї—Ц—Б—В—О –±—Ц–ї–Ї—Ц–≤ –љ–∞ –є–Њ–≥–Њ –њ–Њ–≤–µ—А—Е–љ—Ц. –Т–µ—Б—М –≤—Ц—А—Ц–Њ–љ –Ј–ї–µ–≥–Ї–∞ –њ–ї–µ–є–Њ–Љ–Њ—А—Д–љ–Є–є (—В–Њ–±—В–Њ –Ј–і–∞—В–љ–Є–є –Ј–Љ—Ц–љ—О–≤–∞—В–Є —Д–Њ—А–Љ—Г —Ц —А–Њ–Ј–Љ—Ц—А –Ј–∞–ї–µ–ґ–љ–Њ –≤—Ц–і —Г–Љ–Њ–≤) —Ц –Љ–Њ–ґ–µ –љ–∞–±—Г–≤–∞—В–Є —Д–Њ—А–Љ–Є –≤—Ц–і –Њ–≤–∞–ї—М–љ–Њ—Ч –і–Њ –±–ї–Њ–Ї–Њ–њ–Њ–і—Ц–±–љ–Њ—Ч[ 76] –Ь—Ц–Љ—Ц–≤—Ц—А—Г—Б —Ф –Њ–і–љ–Є–Љ –Ј –љ–∞–є–±—Ц–ї—М—И–Є—Е –Њ–њ–Є—Б–∞–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Ц –Љ–∞—Ф —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ–Є–є –Ї–∞–њ—Б–Є–і –і—Ц–∞–Љ–µ—В—А–Њ–Љ 400вАФ500 –љ–Љ. –С—Ц–ї–Ї–Њ–≤—Ц —Д—Ц–ї–∞–Љ–µ–љ—В–Є, —Й–Њ –≤—Ц–і—Е–Њ–і—П—В—М –≤—Ц–і –њ–Њ–≤–µ—А—Е–љ—Ц –≤—Ц—А—Ц–Њ–љ–∞, —Б—П–≥–∞—О—В—М 100 –љ–Љ –Ј–∞–≤–і–Њ–≤–ґ–Ї–Є[ 77] [ 78] –Њ–Ї–µ–∞–љ—Ц—З–љ–Њ–Љ—Г –і–љ—Ц –њ–Њ–±–ї–Є–Ј—Г —Г–Ј–±–µ—А–µ–ґ–ґ—П –І–Є–ї—Ц . –Т—Ц—А—Г—Б, —П–Ї–Њ–Љ—Г –і–∞–ї–Є —В–Є–Љ—З–∞—Б–Њ–≤—Г –љ–∞–Ј–≤—Г Megavirus chilensis –Њ–њ—В–Є—З–љ–Є–є –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ [ 79]
–У–µ–љ–µ—В–Є—З–љ–∞ —А—Ц–Ј–љ–Њ–Љ–∞–љ—Ц—В–љ—Ц—Б—В—М —Г –≤—Ц—А—Г—Б—Ц–≤
–Т–ї–∞—Б—В–Є–≤–Њ—Б—В—Ц
–Я–∞—А–∞–Љ–µ—В—А–Є
–Э—Г–Ї–ї–µ—Ч–љ–Њ–≤–∞ –Ї–Є—Б–ї–Њ—В–∞
–Ф–Э–Ъ
–†–Э–Ъ
–Ж –Ф–Э–Ъ, —Ц –†–Э–Ъ (–љ–∞ —А—Ц–Ј–љ–Є—Е —Б—В–∞–і—Ц—П—Е –ґ–Є—В—В—Ф–≤–Њ–≥–Њ —Ж–Є–Ї–ї—Г)
–§–Њ—А–Љ–∞
–Ы—Ц–љ—Ц–є–љ–∞
–Ъ—Ц–ї—М—Ж–µ–≤–∞
–°–µ–≥–Љ–µ–љ—В–Њ–≤–∞–љ–∞
–Ъ—Ц–ї—М–Ї—Ц—Б—В—М –ї–∞–љ—Ж—О–≥—Ц–≤
–Ю–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Ц
–Ф–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Ц
–Ф–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Ц –Ј –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є–Љ–Є —Д—А–∞–≥–Љ–µ–љ—В–∞–Љ–Є
–Я–Њ–ї—П—А–љ—Ц—Б—В—М
–Я–Њ–Ј–Є—В–Є–≤–љ–∞ –њ–Њ–ї—П—А–љ—Ц—Б—В—М (+)
–Э–µ–≥–∞—В–Є–≤–љ–∞ –њ–Њ–ї—П—А–љ—Ц—Б—В—М (вИТ)
–Я–Њ–і–≤—Ц–є–љ–∞ –њ–Њ–ї—П—А–љ—Ц—Б—В—М (+/вИТ)
–У–µ–љ–µ—В–Є—З–љ–∞ —А–µ–Ї–Њ–Љ–±—Ц–љ–∞—Ж—Ц—П –Љ–Њ–ґ–µ —Б–њ—А–Є—З–Є–љ–Є—В–Є –њ–Њ—П–≤—Г –љ–Њ–≤–Њ–≥–Њ –≤–Є—Б–Њ–Ї–Њ–њ–∞—В–Њ–≥–µ–љ–љ–Њ–≥–Њ —И—В–∞–Љ—Г –ї—О–і—Б—М–Ї–Њ–≥–Њ –≥—А–Є–њ—Г –Т—Ц—А—Г—Б–Є –њ–Њ–Ї–∞–Ј—Г—О—В—М –≤–µ–ї–Є—З–µ–Ј–љ—Г –Ї—Ц–ї—М–Ї—Ц—Б—В—М –≤–∞—А—Ц–∞–љ—В—Ц–≤ –Њ—А–≥–∞–љ—Ц–Ј–∞—Ж—Ц—Ч –≥–µ–љ–Њ–Љ—Г ; –≤ —Ж—М–Њ–Љ—Г —Б–µ–љ—Б—Ц –≤–Њ–љ–Є —А—Ц–Ј–љ–Њ–Љ–∞–љ—Ц—В–љ—Ц—И—Ц, –љ—Ц–ґ —А–Њ—Б–ї–Є–љ–Є, —В–≤–∞—А–Є–љ–Є, –∞—А—Е–µ—Ч —В–∞ –±–∞–Ї—В–µ—А—Ц—Ч. –Ж—Б–љ—Г—О—В—М –Љ—Ц–ї—М–є–Њ–љ–Є —А—Ц–Ј–љ–Є—Е —В–Є–њ—Ц–≤ –≤—Ц—А—Г—Б—Ц–≤[ 4] –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥–Є , —П–Ї –њ—А–∞–≤–Є–ї–Њ, –Љ–∞—О—В—М –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Ц –Ф–Э–Ъ.
–Т—Ц—А—Г—Б–љ–Є–є –≥–µ–љ–Њ–Љ –±—Г–≤–∞—Ф –Ї—Ц–ї—М—Ж–µ–≤–Є–Љ, —П–Ї —Г –њ–Њ–ї—Ц–Њ–Љ–∞–≤—Ц—А—Г—Б—Ц–≤ , –∞–±–Њ –ї—Ц–љ—Ц–є–љ–Є–Љ, —П–Ї —Г –∞–і–µ–љ–Њ–≤—Ц—А—Г—Б—Ц–≤ . –§–Њ—А–Љ–∞ –≥–µ–љ–Њ–Љ—Г –љ–µ –Ј–∞–ї–µ–ґ–Є—В—М –≤—Ц–і —В–Є–њ—Г –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є. –£ –±–∞–≥–∞—В—М–Њ—Е –†–Э–Ъ-–≤–Љ—Ц—Б–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Ц –і–µ—П–Ї–Є—Е –Ф–Э–Ъ-–≤–Љ—Ц—Б–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –≥–µ–љ–Њ–Љ —З–∞—Б—В–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –і–µ–Ї—Ц–ї—М–Ї–Њ–Љ–∞ –Њ–Ї—А–µ–Љ–Є–Љ–Є –Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є –≤ –Ї–Њ–ґ–љ–Њ–Љ—Г –≤—Ц—А—Ц–Њ–љ—Ц, —Г –Ј–≤'—П–Ј–Ї—Г –Ј —З–Є–Љ –є–Њ–≥–Њ –љ–∞–Ј–Є–≤–∞—О—В—М —Б–µ–≥–Љ–µ–љ—В–Њ–≤–∞–љ–Є–Љ. –£ –†–Э–Ъ-–≤–Љ—Ц—Б–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –Ї–Њ–ґ–µ–љ —Б–µ–≥–Љ–µ–љ—В (–Љ–Њ–ї–µ–Ї—Г–ї–∞) —З–∞—Б—В–Њ –Ї–Њ–і—Г—Ф —В—Ц–ї—М–Ї–Є –Њ–і–Є–љ –±—Ц–ї–Њ–Ї, —Ц –Ј–∞–Ј–≤–Є—З–∞–є —Ж—Ц —Б–µ–≥–Љ–µ–љ—В–Є —Г–њ–∞–Ї–Њ–≤—Г—О—В—М—Б—П –≤ –Њ–і–Є–љ –Ї–∞–њ—Б–Є–і. –Я—А–Њ—В–µ –љ–∞—П–≤–љ—Ц—Б—В—М —Г—Б—Ц—Е —Б–µ–≥–Љ–µ–љ—В—Ц–≤ –љ–µ –Ј–∞–≤–ґ–і–Є –Њ–±–Њ–≤'—П–Ј–Ї–Њ–≤–∞ –і–ї—П —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Њ—Б—В—Ц –≤—Ц—А—Г—Б—Г, —П–Ї —Ж–µ –і–µ–Љ–Њ–љ—Б—В—А—Г—О—В—М –≤—Ц—А—Г—Б –Љ–Њ–Ј–∞—Ч–Ї–Є —Б—В–Њ–Ї–Њ–ї–Њ—Б–∞ [en]
–Т—Ц—А—Г—Б–љ—Ц –≥–µ–љ–Њ–Љ–Є –љ–µ–Ј–∞–ї–µ–ґ–љ–Њ –≤—Ц–і —В–Є–њ—Г –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є –Љ–∞–є–ґ–µ –Ј–∞–≤–ґ–і–Є –±—Г–≤–∞—О—В—М –∞–±–Њ –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є–Љ–Є, –∞–±–Њ –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є–Љ–Є. –Ф–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є–є –≥–µ–љ–Њ–Љ –≤–Ї–ї—О—З–∞—Ф –њ–∞—А—Г –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞—А–љ–Є—Е –ї–∞–љ—Ж—О–≥—Ц–≤ –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є, –∞ –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є–є вАФ –ї–Є—И–µ –Њ–і–Є–љ –ї–∞–љ—Ж—О–≥. –У–µ–љ–Њ–Љ –≤—Ц—А—Г—Б—Ц–≤ –і–µ—П–Ї–Є—Е —А–Њ–і–Є–љ (–љ–∞–њ—А–Є–Ї–ї–∞–і, –≥–µ–њ–∞–і–љ–∞–≤—Ц—А—Г—Б–Є
–Ф–ї—П –±—Ц–ї—М—И–Њ—Б—В—Ц –†–Э–Ъ-–≤–Љ—Ц—Б–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Ц –і–µ—П–Ї–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –Ј –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Њ—Ч –Ф–Э–Ъ –≤–Є–Ј–љ–∞—З–∞—О—В—М –њ–Њ–ї—П—А–љ—Ц—Б—В—М –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є –Ј–∞–ї–µ–ґ–љ–Њ –≤—Ц–і —В–Њ–≥–Њ, —З–Є –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞—А–љ–∞ –≤–Њ–љ–∞ –≤—Ц—А—Г—Б–љ—Ц–є –Љ–†–Э–Ъ . –Ь–Њ–ї–µ–Ї—Г–ї–∞ –†–Э–Ъ –Ј –њ–Њ–Ј–Є—В–Є–≤–љ–Њ—О –њ–Њ–ї—П—А–љ—Ц—Б—В—О (–њ–ї—О—Б-–ї–∞–љ—Ж—О–≥) –Љ–∞—Ф —В—Г –ґ –њ–Њ—Б–ї—Ц–і–Њ–≤–љ—Ц—Б—В—М –љ—Г–Ї–ї–µ–Њ—В–Є–і—Ц–≤ , —Й–Њ –є –Љ–†–Э–Ъ, —З–µ—А–µ–Ј —В–µ, –њ—А–Є–љ–∞–є–Љ–љ—Ц, —П–Ї–∞—Б—М —Ч—Ч —З–∞—Б—В–Є–љ–∞ –Љ–Њ–ґ–µ –Њ–і—А–∞–Ј—Г –ґ –њ–Њ—З–∞—В–Є —В—А–∞–љ—Б–ї—О–≤–∞—В–Є—Б—П –Ї–ї—Ц—В–Є–љ–Њ—О-–≥–Њ—Б–њ–Њ–і–∞—А–µ–Љ. –†–Э–Ъ –Ј –љ–µ–≥–∞—В–Є–≤–љ–Њ—О –њ–Њ–ї—П—А–љ—Ц—Б—В—О (–Љ—Ц–љ—Г—Б-–ї–∞–љ—Ж—О–≥) –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞—А–љ–∞ –Љ–†–Э–Ъ, —В–Њ–Љ—Г –і–Њ –њ–Њ—З–∞—В–Ї—Г —В—А–∞–љ—Б–ї—П—Ж—Ц—Ч –љ–∞ –љ—Ц–є –Љ–∞—Ф –±—Г—В–Є —Б–Є–љ—В–µ–Ј–Њ–≤–∞–љ–∞ –њ–Њ–Ј–Є—В–Є–≤–љ–∞ –†–Э–Ъ –Ј–∞ –і–Њ–њ–Њ–Љ–Њ–≥–Њ—О —Д–µ—А–Љ–µ–љ—В—Г –†–Э–Ъ-–Ј–∞–ї–µ–ґ–љ–Њ—Ч-–†–Э–Ъ-–њ–Њ–ї—Ц–Љ–µ—А–∞–Ј–Є . –Э–∞–Ј–≤–Є –ї–∞–љ—Ж—О–≥—Ц–≤ –Ф–Э–Ъ –і–ї—П –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –Љ—Ц—Б—В—П—В—М –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –Ф–Э–Ъ, –њ–Њ–і—Ц–±–љ—Ц –і–Њ –љ–∞–Ј–≤ –ї–∞–љ—Ж—О–≥—Ц–≤ –і–ї—П –†–Э–Ъ: –ї–∞–љ—Ж—О–≥, —Й–Њ –Ї–Њ–і—Г—Ф, –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞—А–љ–Є–є –Љ–†–Э–Ъ (-), –∞ —В–Њ–є, —Й–Њ –љ–µ –Ї–Њ–і—Г—Ф, —Ф —Ч—Ч –Ї–Њ–њ—Ц—Ф—О (+). –Ю–і–љ–∞–Ї –≥–µ–љ–Њ–Љ–Є –і–µ–Ї—Ц–ї—М–Ї–Њ—Е —В–Є–њ—Ц–≤ –Ф–Э–Ъ вАФ —Ц –†–Э–Ъ-–≤–Љ—Ц—Б–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Ц –Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є, —Й–Њ –Љ–∞—О—В—М —А—Ц–Ј–љ—Г –њ–Њ–ї—П—А–љ—Ц—Б—В—М, —В–Њ–±—В–Њ —В—А–∞–љ—Б–Ї—А–Є–њ—Ж—Ц—Ч –Љ–Њ–ґ–µ –њ—Ц–і–ї—П–≥–∞—В–Є –±—Г–і—М-—П–Ї–Є–є –ї–∞–љ—Ж—О–≥. –¶–µ —Б—В–Њ—Б—Г—Ф—В—М—Б—П, –љ–∞–њ—А–Є–Ї–ї–∞–і, –≥–µ–Љ—Ц–љ—Ц–≤—Ц—А—Г—Б—Ц–≤ [en] –∞—А–µ–љ–∞–≤—Ц—А—Г—Б—Ц–≤ [en] [ 81]
–†–Њ–Ј–Љ—Ц—А –≥–µ–љ–Њ–Љ—Г —И–Є—А–Њ–Ї–Њ —А—Ц–Ј–љ–Є—В—М—Б—П –≤ —А—Ц–Ј–љ–Є—Е –≤–Є–і—Ц–≤. –Э–∞–є–Љ–µ–љ—И–Є–є –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є–є –Ф–Э–Ъ-–≥–µ–љ–Њ–Љ –Љ–∞—Ф –≤—Ц—А—Г—Б –Ј —А–Њ–і–Є–љ–Є —Ж–Є—А–Ї–Њ–≤—Ц—А—Г—Б—Ц–≤ [en] –Љ—Ц–Љ—Ц–≤—Ц—А—Г—Б—Г : –≤—Ц–љ –Љ—Ц—Б—В–Є—В—М –њ–Њ–љ–∞–і 1,2 –Љ–ї–љ –њ–∞—А –Њ—Б–љ–Њ–≤ —Ц –Ї–Њ–і—Г—Ф –њ–Њ–љ–∞–і —В–Є—Б—П—З—Г –±—Ц–ї–Ї—Ц–≤[ 82] —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—Ч [ 83] [ 84] –Љ—Г—В–∞—Ж—Ц–є –≤ —Ч—Е–љ—Ц—Е –≥–µ–љ–Њ–Љ–∞—Е –љ–∞–±–ї–Є–ґ–∞—Ф—В—М—Б—П –і–Њ —И–≤–Є–і–Ї–Њ—Б—В—Ц –і–ї—П –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –Љ—Ц—Б—В—П—В—М –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Ц –†–Э–Ъ[ 85]
–У–µ–љ–µ—В–Є—З–љ—Ц –Ј–Љ—Ц–љ–Є –≤—Ц–і–±—Г–≤–∞—О—В—М—Б—П —Г –≤—Ц—А—Г—Б—Ц–≤ –Ј–∞ —А—Ц–Ј–љ–Є–Љ–Є –Љ–µ—Е–∞–љ—Ц–Ј–Љ–∞–Љ–Є. –Ф–Њ –љ–Є—Е –љ–∞–ї–µ–ґ–∞—В—М –≤–Є–њ–∞–і–Ї–Њ–≤—Ц –Ј–∞–Љ—Ц–љ–Є –Њ–Ї—А–µ–Љ–Є—Е –Њ—Б–љ–Њ–≤ —Г –†–Э–Ъ –∞–±–Њ –Ф–Э–Ъ. –£ –±—Ц–ї—М—И–Њ—Б—В—Ц –≤–Є–њ–∞–і–Ї—Ц–≤ —Ж—Ц —В–Њ—З–Ї–Њ–≤—Ц –Љ—Г—В–∞—Ж—Ц—Ч [en] –њ—А–Њ—В–Є–≤—Ц—А—Г—Б–љ–Є—Е –њ—А–µ–њ–∞—А–∞—В—Ц–≤ [ 86] –Ф—А–µ–є—Д –∞–љ—В–Є–≥–µ–љ—Ц–≤ –≤—Ц–і–±—Г–≤–∞—Ф—В—М—Б—П —В–Њ–і—Ц, –Ї–Њ–ї–Є –≥–µ–љ–Њ–Љ –≤—Ц—А—Г—Б—Г –Ј–∞–Ј–љ–∞—Ф –Ј–љ–∞—З–љ–Є—Е –Ј–Љ—Ц–љ. –¶–µ –Љ–Њ–ґ–µ –±—Г—В–Є –љ–∞—Б–ї—Ц–і–Ї–Њ–Љ —А–µ–Ї–Њ–Љ–±—Ц–љ–∞—Ж—Ц—Ч –∞–±–Њ —А–µ–∞—Б–Њ—А—В–Є–Љ–µ–љ—В—Г . –Ъ–Њ–ї–Є —Ж–µ —В—А–∞–њ–ї—П—Ф—В—М—Б—П –Ј –≤—Ц—А—Г—Б–Њ–Љ –≥—А–Є–њ—Г, –љ–∞—Б–ї—Ц–і–Ї–Њ–Љ –Љ–Њ–ґ–µ —Б—В–∞—В–Є –њ–∞–љ–і–µ–Љ—Ц—П [ 87] –Ї–≤–∞–Ј—Ц–≤–Є–і–Є [ru] –њ—А–Є—А–Њ–і–љ–Њ–≥–Њ –і–Њ–±–Њ—А—Г [ 88]
–°–µ–≥–Љ–µ–љ—В–Њ–≤–∞–љ–Є–є –≥–µ–љ–Њ–Љ –і–∞—Ф –µ–≤–Њ–ї—О—Ж—Ц–є–љ—Ц –њ–µ—А–µ–≤–∞–≥–Є: —А—Ц–Ј–љ—Ц —И—В–∞–Љ–Є –≤—Ц—А—Г—Б—Г –Ј —Б–µ–≥–Љ–µ–љ—В–Њ–≤–∞–љ–Є–Љ –≥–µ–љ–Њ–Љ–Њ–Љ –Љ–Њ–ґ—Г—В—М –Њ–±–Љ—Ц–љ—О–≤–∞—В–Є—Б—П –≥–µ–љ–∞–Љ–Є —Ц –≤–Є—А–Њ–±–ї—П—В–Є –љ–∞—Й–∞–і–Ї—Ц–≤ –Ј —Г–љ—Ц–Ї–∞–ї—М–љ–Є–Љ–Є –≤–ї–∞—Б—В–Є–≤–Њ—Б—В—П–Љ–Є. –¶–µ —П–≤–Є—Й–µ –љ–∞–Ј–Є–≤–∞—Ф—В—М—Б—П —А–µ–∞—Б–Њ—А—В–Є–Љ–µ–љ—В–Њ–Љ[ 89]
–У–µ–љ–µ—В–Є—З–љ–∞ —А–µ–Ї–Њ–Љ–±—Ц–љ–∞—Ж—Ц—П вАФ —Ж–µ –њ—А–Њ—Ж–µ—Б –≤–љ–µ—Б–µ–љ–љ—П —А–Њ–Ј—А–Є–≤—Г –≤ –Љ–Њ–ї–µ–Ї—Г–ї—Г –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є –Ј –љ–∞—Б—В—Г–њ–љ–Є–Љ ¬Ђ–Ј—И–Є–≤–∞–љ–љ—П–Љ¬ї —Ч—Ч –Ј —Ц–љ—И–Є–Љ–Є –Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є. –†–µ–Ї–Њ–Љ–±—Ц–љ–∞—Ж—Ц—П –Љ–Њ–ґ–µ –≤—Ц–і–±—Г–≤–∞—В–Є—Б—П –Љ—Ц–ґ –≥–µ–љ–Њ–Љ–∞–Љ–Є –і–≤–Њ—Е –≤—Ц—А—Г—Б—Ц–≤, –Ї–Њ–ї–Є –≤–Њ–љ–Є –Ј–∞—А–∞–ґ–∞—О—В—М –Ї–ї—Ц—В–Є–љ—Г –Њ–і–љ–Њ—З–∞—Б–љ–Њ. –Ф–Њ—Б–ї—Ц–і–ґ–µ–љ–љ—П –µ–≤–Њ–ї—О—Ж—Ц—Ч –≤—Ц—А—Г—Б—Ц–≤ –њ–Њ–Ї–∞–Ј–∞–ї–Є, —Й–Њ —Г –≤–Є–≤—З–µ–љ–Є—Е –≤–Є–і—Ц–≤ —А–µ–Ї–Њ–Љ–±—Ц–љ–∞—Ж—Ц—П –і–Њ—Б–Є—В—М –њ–Њ—И–Є—А–µ–љ–∞[ 90] [ 91] [ 92]
–Ґ–Є–њ–Њ–≤–Є–є –ґ–Є—В—В—Ф–≤–Є–є —Ж–Є–Ї–ї –≤—Ц—А—Г—Б—Г –љ–∞ –њ—А–Є–Ї–ї–∞–і—Ц –≤—Ц—А—Г—Б—Г –≥–µ–њ–∞—В–Є—В—Г C –Т—Ц—А—Г—Б–Є –љ–µ —А–Њ–Ј–Љ–љ–Њ–ґ—Г—О—В—М—Б—П –Ї–ї—Ц—В–Є–љ–љ–Є–Љ –њ–Њ–і—Ц–ї–Њ–Љ, –Њ—Б–Ї—Ц–ї—М–Ї–Є –љ–µ –Љ–∞—О—В—М –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч –±—Г–і–Њ–≤–Є. –Ч–∞–Љ—Ц—Б—В—М —Ж—М–Њ–≥–Њ –≤–Њ–љ–Є –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М —А–µ—Б—Г—А—Б–Є –Ї–ї—Ц—В–Є–љ–Є-—Е–∞–Ј—П—Ч–љ–∞ –і–ї—П —Г—В–≤–Њ—А–µ–љ–љ—П –Љ–љ–Њ–ґ–Є–љ–љ–Є—Е –Ї–Њ–њ—Ц–є —Б–∞–Љ–Є—Е —Б–µ–±–µ, —Ц —Ч—Е —Б–Ї–ї–∞–і–∞–љ–љ—П –≤—Ц–і–±—Г–≤–∞—Ф—В—М—Б—П –≤—Б–µ—А–µ–і–Є–љ—Ц –Ї–ї—Ц—В–Є–љ–Є.
–£–Љ–Њ–≤–љ–Њ –ґ–Є—В—В—Ф–≤–Є–є —Ж–Є–Ї–ї –≤—Ц—А—Г—Б—Г –Љ–Њ–ґ–љ–∞ —А–Њ–Ј–±–Є—В–Є –љ–∞ –Ї—Ц–ї—М–Ї–∞ –µ—В–∞–њ—Ц–≤, —Й–Њ –≤–Ј–∞—Ф–Љ–љ–Њ –њ–µ—А–µ–Ї—А–Є–≤–∞—О—В—М—Б—П (–Ј–∞–Ј–≤–Є—З–∞–є –≤–Є–і—Ц–ї—П—О—В—М 6 –µ—В–∞–њ—Ц–≤):
–Я—А–Є–Ї—А—Ц–њ–ї–µ–љ–љ—П вАФ —Ж–µ —Г—В–≤–Њ—А–µ–љ–љ—П —Б–њ–µ—Ж–Є—Д—Ц—З–љ–Њ–≥–Њ –Ј–≤'—П–Ј–Ї—Г –Љ—Ц–ґ –±—Ц–ї–Ї–∞–Љ–Є –≤—Ц—А—Г—Б–љ–Њ–≥–Њ –Ї–∞–њ—Б–Є–і—Г —Ц —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –љ–∞ –њ–Њ–≤–µ—А—Е–љ—Ц –Ї–ї—Ц—В–Є–љ–Є-—Е–∞–Ј—П—Ч–љ–∞. –¶–µ –Њ—Б–Њ–±–ї–Є–≤–µ –Ј–≤'—П–Ј—Г–≤–∞–љ–љ—П –≤–Є–Ј–љ–∞—З–∞—Ф –Ї–Њ–ї–Њ —Е–∞–Ј—П—Ч–љ—Ц–≤ –≤—Ц—А—Г—Б—Г. –Э–∞–њ—А–Є–Ї–ї–∞–і, –Т–Ж–Ы –≤—А–∞–ґ–∞—Ф —В—Ц–ї—М–Ї–Є –њ–µ–≤–љ–Є–є —В–Є–њ –ї—О–і—Б—М–Ї–Є—Е –ї–µ–є–Ї–Њ—Ж–Є—В—Ц–≤ . –¶–µ –њ–Њ–≤'—П–Ј–∞–љ–Њ –Ј —В–Є–Љ, —Й–Њ –Њ–±–Њ–ї–Њ–љ–Ї–Њ–≤–Є–є –≥–ї—Ц–Ї–Њ–њ—А–Њ—В–µ—Ч–љ –≤—Ц—А—Г—Б—Г gp120 —Б–њ–µ—Ж–Є—Д—Ц—З–љ–Њ –Ј–≤'—П–Ј—Г—Ф—В—М—Б—П –Ј –Љ–Њ–ї–µ–Ї—Г–ї–Њ—О CD4 вАФ —Е–µ–Љ–Њ–Ї—Ц–љ–Њ–≤–Є–Љ —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ, —П–Ї–Є–є –Ј–∞–Ј–≤–Є—З–∞–є –Ј—Г—Б—В—А—Ц—З–∞—Ф—В—М—Б—П –љ–∞ –њ–Њ–≤–µ—А—Е–љ—Ц CD4+ T-–ї—Ц–Љ—Д–Њ—Ж–Є—В—Ц–≤ . –¶–µ–є –Љ–µ—Е–∞–љ—Ц–Ј–Љ –Ј–∞–±–µ–Ј–њ–µ—З—Г—Ф —Ц–љ—Д—Ц–Ї—Г–≤–∞–љ–љ—П –≤—Ц—А—Г—Б–Њ–Љ —В—Ц–ї—М–Ї–Є —В–Є—Е –Ї–ї—Ц—В–Є–љ, —П–Ї—Ц –Ј–і–∞—В–љ—Ц –Ј–і—Ц–є—Б–љ–Є—В–Є –є–Њ–≥–Њ —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—О. –Ч–≤'—П–Ј—Г–≤–∞–љ–љ—П –Ј —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ –Љ–Њ–ґ–µ —Б–њ—А–Є—З–Є–љ–Є—В–Є –Ї–Њ–љ—Д–Њ—А–Љ–∞—Ж—Ц–є–љ—Ц –Ј–Љ—Ц–љ–Є –±—Ц–ї–Ї—Ц–≤ –Њ–±–Њ–ї–Њ–љ–Ї–Є (–∞–±–Њ –±—Ц–ї–Ї–∞ –Ї–∞–њ—Б–Є–і—Г –≤ —А–∞–Ј—Ц –±–µ–Ј–Њ–±–Њ–ї–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –≤—Ц—А—Г—Б—Г), —Й–Њ –≤–Њ–і–љ–Њ—З–∞—Б —Ф —Б–Є–≥–љ–∞–ї–Њ–Љ –і–Њ –Ј–ї–Є—В—В—П –≤—Ц—А—Г—Б–љ–Њ—Ч —Ц –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч –Љ–µ–Љ–±—А–∞–љ —Ц –њ—А–Њ–љ–Є–Ї–љ–µ–љ–љ—П –≤—Ц—А—Г—Б—Г –≤ –Ї–ї—Ц—В–Є–љ—Г.–Я—А–Њ–љ–Є–Ї–љ–µ–љ–љ—П –≤ –Ї–ї—Ц—В–Є–љ—Г. –Э–∞ –љ–∞—Б—В—Г–њ–љ–Њ–Љ—Г –µ—В–∞–њ—Ц –≤—Ц—А—Г—Б –Љ–∞—Ф –і–Њ–њ—А–∞–≤–Є—В–Є –≤—Б–µ—А–µ–і–Є–љ—Г –Ї–ї—Ц—В–Є–љ–Є —Б–≤—Ц–є –≥–µ–љ–µ—В–Є—З–љ–Є–є –Љ–∞—В–µ—А—Ц–∞–ї. –Ф–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є –≤–љ–Њ—Б—П—В—М —В–∞–Ї–Њ–ґ –≤–ї–∞—Б–љ—Ц –±—Ц–ї–Ї–Є, –љ–µ–Њ–±—Е—Ц–і–љ—Ц –і–ї—П —Ч—Ч —А–µ–∞–ї—Ц–Ј–∞—Ж—Ц—Ч (–Њ—Б–Њ–±–ї–Є–≤–Њ —Ж–µ –њ—А–Є—В–∞–Љ–∞–љ–љ–Њ –і–ї—П –≤—Ц—А—Г—Б—Ц–≤, —П–Ї—Ц –Љ—Ц—Б—В—П—В—М –љ–µ–≥–∞—В–Є–≤–љ—Ц –†–Э–Ъ). –†—Ц–Ј–љ—Ц –≤—Ц—А—Г—Б–Є –і–ї—П –њ—А–Њ–љ–Є–Ї–љ–µ–љ–љ—П –≤ –Ї–ї—Ц—В–Є–љ—Г –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М –≤—Ц–і–Љ—Ц–љ–љ—Ц —Б—В—А–∞—В–µ–≥—Ц—Ч: –љ–∞–њ—А–Є–Ї–ї–∞–і, –њ—Ц–Ї–Њ—А–љ–∞–≤—Ц—А—Г—Б–Є –≤–њ–Њ—А—Б–Ї—Г—О—В—М —Б–≤–Њ—О –†–Э–Ъ –Ї—А—Ц–Ј—М –њ–ї–∞–Ј–Љ–∞—В–Є—З–љ—Г –Љ–µ–Љ–±—А–∞–љ—Г, –∞ –≤—Ц—А—Ц–Њ–љ–Є –Њ—А—В–Њ–Љ—Ц–Ї—Б–Њ–≤—Ц—А—Г—Б—Ц–≤ –Ј–∞—Е–Њ–њ–ї—О—О—В—М—Б—П –Ї–ї—Ц—В–Є–љ–Њ—О –≤ —Е–Њ–і—Ц –µ–љ–і–Њ—Ж–Є—В–Њ–Ј—Г –є –њ–Њ—В—А–∞–њ–ї—П—О—В—М –≤ –Ї–Є—Б–ї–µ —Б–µ—А–µ–і–Њ–≤–Є—Й–µ –ї—Ц–Ј–Њ—Б–Њ–Љ , –і–µ –≤—Ц–і–±—Г–≤–∞—Ф—В—М—Б—П –і–µ–њ—А–Њ—В–µ—Ч–љ—Ц–Ј–∞—Ж—Ц—П –≤—Ц—А—Г—Б–љ–Њ—Ч —З–∞—Б—В–Є–љ–Ї–Є, –њ—Ц—Б–ї—П —З–Њ–≥–Њ –†–Э–Ъ –≤ —Б—Г–Ї—Г–њ–љ–Њ—Б—В—Ц –Ј –≤—Ц—А—Г—Б–љ–Є–Љ–Є –±—Ц–ї–Ї–∞–Љ–Є –і–Њ–ї–∞—Ф –ї—Ц–Ј–Њ—Б–Њ–Љ–∞–ї—М–љ—Г –Љ–µ–Љ–±—А–∞–љ—Г —Ц –њ—А–Њ—Е–Њ–і–Є—В—М —Г —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ—Г . –Т—Ц—А—Г—Б–Є —В–∞–Ї–Њ–ґ —А–Њ–Ј—А—Ц–Ј–љ—П—О—В—М –Ј–∞ —В–Є–Љ, –і–µ –≤—Ц–і–±—Г–≤–∞—Ф—В—М—Б—П —Ч—Е–љ—П —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—П: —З–∞—Б—В–Є–љ–∞ –≤—Ц—А—Г—Б—Ц–≤ (–љ–∞–њ—А–Є–Ї–ї–∞–і, —В—Ц –ґ –њ—Ц–Ї–Њ—А–љ–∞–≤—Ц—А—Г—Б–Є) —А–Њ–Ј–Љ–љ–Њ–ґ—Г—Ф—В—М—Б—П –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ—Ц –Ї–ї—Ц—В–Є–љ–Є, –∞ —З–∞—Б—В–Є–љ–∞ (–љ–∞–њ—А–Є–Ї–ї–∞–і, –Њ—А—В–Њ–Љ—Ц–Ї—Б–Њ–≤—Ц—А—Г—Б–Є ) –≤ —Ч—Ч —П–і—А—Ц . –•—Ц–і —Ц–љ—Д—Ц–Ї—Г–≤–∞–љ–љ—П –≤—Ц—А—Г—Б–∞–Љ–Є –Ї–ї—Ц—В–Є–љ –≥—А–Є–±—Ц–≤ —Ц —А–Њ—Б–ї–Є–љ –≤—Ц–і—А—Ц–Ј–љ—П—Ф—В—М—Б—П –≤—Ц–і —Ц–љ—Д—Ц–Ї—Г–≤–∞–љ–љ—П –Ї–ї—Ц—В–Є–љ —В–≤–∞—А–Є–љ. –†–Њ—Б–ї–Є–љ–Є –Љ–∞—О—В—М –Љ—Ц—Ж–љ—Г –Ї–ї—Ц—В–Є–љ–љ—Г —Б—В—Ц–љ–Ї—Г , —Й–Њ —Б–Ї–ї–∞–і–∞—Ф—В—М—Б—П –Ј —Ж–µ–ї—О–ї–Њ–Ј–Є , –∞ –≥—А–Є–±–Є вАФ –Ј —Е—Ц—В–Є–љ—Г , —В–Њ–ґ –±—Ц–ї—М—И—Ц—Б—В—М –≤—Ц—А—Г—Б—Ц–≤ –Љ–Њ–ґ—Г—В—М –њ—А–Њ–є—В–Є –≤ –љ–Є—Е –ї–Є—И–µ –њ—Ц—Б–ї—П —Г—И–Ї–Њ–і–ґ–µ–љ–љ—П –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч —Б—В—Ц–љ–Ї–Є. –Ю–і–љ–∞–Ї –Љ–∞–є–ґ–µ –≤—Б—Ц –≤—Ц—А—Г—Б–Є —А–Њ—Б–ї–Є–љ (–Ј–Њ–Ї—А–µ–Љ–∞ –≤—Ц—А—Г—Б —В—О—В—О–љ–Њ–≤–Њ—Ч –Љ–Њ–Ј–∞—Ч–Ї–Є) –Љ–Њ–ґ—Г—В—М –њ–µ—А–µ–Љ—Ц—Й–∞—В–Є—Б—П –Ј –Ї–ї—Ц—В–Є–љ–Є –≤ –Ї–ї—Ц—В–Є–љ—Г —Г —Д–Њ—А–Љ—Ц –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є—Е –љ—Г–Ї–ї–µ–Њ–њ—А–Њ—В–µ—Ч–љ–Њ–≤–Є—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б—Ц–≤ —З–µ—А–µ–Ј –њ–ї–∞–Ј–Љ–Њ–і–µ—Б–Љ–Є [ 95] –Я–Њ–Ј–±–∞–≤–ї–µ–љ–љ—П –Њ–±–Њ–ї–Њ–љ–Њ–Ї вАФ —Ж–µ –њ—А–Њ—Ж–µ—Б –≤—В—А–∞—В–Є –Ї–∞–њ—Б–Є–і—Г. –¶–µ –і–Њ—Б—П–≥–∞—Ф—В—М—Б—П –Ј–∞ –і–Њ–њ–Њ–Љ–Њ–≥–Њ—О –≤—Ц—А—Г—Б–љ–Є—Е —Д–µ—А–Љ–µ–љ—В—Ц–≤ –∞–±–Њ —Д–µ—А–Љ–µ–љ—В—Ц–≤ –Ї–ї—Ц—В–Є–љ–Є-–≥–Њ—Б–њ–Њ–і–∞—А—П, –∞ –Љ–Њ–ґ–µ –±—Г—В–Є —Ц –љ–∞—Б–ї—Ц–і–Ї–Њ–Љ –њ—А–Њ—Б—В–Њ—Ч –і–Є—Б–Њ—Ж—Ц–∞—Ж—Ц—Ч . –Ч—А–µ—И—В–Њ—О –≤—Ц—А—Г—Б–љ–∞ –≥–µ–љ–Њ–Љ–љ–∞ –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–∞ –Ї–Є—Б–ї–Њ—В–∞ –≤–Є–≤—Ц–ї—М–љ—П—Ф—В—М—Б—П.–†–µ–њ–ї—Ц–Ї–∞—Ж—Ц—П –≤—Ц—А—Ц–Њ–љ–љ–Є—Е –±—Ц–ї–Ї—Ц–≤.–Т—Ц–і–±—А—Г–љ—М–Ї—Г–≤–∞–љ–љ—П –≤—Ц—А—Г—Б—Г –≤—Ц–і –Ї–ї—Ц—В–Є–љ–Є-—Е–∞–Ј—П—Ч–љ–∞ –Я—Ц—Б–ї—П —Ж—М–Њ–≥–Њ –≤—Ц–і–±—Г–≤–∞—Ф—В—М—Б—П —Б–Ї–ї–∞–і–∞–љ–љ—П –≤—Ц—А—Г—Б–љ–Є—Е —З–∞—Б—В–Є–љ–Њ–Ї, –Ј–≥–Њ–і–Њ–Љ —Б—В–∞—О—В—М—Б—П –і–µ—П–Ї—Ц –Љ–Њ–і–Є—Д—Ц–Ї–∞—Ж—Ц—Ч –±—Ц–ї–Ї—Ц–≤. –£ –≤—Ц—А—Г—Б—Ц–≤, —В–∞–Ї–Є—Е —П–Ї –Т–Ж–Ы, —В–∞–Ї—Ц –њ–µ—А–µ—В–≤–Њ—А–µ–љ–љ—П (—Ц–љ–Њ–і—Ц –Ј–≤–∞–љ—Ц –і–Њ–Ј—А—Ц–≤–∞–љ–љ—П–Љ) –≤—Ц–і–±—Г–≤–∞—О—В—М—Б—П –њ—Ц—Б–ї—П –≤–Є—Е–Њ–і—Г –≤—Ц—А—Г—Б—Г –Ј –Ї–ї—Ц—В–Є–љ–Є-–≥–Њ—Б–њ–Њ–і–∞—А—П[ 97]
–Т–Є—Е—Ц–і —Ц–Ј –Ї–ї—Ц—В–Є–љ–Є. –Т—Ц—А—Г—Б–Є –Љ–Њ–ґ—Г—В—М –њ–Њ–Ї–Є–љ—Г—В–Є –Ї–ї—Ц—В–Є–љ—Г –њ—Ц—Б–ї—П –ї—Ц–Ј–Є—Б—Г , –њ—А–Њ—Ж–µ—Б—Г, –њ—Ц–і —З–∞—Б —П–Ї–Њ–≥–Њ –Ї–ї—Ц—В–Є–љ–∞ –≥–Є–љ–µ —З–µ—А–µ–Ј —А–Њ–Ј—А–Є–≤ –Љ–µ–Љ–±—А–∞–љ–Є —Ц –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч —Б—В—Ц–љ–Ї–Є, —П–Ї—Й–Њ –≤–Њ–љ–∞ —Ф. –¶—П –Њ—Б–Њ–±–ї–Є–≤—Ц—Б—В—М —Ф —Г –±–∞–≥–∞—В—М–Њ—Е –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Є—Е —Ц –і–µ—П–Ї–Є—Е —В–≤–∞—А–Є–љ–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤. –Ф–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є –њ—Ц–і–ї—П–≥–∞—О—В—М –ї—Ц–Ј–Њ–≥–µ–љ–љ–Њ–Љ—Г —Ж–Є–Ї–ї—Г , –і–µ –≤—Ц—А—Г—Б–љ–Є–є –≥–µ–љ–Њ–Љ –Ј–∞–ї—Г—З–∞—Ф—В—М—Б—П —И–ї—П—Е–Њ–Љ –≥–µ–љ–µ—В–Є—З–љ–Њ—Ч —А–µ–Ї–Њ–Љ–±—Ц–љ–∞—Ж—Ц—Ч —Г —Б–њ–µ—Ж—Ц–∞–ї—М–љ–µ –Љ—Ц—Б—Ж–µ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–Є –Ї–ї—Ц—В–Є–љ–Є-–≥–Њ—Б–њ–Њ–і–∞—А—П. –Ґ–Њ–і—Ц –≤—Ц—А—Г—Б–љ–Є–є –≥–µ–љ–Њ–Љ –љ–∞–Ј–Є–≤–∞—О—В—М –њ—А–Њ–≤—Ц—А—Г—Б–Њ–Љ –њ—А–Њ—Д–∞–≥–Њ–Љ –Т—Ц—А—Г—Б, —Й–Њ –∞–Ї—В–Є–≤–љ–Њ —А–Њ–Ј–Љ–љ–Њ–ґ—Г—Ф—В—М—Б—П, –љ–µ –Ј–∞–≤–ґ–і–Є –≤–±–Є–≤–∞—Ф –Ї–ї—Ц—В–Є–љ—Г-–≥–Њ—Б–њ–Њ–і–∞—А—П. –Ю–±–Њ–ї–Њ–љ–Ї–Њ–≤—Ц –≤—Ц—А—Г—Б–Є, –Ј–Њ–Ї—А–µ–Љ–∞ –Т–Ж–Ы, –Ј–∞–Ј–≤–Є—З–∞–є –≤—Ц–і–Њ–Ї—А–µ–Љ–ї—О—О—В—М—Б—П –≤—Ц–і –Ї–ї—Ц—В–Є–љ–Є —И–ї—П—Е–Њ–Љ –±—А—Г–љ—М–Ї—Г–≤–∞–љ–љ—П . –£ —Е–Њ–і—Ц —Ж—М–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Г –≤—Ц—А—Г—Б –Њ—В—А–Є–Љ—Г—Ф —Б–≤–Њ—О –Њ–±–Њ–ї–Њ–љ–Ї—Г, —Й–Њ —Ф –Љ–Њ–і–Є—Д—Ц–Ї–Њ–≤–∞–љ–Є–Љ —Д—А–∞–≥–Љ–µ–љ—В–Њ–Љ –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч –Љ–µ–Љ–±—А–∞–љ–Є –≥–Њ—Б–њ–Њ–і–∞—А—П –∞–±–Њ —Ц–љ—И–Њ—Ч –≤–љ—Г—В—А—Ц—И–љ—М–Њ—Ч –Љ–µ–Љ–±—А–∞–љ–Є. –Ю—В–ґ–µ, –Ї–ї—Ц—В–Є–љ–∞ –Љ–Њ–ґ–µ –њ—А–Њ–і–Њ–≤–ґ—Г–≤–∞—В–Є –ґ–Є—В–Є —Ц –≤–Є—А–Њ–±–ї—П—В–Є –≤—Ц—А—Г—Б.
–У–µ–љ–µ—В–Є—З–љ–Є–є –Љ–∞—В–µ—А—Ц–∞–ї –≤—Б–µ—А–µ–і–Є–љ—Ц –≤—Ц—А—Г—Б–љ–Є—Е —З–∞—Б—В–Є–љ–Њ–Ї —Ц —Б–њ–Њ—Б—Ц–± –є–Њ–≥–Њ —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—Ч –Ј–љ–∞—З–љ–Њ –≤—Ц–і—А—Ц–Ј–љ—П—Ф—В—М—Б—П —Г —А—Ц–Ј–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤.
–Ф–Э–Ъ-–≤–Љ—Ц—Б–љ—Ц –≤—Ц—А—Г—Б–Є [en] –≥–µ—А–њ–µ—Б–≤—Ц—А—Г—Б–Є ), –∞–±–Њ, —Й–Њ –±—Г–≤–∞—Ф —З–∞—Б—В—Ц—И–µ вАФ —И–ї—П—Е–Њ–Љ —А–µ—Ж–µ–њ—В–Њ—А-–Ј–∞–ї–µ–ґ–љ–Њ–≥–Њ –µ–љ–і–Њ—Ж–Є—В–Њ–Ј—Г. –С—Ц–ї—М—И—Ц—Б—В—М –Ф–Э–Ъ-–≤–Љ—Ц—Б–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –њ–Њ–≤–љ—Ц—Б—В—О –њ–Њ–Ї–ї–∞–і–∞—О—В—М—Б—П –љ–∞ —Б–Є–љ—В–µ—В–Є—З–љ–Є–є –∞–њ–∞—А–∞—В –Ї–ї—Ц—В–Є–љ–Є-–≥–Њ—Б–њ–Њ–і–∞—А—П –і–ї—П –≤–Є—А–Њ–±–љ–Є—Ж—В–≤–∞ —Ч—Е–љ—М–Њ–≥–Њ –Ф–Э–Ъ —Ц –†–Э–Ъ , –∞ —В–∞–Ї–Њ–ґ –њ–Њ–і–∞–ї—М—И–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б–Є–љ–≥—Г –†–Э–Ъ . –Ю–і–љ–∞–Ї –≤—Ц—А—Г—Б–Є –Ј –≤–µ–ї–Є–Ї–Є–Љ–Є –≥–µ–љ–Њ–Љ–∞–Љ–Є (–љ–∞–њ—А–Є–Ї–ї–∞–і, –њ–Њ–Ї—Б–≤—Ц—А—Г—Б–Є ) –Љ–Њ–ґ—Г—В—М —Б–∞–Љ–Њ—Б—В—Ц–є–љ–Њ –Ї–Њ–і—Г–≤–∞—В–Є –±—Ц–ї—М—И—Г —З–∞—Б—В–Є–љ—Г –љ–µ–Њ–±—Е—Ц–і–љ–Є—Е –і–ї—П —Ж—М–Њ–≥–Њ –±—Ц–ї–Ї—Ц–≤. –У–µ–љ–Њ–Љ –≤—Ц—А—Г—Б—Г –µ—Г–Ї–∞—А—Ц–Њ—В—Ц–≤ –Љ–∞—Ф –њ–Њ–і–Њ–ї–∞—В–Є —П–і–µ—А–љ—Г –Њ–±–Њ–ї–Њ–љ–Ї—Г –і–ї—П —В–Њ–≥–Њ, —Й–Њ–± –Њ—В—А–Є–Љ–∞—В–Є –і–Њ—Б—В—Г–њ –і–Њ —Д–µ—А–Љ–µ–љ—В—Ц–≤, —П–Ї—Ц —Б–Є–љ—В–µ–Ј—Г—О—В—М –Ф–Э–Ъ —Ц –†–Э–Ъ, —Г —А–∞–Ј—Ц –ґ –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥—Ц–≤ –є–Њ–Љ—Г –і–Њ—Б–Є—В—М –њ—А–Њ—Б—В–Њ –њ—А–Њ–є—В–Є –≤ –Ї–ї—Ц—В–Є–љ—Г.–†–Э–Ъ-–≤–Љ—Ц—Б–љ—Ц –≤—Ц—А—Г—Б–Є [en] [ 103] –†–Э–Ъ-—А–µ–њ–ї—Ц–Ї–∞–Ј—Г –і–ї—П –Ї–Њ–њ—Ц—О–≤–∞–љ–љ—П —Б–≤–Њ—Ч—Е –≥–µ–љ–Њ–Љ—Ц–≤.–Т—Ц—А—Г—Б–Є, —Й–Њ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М –Ј–≤–Њ—А–Њ—В–љ—Г —В—А–∞–љ—Б–Ї—А–Є–њ—Ж—Ц—О . –¶—Ц –≤—Ц—А—Г—Б–Є –Љ—Ц—Б—В—П—В—М –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –†–Э–Ъ (—А–µ—В—А–Њ–≤—Ц—А—Г—Б–Є Metaviridae Pseudoviridae [en] –Ї–∞—Г–ї—Ц–Љ–Њ–≤—Ц—А—Г—Б–Є –≥–µ–њ–∞–і–љ–∞–≤—Ц—А—Г—Б–Є —А–µ—В—А–Њ–≤—Ц—А—Г—Б–Є , –љ–∞–њ—А–Є–Ї–ї–∞–і, –Т–Ж–Ы), –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М –Ф–Э–Ъ-–Ї–Њ–њ—Ц—О –≥–µ–љ–Њ–Љ—Г —П–Ї –њ—А–Њ–Љ—Ц–ґ–љ—Г –Љ–Њ–ї–µ–Ї—Г–ї—Г –њ—Ц–і —З–∞—Б —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—Ч, –∞ —В—Ц, —Й–Њ –Љ—Ц—Б—В—П—В—М –Ф–Э–Ъ (–њ–∞—А–∞—А–µ—В—А–Њ–≤—Ц—А—Г—Б–Є , –љ–∞–њ—А–Є–Ї–ї–∞–і, –≤—Ц—А—Г—Б –≥–µ–њ–∞—В–Є—В—Г B ) вАФ –†–Э–Ъ. –Т –Њ–±–Њ—Е –≤–Є–њ–∞–і–Ї–∞—Е –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—Ф—В—М—Б—П –Ј–≤–Њ—А–Њ—В–љ–∞ —В—А–∞–љ—Б–Ї—А–Є–њ—В–∞–Ј–∞ , –∞–±–Њ –†–Э–Ъ-–Ј–∞–ї–µ–ґ–љ–∞ –Ф–Э–Ъ-–њ–Њ–ї—Ц–Љ–µ—А–∞–Ј–∞. –†–µ—В—А–Њ–≤—Ц—А—Г—Б–Є –≤–±—Г–і–Њ–≤—Г—О—В—М –Ф–Э–Ъ, —Й–Њ —Г—В–≤–Њ—А—О—Ф—В—М—Б—П —Г –њ—А–Њ—Ж–µ—Б—Ц –Ј–≤–Њ—А–Њ—В–љ–Њ—Ч —В—А–∞–љ—Б–Ї—А–Є–њ—Ж—Ц—Ч, –≤ –≥–µ–љ–Њ–Љ –≥–Њ—Б–њ–Њ–і–∞—А—П, —В–∞–Ї–Є–є —Б—В–∞–љ –≤—Ц—А—Г—Б—Г –љ–∞–Ј–Є–≤–∞—О—В—М –њ—А–Њ–≤—Ц—А—Г—Б–Њ–Љ . –Я–∞—А–∞—А–µ—В—А–Њ–≤—Ц—А—Г—Б–Є –ґ —Ж—М–Њ–≥–Њ –љ–µ —А–Њ–±–ї—П—В—М, —Е–Њ—З–∞ –≤–±—Г–і–Њ–≤–∞–љ—Ц –Ї–Њ–њ—Ц—Ч —Ч—Е–љ—М–Њ–≥–Њ –≥–µ–љ–Њ–Љ—Г –Љ–Њ–ґ—Г—В—М –і–∞–≤–∞—В–Є –њ–Њ—З–∞—В–Њ–Ї —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є–Љ –≤—Ц—А—Г—Б–∞–Љ, –Њ—Б–Њ–±–ї–Є–≤–Њ —Г —А–Њ—Б–ї–Є–љ[ 106] –њ—А–Њ—В–Є–≤—Ц—А—Г—Б–љ–Є—Е –њ—А–µ–њ–∞—А–∞—В—Ц–≤ , —Й–Њ —Ц–љ–≥—Ц–±—Г—О—В—М –Ј–≤–Њ—А–Њ—В–љ—Г —В—А–∞–љ—Б–Ї—А–Є–њ—В–∞–Ј—Г, –Ј–Њ–Ї—А–µ–Љ–∞ –і–Њ –Ј—Ц–і–Њ–≤—Г–і–Є–љ—Г —В–∞ –ї–∞–Љ—Ц–≤—Г–і–Є–љ—Г .
–Ь—Ц–Ї—А–Њ—Д–Њ—В–Њ–≥—А–∞—Д—Ц—П , —Й–Њ –њ–Њ–Ї–∞–Ј—Г—Ф —Ж–Є—В–Њ–њ–∞—В–Є—З–љ—Ц –µ—Д–µ–Ї—В–Є, —Б–њ—А–Є—З–Є–љ–µ–љ—Ц –≤—Ц—А—Г—Б–Њ–Љ –њ—А–Њ—Б—В–Њ–≥–Њ –≥–µ—А–њ–µ—Б—Г 1-–≥–Њ —В–Є–њ—Г. –Ґ–µ—Б—В –Я–∞–њ–∞–љ—Ц–Ї–Њ–ї–∞—Г –Ф—Ц–∞–њ–∞–Ј–Њ–љ —Б—В—А—Г–Ї—В—Г—А–љ–Є—Е —В–∞ –±—Ц–Њ—Е—Ц–Љ—Ц—З–љ–Є—Е –µ—Д–µ–Ї—В—Ц–≤, —Й–Њ —Б–њ—А–Є—З–Є–љ—О—Ф –≤—Ц—А—Г—Б –≤ —Ц–љ—Д—Ц–Ї–Њ–≤–∞–љ—Ц–є –Ї–ї—Ц—В–Є–љ—Ц, –і—Г–ґ–µ —И–Є—А–Њ–Ї–Є–є. –З—Е –љ–∞–Ј–Є–≤–∞—О—В—М —Ж–Є—В–Њ–њ–∞—В–Є—З–љ–Є–Љ–Є –µ—Д–µ–Ї—В–∞–Љ–Є [en] –∞–њ–Њ–њ—В–Њ–Ј [ 109] [ 110]
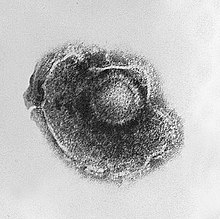
–Ф–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є –љ–µ —Б–њ—А–Є—З–Є–љ—О—О—В—М –ґ–Њ–і–љ–Є—Е –≤–Є–і–Є–Љ–Є—Е –Ј–Љ—Ц–љ –≤ —Г—А–∞–ґ–µ–љ—Ц–є –Ї–ї—Ц—В–Є–љ—Ц. –Ъ–ї—Ц—В–Є–љ–Є, –≤ —П–Ї–Є—Е –≤—Ц—А—Г—Б –њ–µ—А–µ–±—Г–≤–∞—Ф –≤ –ї–∞—В–µ–љ—В–љ–Њ–Љ—Г —Б—В–∞–љ—Ц —Ц –љ–µ–∞–Ї—В–Є–≤–љ–Є–є, –Љ–∞—О—В—М –Љ–∞–ї–Њ –Њ–Ј–љ–∞–Ї —Ц–љ—Д–µ–Ї—Ж—Ц—Ч —Ц –љ–Њ—А–Љ–∞–ї—М–љ–Њ —Д—Г–љ–Ї—Ж—Ц—О—О—В—М[ 111] –≥–µ—А–њ–µ—Б—Г [ 112] [ 113] –≤—Ц—А—Г—Б –Х–њ—И—В–µ–є–љ–∞ вАФ –С–∞—А—А , –Љ–Њ–ґ—Г—В—М —Б–њ—А–Є—З–Є–љ–Є—В–Є —И–≤–Є–і–Ї–µ —А–Њ–Ј–Љ–љ–Њ–ґ–µ–љ–љ—П –Ї–ї—Ц—В–Є–љ –±–µ–Ј –њ–Њ—П–≤–Є –Ј–ї–Њ—П–Ї—Ц—Б–љ–Њ—Б—В—Ц[ 114] –њ–∞–њ—Ц–ї–Њ–Љ–∞–≤—Ц—А—Г—Б–Є , –Љ–Њ–ґ—Г—В—М –њ–Њ—А–Њ–і–Є—В–Є —А–∞–Ї [ 115]
–Т—Ц—А—Г—Б–Є, –±–µ–Ј–њ–µ—А–µ—З–љ–Њ, —Ф –љ–∞–є—З–Є—Б–ї–µ–љ–љ—Ц—И–Є–Љ–Є –±—Ц–Њ–ї–Њ–≥—Ц—З–љ–Є–Љ–Є –Њ–±'—Ф–Ї—В–∞–Љ–Є –љ–∞ –Ч–µ–Љ–ї—Ц, —Ц –Ј–∞ —Ж–Є–Љ –њ–Њ–Ї–∞–Ј–љ–Є–Ї–Њ–Љ –≤–Њ–љ–Є –њ–µ—А–µ–≤–µ—А—И—Г—О—В—М —Г—Б—Ц –Њ—А–≥–∞–љ—Ц–Ј–Љ–Є, —А–∞–Ј–Њ–Љ —Г–Ј—П—В—Ц[ 116] —Е–∞–Ј—П—Ч–≤ , –±–∞–≥–∞—В–Њ –≤—Ц—А—Г—Б—Ц–≤ –≤–Є–і–Њ—Б–њ–µ—Ж–Є—Д—Ц—З–љ—Ц. –Ф–µ—П–Ї—Ц, —П–Ї, –љ–∞–њ—А–Є–Ї–ї–∞–і, –≤—Ц—А—Г—Б –≤—Ц—Б–њ–Є , –Љ–Њ–ґ—Г—В—М –≤—А–∞–ґ–∞—В–Є —В—Ц–ї—М–Ї–Є –Њ–і–Є–љ –≤–Є–і вАФ –ї—О–і–µ–є , —Г —В–∞–Ї–Є—Е –≤–Є–њ–∞–і–Ї–∞—Е –Ї–∞–ґ—Г—В—М, —Й–Њ –≤—Ц—А—Г—Б –Љ–∞—Ф –≤—Г–Ј—М–Ї–Є–є –і—Ц–∞–њ–∞–Ј–Њ–љ —Е–∞–Ј—П—Ч–≤. –Э–∞–≤–њ–∞–Ї–Є, –≤—Ц—А—Г—Б —Б–Ї–∞–Ј—Г –Љ–Њ–ґ–µ –≤—А–∞–ґ–∞—В–Є —А—Ц–Ј–љ—Ц –≤–Є–і–Є —Б—Б–∞–≤—Ж—Ц–≤, —В–Њ–±—В–Њ –≤—Ц–љ –Љ–∞—Ф —И–Є—А–Њ–Ї–Є–є –і—Ц–∞–њ–∞–Ј–Њ–љ —Е–∞–Ј—П—Ч–≤. –Т—Ц—А—Г—Б–Є —А–Њ—Б–ї–Є–љ –љ–µ—И–Ї—Ц–і–ї–Є–≤—Ц –і–ї—П —В–≤–∞—А–Є–љ, –∞ –±—Ц–ї—М—И—Ц—Б—В—М –≤—Ц—А—Г—Б—Ц–≤ —В–≤–∞—А–Є–љ –±–µ–Ј–њ–µ—З–љ—Ц –і–ї—П –ї—О–і–Є–љ–Є. –Ф—Ц–∞–њ–∞–Ј–Њ–љ –≥–Њ—Б–њ–Њ–і–∞—А—Ц–≤ –і–µ—П–Ї–Є—Е –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥—Ц–≤ –Њ–±–Љ–µ–ґ—Г—Ф—В—М—Б—П –Њ–і–љ–Є–Љ —И—В–∞–Љ–Њ–Љ –±–∞–Ї—В–µ—А—Ц–є, —Ц —Ч—Е –Љ–Њ–ґ–љ–∞ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞—В–Є –і–ї—П –≤–Є–Ј–љ–∞—З–µ–љ–љ—П —И—В–∞–Љ—Ц–≤, —Й–Њ —Б–њ—А–Є—З–Є–љ—О—О—В—М —Б–њ–∞–ї–∞—Е–Є —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є—Е –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ—М –Љ–µ—В–Њ–і–Њ–Љ —Д–∞–≥–Њ–≤–Њ–≥–Њ —В–Є–њ—Г–≤–∞–љ–љ—П[ 120]
–Т—Ц—А—Г—Б–Є –њ–Њ—И–Є—А—О—О—В—М—Б—П –±–∞–≥–∞—В—М–Љ–∞ —Б–њ–Њ—Б–Њ–±–∞–Љ–Є: –≤—Ц—А—Г—Б–Є —А–Њ—Б–ї–Є–љ —З–∞—Б—В–Њ –њ–µ—А–µ–і–∞—О—В—М—Б—П –≤—Ц–і —А–Њ—Б–ї–Є–љ–Є –і–Њ —А–Њ—Б–ї–Є–љ–Є –Ї–Њ–Љ–∞—Е–∞–Љ–Є , —Й–Њ —Е–∞—А—З—Г—О—В—М—Б—П —А–Њ—Б–ї–Є–љ–љ–Є–Љ–Є —Б–Њ–Ї–∞–Љ–Є, –љ–∞–њ—А–Є–Ї–ї–∞–і, –њ–Њ–њ–µ–ї–Є—Ж—П–Љ–Є ; –≤—Ц—А—Г—Б–Є —В–≤–∞—А–Є–љ –Љ–Њ–ґ—Г—В—М –њ–Њ—И–Є—А—О–≤–∞—В–Є—Б—П –Ї–Њ–Љ–∞—Е–∞–Љ–Є, —В–∞–Ї—Ц –Њ—А–≥–∞–љ—Ц–Ј–Љ–Є –≤—Ц–і–Њ–Љ—Ц —П–Ї –њ–µ—А–µ–љ–Њ—Б–љ–Є–Ї–Є . –Т—Ц—А—Г—Б –≥—А–Є–њ—Г –њ–Њ—И–Є—А—О—Ф—В—М—Б—П –њ–Њ–≤—Ц—В—А—П–љ–Њ-–Ї—А–∞–њ–µ–ї—М–љ–Є–Љ —И–ї—П—Е–Њ–Љ –њ—Ц–і —З–∞—Б –Ї–∞—И–ї—О —В–∞ —З—Е–∞–љ–љ—П . –Э–Њ—А–Њ–≤—Ц—А—Г—Б —Ц —А–Њ—В–∞–≤—Ц—А—Г—Б , —Й–Њ –Ј–∞–Ј–≤–Є—З–∞–є —Б–њ—А–Є—З–Є–љ—О—О—В—М –≤—Ц—А—Г—Б–љ—Ц –≥–∞—Б—В—А–Њ–µ–љ—В–µ—А–Є—В–Є , –њ–µ—А–µ–і–∞—О—В—М—Б—П —Д–µ–Ї–∞–ї—М–љ–Њ-–Њ—А–∞–ї—М–љ–Є–Љ —И–ї—П—Е–Њ–Љ –њ—Ц–і —З–∞—Б –Ї–Њ–љ—В–∞–Ї—В—Г –Ј –Ј–∞—А–∞–ґ–µ–љ–Њ—О —Ч–ґ–µ—О –∞–±–Њ –≤–Њ–і–Њ—О. –Т–Ж–Ы —Ф –Њ–і–љ–Є–Љ –Ј –і–µ–Ї—Ц–ї—М–Ї–Њ—Е –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –њ–µ—А–µ–і–∞—О—В—М—Б—П —Б—В–∞—В–µ–≤–Є–Љ —И–ї—П—Е–Њ–Љ —Ц –њ—Ц–і —З–∞—Б –њ–µ—А–µ–ї–Є–≤–∞–љ–љ—П –Ј–∞—А–∞–ґ–µ–љ–Њ—Ч –Ї—А–Њ–≤—Ц. –Ъ–Њ–ґ–µ–љ –≤—Ц—А—Г—Б –Љ–∞—Ф –њ–µ–≤–љ—Г —Б–њ–µ—Ж–Є—Д—Ц—З–љ—Ц—Б—В—М –і–Њ —Е–∞–Ј—П—Ч–≤ , —Й–Њ –≤–Є–Ј–љ–∞—З–∞—Ф—В—М—Б—П —В–Є–њ–∞–Љ–Є –Ї–ї—Ц—В–Є–љ, —П–Ї—Ц –≤—Ц–љ –Љ–Њ–ґ–µ —Ц–љ—Д—Ц–Ї—Г–≤–∞—В–Є. –Ъ–Њ–ї–Њ –≥–Њ—Б–њ–Њ–і–∞—А—Ц–≤ –Љ–Њ–ґ–µ –±—Г—В–Є –≤—Г–Ј—М–Ї–Є–Љ –∞–±–Њ, —П–Ї—Й–Њ –≤—Ц—А—Г—Б –≤—А–∞–ґ–∞—Ф –±–∞–≥–∞—В–Њ –≤–Є–і—Ц–≤, —И–Є—А–Њ–Ї–Є–Љ.
–£ –±—Ц–Њ–ї–Њ–≥—Ц—З–љ—Ц–є –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—Ч –≤—Ц—А—Г—Б–Є –≤–Є–і—Ц–ї—П—О—В—М –≤ –Њ–Ї—А–µ–Љ–Є–є —В–∞–Ї—Б–Њ–љ, —П–Ї–Є–є —Г—В–≤–Њ—А—О—Ф –≤ –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—Ч Systema Naturae 2000 —А–∞–Ј–Њ–Љ –Ј –і–Њ–Љ–µ–љ–∞–Љ–Є Bacteria , Archaea —Ц Eukaryota –Ї–Њ—А–µ–љ–µ–≤–Є–є —В–∞–Ї—Б–Њ–љ Biota [ 122] Aphanobionta Novak, 1930 [ 123] Acytota Jeffrey, 1971 [ 124] Acellularia [ 125] [ 126]
–У–Њ–ї–Њ–≤–љ–Є–Љ –Ј–∞–≤–і–∞–љ–љ—П–Љ –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—Ч —Ф –Њ–њ–Є—Б —А—Ц–Ј–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Ц –≥—А—Г–њ—Г–≤–∞–љ–љ—П —Ч—Е –љ–∞ –њ—Ц–і—Б—В–∞–≤—Ц —Б–њ—Ц–ї—М–љ–Є—Е –≤–ї–∞—Б—В–Є–≤–Њ—Б—В–µ–є. 1962 —А–Њ–Ї—Г –Р–љ–і—А–µ –Ы—М–≤–Њ–≤ , –†–Њ–±–µ—А—В –У–Њ—А–љ —Ц –Я–∞—Г–ї—М –Ґ—Г—А–љ—М—Ф [en] –Ы—Ц–љ–љ–µ—Ч–≤—Б—М–Ї–Њ—Ч —Ц—Ф—А–∞—А—Е—Ц—З–љ–Њ—Ч —Б–Є—Б—В–µ–Љ–Є[ 127] —В–∞–Ї—Б–Њ–љ–∞–Љ–Є –≤ —Ж—Ц–є —Б–Є—Б—В–µ–Љ—Ц —Ф —В–Є–њ , –Ї–ї–∞—Б , —А—П–і , —А–Њ–і–Є–љ–∞ , —А—Ц–і —Ц –≤–Є–і . –Т—Ц—А—Г—Б–Є –±—Г–ї–Њ —А–Њ–Ј–і—Ц–ї–µ–љ–Њ –љ–∞ –≥—А—Г–њ–Є –Ј–∞ –Ј–∞–≥–∞–ї—М–љ–Є–Љ–Є –≤–ї–∞—Б—В–Є–≤–Њ—Б—В—П–Љ–Є (–∞–ї–µ –љ–µ –≤–ї–∞—Б—В–Є–≤–Њ—Б—В—П–Љ–Є —Ч—Е–љ—Ц—Е —Е–∞–Ј—П—Ч–≤) —Ц —В–Є–њ–Њ–Љ –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Є—Е –Ї–Є—Б–ї–Њ—В —Г –≥–µ–љ–Њ–Љ–∞—Е [ 128] –Ь—Ц–ґ–љ–∞—А–Њ–і–љ–Є–є –Ї–Њ–Љ—Ц—В–µ—В –Ј —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—Ч –≤—Ц—А—Г—Б—Ц–≤ . –Ю–і–љ–∞–Ї —Г —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—Ч –≤—Ц—А—Г—Б—Ц–≤ –љ–µ –Ј–∞—Б—В–Њ—Б–Њ–≤—Г—О—В—М –њ–Њ–љ—П—В—В—П ¬Ђ—Ж–∞—А—Б—В–≤–Њ¬ї, ¬Ђ–≤—Ц–і–і—Ц–ї¬ї —Ц ¬Ђ–Ї–ї–∞—Б¬ї, –Њ—Б–Ї—Ц–ї—М–Ї–Є —Ч—Е–љ—Ц–є –Љ–∞–ї–Є–є —А–Њ–Ј–Љ—Ц—А –≥–µ–љ–Њ–Љ—Г —Ц –≤–Є—Б–Њ–Ї–∞ —З–∞—Б—В–Њ—В–∞ –Љ—Г—В–∞—Ж—Ц–є —Г—Б–Ї–ї–∞–і–љ—О—Ф –Ј'—П—Б—Г–≤–∞–љ–љ—П —Б–њ–Њ—А—Ц–і–љ–µ–љ–Њ—Б—В—Ц –≥—А—Г–њ —Б—В–∞—А—И–Є—Е –Ј–∞ –њ–Њ—А—П–і–Њ–Ї. –Я–Њ —Б—Г—В—Ц, –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—П –≤—Ц—А—Г—Б—Ц–≤ –Ј–∞ –С–∞–ї—В—Ц–Љ–Њ—А–Њ–Љ —Ф –і–Њ–њ–Њ–≤–љ–µ–љ–љ—П–Љ —В—А–∞–і–Є—Ж—Ц–є–љ—Ц—И–Њ—Ч –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—Ч.
–°–Є—Б—В–µ–Љ–∞—В–Є–Ї—Г —В–∞ —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—О –≤—Ц—А—Г—Б—Ц–≤ –љ–Є–љ—Ц –Ї–Њ–і–Є—Д—Ц–Ї—Г—Ф —Ц –њ—Ц–і—В—А–Є–Љ—Г—Ф –Ь—Ц–ґ–љ–∞—А–Њ–і–љ–Є–є –Ї–Њ–Љ—Ц—В–µ—В –Ј —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—Ч –≤—Ц—А—Г—Б—Ц–≤ (International Committee on Taxonomy of Viruses, ICTV), —Й–Њ –њ—Ц–і—В—А–Є–Љ—Г—Ф —В–∞–Ї–Њ–ґ —Ц —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—З–љ—Г –±–∞–Ј—Г The Universal Virus Database ICTVdB.
–Ь—Ц–ґ–љ–∞—А–Њ–і–љ–Є–є –Ї–Њ–Љ—Ц—В–µ—В –Ј —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—Ч –≤—Ц—А—Г—Б—Ц–≤ —А–Њ–Ј—А–Њ–±–Є–≤ —Б—Г—З–∞—Б–љ—Г –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—О –≤—Ц—А—Г—Б—Ц–≤ —Ц –≤–Є–і—Ц–ї–Є–≤ –Њ—Б–љ–Њ–≤–љ—Ц –≤–ї–∞—Б—В–Є–≤–Њ—Б—В—Ц –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –Љ–∞—О—В—М –±—Ц–ї—М—И—Г –≤–∞–≥—Г –і–ї—П –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—Ч –Ј—Ц –Ј–±–µ—А–µ–ґ–µ–љ–љ—П–Љ –Њ–і–љ–Њ–Љ–∞–љ—Ц—В–љ–Њ—Б—В—Ц —А–Њ–і–Є–љ.
–†–Њ–Ј—А–Њ–±–ї–µ–љ–Њ –Њ–±'—Ф–і–љ–∞–љ—Г —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—О (—Г–љ—Ц–≤–µ—А—Б–∞–ї—М–љ—Г —Б–Є—Б—В–µ–Љ—Г –і–ї—П –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—Ч –≤—Ц—А—Г—Б—Ц–≤). –°—М–Њ–Љ–Є–є –Ј–≤—Ц—В ICTV –Ј–∞–Ї—А—Ц–њ–Є–≤ –і–ї—П –њ–Њ—З–∞—В–Ї—Г –њ–Њ–љ—П—В—В—П –њ—А–Њ –≤–Є–і –≤—Ц—А—Г—Б—Г —П–Ї –њ—А–Њ –љ–∞–є–љ–Є–ґ—З–Є–є —В–∞–Ї—Б–Њ–љ –≤ —Ц—Ф—А–∞—А—Е—Ц—Ч –≤—Ц—А—Г—Б—Ц–≤. –Ю–і–љ–∞–Ї –і–Њ—В–µ–њ–µ—А –≤–Є–≤—З–µ–љ–Њ –ї–Є—И–µ –љ–µ–≤–µ–ї–Є–Ї—Г —З–∞—Б—В–Є–љ—Г –≤—Ц–і –Ј–∞–≥–∞–ї—М–љ–Њ–≥–Њ —А—Ц–Ј–љ–Њ–Љ–∞–љ—Ц—В—В—П –≤—Ц—А—Г—Б—Ц–≤, –∞–љ–∞–ї—Ц–Ј –Ј—А–∞–Ј–Ї—Ц–≤ –≤—Ц—А—Г—Б—Ц–≤ –Ј –ї—О–і—Б—М–Ї–Њ–≥–Њ –Њ—А–≥–∞–љ—Ц–Ј–Љ—Г –≤–Є—П–≤–Є–≤, —Й–Њ –±–ї–Є–Ј—М–Ї–Њ 20 % –њ–Њ—Б–ї—Ц–і–Њ–≤–љ–Њ—Б—В–µ–є –≤—Ц—А—Г—Б–љ–Є—Е –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Є—Е –Ї–Є—Б–ї–Њ—В —Й–µ –љ–µ –±—Г–ї–Њ —А–Њ–Ј–≥–ї—П–љ—Г—В–Њ —А–∞–љ—Ц—И–µ, –∞ –Ј—А–∞–Ј–Ї–Є –Ј –љ–∞–≤–Ї–Њ–ї–Є—И–љ—М–Њ–≥–Њ —Б–µ—А–µ–і–Њ–≤–Є—Й–∞, –љ–∞–њ—А–Є–Ї–ї–∞–і, –Љ–Њ—А—Б—М–Ї–Њ—Ч –≤–Њ–і–Є —Ц –Њ–Ї–µ–∞–љ—Б—М–Ї–Њ–≥–Њ –і–љ–∞, –њ–Њ–Ї–∞–Ј–∞–ї–Є, —Й–Њ –њ–µ—А–µ–≤–∞–ґ–љ–∞ –±—Ц–ї—М—И—Ц—Б—В—М –њ–Њ—Б–ї—Ц–і–Њ–≤–љ–Њ—Б—В–µ–є —Ф –∞–±—Б–Њ–ї—О—В–љ–Њ –љ–Њ–≤–Є–Љ–Є[ 130]
–Ю—Б–љ–Њ–≤–љ–Є–Љ–Є —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—З–љ–Є–Љ–Є –Њ–і–Є–љ–Є—Ж—П–Љ–Є —Ф[ 131]
–†—П–і (-virales )
–†–Њ–і–Є–љ–∞ (-viridae )
–Я—Ц–і—А–Њ–і–Є–љ–∞ (-virinae )
–†—Ц–і (-virus )
–Т–Є–і (-virus )–°—Г—З–∞—Б–љ–∞ –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—П ICTV (2017 —А–Њ–Ї—Г) –Љ—Ц—Б—В–Є—В—М 9 –њ–Њ—А—П–і–Ї—Ц–≤ –≤—Ц—А—Г—Б—Ц–≤: Bunyavirales [en] Caudovirales Herpesvirales [en] Ligamenvirales [en] Mononegavirales Nidovirales Ortervirales Picornavirales Tymovirales [en] Megavirales [en] [ 132] –њ—Ц–і–≤–Є–і–Є , —И—В–∞–Љ–Є —В–∞ —Ц–Ј–Њ–ї—П—В–Є . –Ч–∞–≥–∞–ї–Њ–Љ –љ–∞–ї—Ц—З—Г—Ф—В—М—Б—П 9 –њ–Њ—А—П–і–Ї—Ц–≤, 127 —А–Њ–і–Є–љ, 44 –њ—Ц–і—А–Њ–і–Є–љ–Є, 782 —А–Њ–і–Є, 4686 –≤–Є–і—Ц–≤[ 133] [ 134]
–У—А—Г–њ–Є –≤—Ц—А—Г—Б—Ц–≤ –Ј–∞ –С–∞–ї—В—Ц–Љ–Њ—А–Њ–Љ. –£–Љ–Њ–≤–љ—Ц –њ–Њ–Ј–љ–∞—З–µ–љ–љ—П: –Њ–ї вАФ –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–∞, –і–ї вАФ –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–∞, –†–Ґ вАФ —А–µ—В—А–Њ–≤—Ц—А—Г—Б –∞–±–Њ —А–µ—В—А–Њ—Ч–і–љ–Є–є –≤—Ц—А—Г—Б –Ы–∞—Г—А–µ–∞—В –Э–Њ–±–µ–ї—Ц–≤—Б—М–Ї–Њ—Ч –њ—А–µ–Љ—Ц—Ч –±—Ц–Њ–ї–Њ–≥ –Ф–µ–≤—Ц–і –С–∞–ї—В—Ц–Љ–Њ—А —А–Њ–Ј—А–Њ–±–Є–≤ –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—О –≤—Ц—А—Г—Б—Ц–≤ –Ј–∞ –С–∞–ї—В—Ц–Љ–Њ—А–Њ–Љ[ 29] [ 135] [ 136] [ 137]
–Ъ–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—П –≤—Ц—А—Г—Б—Ц–≤ –Ј–∞ –С–∞–ї—В—Ц–Љ–Њ—А–Њ–Љ “С—А—Г–љ—В—Г—Ф—В—М—Б—П –љ–∞ –Љ–µ—Е–∞–љ—Ц–Ј–Љ—Ц —Г—В–≤–Њ—А–µ–љ–љ—П –Љ–†–Э–Ъ. –Т—Ц—А—Г—Б–Є –Љ–∞—О—В—М —Б–Є–љ—В–µ–Ј—Г–≤–∞—В–Є –Љ–†–Э–Ъ –Ј –≤–ї–∞—Б–љ–Є—Е –≥–µ–љ–Њ–Љ—Ц–≤ –і–ї—П —Г—В–≤–Њ—А–µ–љ–љ—П –±—Ц–ї–Ї—Ц–≤ —Ц —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—Ч —Б–≤–Њ—Ф—Ч –љ—Г–Ї–ї–µ—Ч–љ–Њ–≤–Њ—Ч –Ї–Є—Б–ї–Њ—В–Є, –Њ–і–љ–∞–Ї –Ї–Њ–ґ–љ–∞ —А–Њ–і–Є–љ–∞ –≤—Ц—А—Г—Б—Ц–≤ –Љ–∞—Ф –≤–ї–∞—Б–љ–Є–є –Љ–µ—Е–∞–љ—Ц–Ј–Љ –Ј–і—Ц–є—Б–љ–µ–љ–љ—П —Ж—М–Њ–≥–Њ. –Т—Ц—А—Г—Б–љ—Ц –≥–µ–љ–Њ–Љ–Є –±—Г–≤–∞—О—В—М –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є–Љ–Є (–Њ–ї) –∞–±–Њ –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є–Љ–Є (–і–ї), –Ф–Э–Ъ вАФ –∞–±–Њ –†–Э–Ъ-–≤–Љ—Ц—Б–љ–Є–Љ–Є, –Љ–Њ–ґ—Г—В—М –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞—В–Є –∞–±–Њ –љ–µ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞—В–Є –Ј–≤–Њ—А–Њ—В–љ—Г —В—А–∞–љ—Б–Ї—А–Є–њ—В–∞–Ј—Г . –Ъ—А—Ц–Љ —В–Њ–≥–Њ, –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Ц –†–Э–Ъ-–≤—Ц—А—Г—Б–Є –Љ–Њ–ґ—Г—В—М –Љ–∞—В–Є –њ–Њ–Ј–Є—В–Є–≤–љ–Є–є (+) –∞–±–Њ –љ–µ–≥–∞—В–Є–≤–љ–Є–є (-) –ї–∞–љ—Ж—О–≥ –†–Э–Ъ —Г —Б–Ї–ї–∞–і—Ц —Б–≤–Њ–≥–Њ –≥–µ–љ–Њ–Љ—Г.
–¶—П —Б–Є—Б—В–µ–Љ–∞ –Љ—Ц—Б—В–Є—В—М —Б—Ц–Љ –Њ—Б–љ–Њ–≤–љ–Є—Е –≥—А—Г–њ[ 138] [ 139]
(I) –Т—Ц—А—Г—Б–Є, —Й–Њ –Љ—Ц—Б—В—П—В—М –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –Ф–Э–Ъ —Ц –љ–µ –Љ–∞—О—В—М –†–Э–Ъ-—Б—В–∞–і—Ц—Ч (–љ–∞–њ—А–Є–Ї–ї–∞–і, –≥–µ—А–њ–µ—Б–≤—Ц—А—Г—Б–Є , –њ–Њ–Ї—Б–≤—Ц—А—Г—Б–Є , –њ–∞–њ–Њ–≤–∞–≤—Ц—А—Г—Б–Є [en] –Љ—Ц–Љ—Ц–≤—Ц—А—Г—Б ).
(II) –Т—Ц—А—Г—Б–Є, —Й–Њ –Љ—Ц—Б—В—П—В—М –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –Љ–Њ–ї–µ–Ї—Г–ї—Г –Ф–Э–Ъ (–љ–∞–њ—А–Є–Ї–ї–∞–і, –њ–∞—А–≤–Њ–≤—Ц—А—Г—Б–Є [en]
(III) –Т—Ц—А—Г—Б–Є, —Й–Њ –Љ—Ц—Б—В—П—В—М –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –†–Э–Ъ (–љ–∞–њ—А–Є–Ї–ї–∞–і, —А–Њ—В–∞–≤—Ц—А—Г—Б–Є ).
(IV) –Т—Ц—А—Г—Б–Є, —Й–Њ –Љ—Ц—Б—В—П—В—М –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –Љ–Њ–ї–µ–Ї—Г–ї—Г –†–Э–Ъ –њ–Њ–Ј–Є—В–Є–≤–љ–Њ—Ч –њ–Њ–ї—П—А–љ–Њ—Б—В—Ц (–љ–∞–њ—А–Є–Ї–ї–∞–і, –њ—Ц–Ї–Њ—А–љ–∞–≤—Ц—А—Г—Б–Є , —Д–ї–∞–≤—Ц–≤—Ц—А—Г—Б–Є [en]
(V) –Т—Ц—А—Г—Б–Є, —Й–Њ –Љ—Ц—Б—В—П—В—М –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –Љ–Њ–ї–µ–Ї—Г–ї—Г –†–Э–Ъ –љ–µ–≥–∞—В–Є–≤–љ–Њ—Ч –∞–±–Њ –њ–Њ–і–≤—Ц–є–љ–Њ—Ч –њ–Њ–ї—П—А–љ–Њ—Б—В—Ц (–љ–∞–њ—А–Є–Ї–ї–∞–і, –Њ—А—В–Њ–Љ—Ц–Ї—Б–Њ–≤—Ц—А—Г—Б–Є , —Д—Ц–ї–Њ–≤—Ц—А—Г—Б–Є ).
(VI) –Т—Ц—А—Г—Б–Є, —Й–Њ –Љ—Ц—Б—В—П—В—М –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –Љ–Њ–ї–µ–Ї—Г–ї—Г –†–Э–Ъ –њ–Њ–Ј–Є—В–Є–≤–љ–Њ—Ч –њ–Њ–ї—П—А–љ–Њ—Б—В—Ц —Ц –Љ–∞—О—В—М —Г —Б–≤–Њ—Ф–Љ—Г –ґ–Є—В—В—Ф–≤–Њ–Љ—Г —Ж–Є–Ї–ї—Ц —Б—В–∞–і—Ц—О —Б–Є–љ—В–µ–Ј—Г –Ф–Э–Ъ –љ–∞ –Љ–∞—В—А–Є—Ж—Ц –†–Э–Ъ, —А–µ—В—А–Њ–≤—Ц—А—Г—Б–Є (–љ–∞–њ—А–Є–Ї–ї–∞–і, –Т–Ж–Ы ).
(VII) –Т—Ц—А—Г—Б–Є, —Й–Њ –Љ—Ц—Б—В—П—В—М —З–∞—Б—В–Ї–Њ–≤–Њ –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г, —З–∞—Б—В–Ї–Њ–≤–Њ –Њ–і–љ–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –Ф–Э–Ъ[ 140] [ 141] —А–µ—В—А–Њ—Ч–і–љ—Ц –≤—Ц—А—Г—Б–Є (–љ–∞–њ—А–Є–Ї–ї–∞–і, –≤—Ц—А—Г—Б –≥–µ–њ–∞—В–Є—В—Г B )[ 142] –Я–Њ–і–∞–ї—М—И–Є–є –њ–Њ–і—Ц–ї –Ј–і—Ц–є—Б–љ—О—О—В—М –љ–∞ –Њ—Б–љ–Њ–≤—Ц —В–∞–Ї–Є—Е –Њ–Ј–љ–∞–Ї —П–Ї —Б—В—А—Г–Ї—В—Г—А–∞ –≥–µ–љ–Њ–Љ—Г (–љ–∞—П–≤–љ—Ц—Б—В—М —Б–µ–≥–Љ–µ–љ—В—Ц–≤, –Ї—Ц–ї—М—Ж–µ–≤–∞ –∞–±–Њ –ї—Ц–љ—Ц–є–љ–∞ –Љ–Њ–ї–µ–Ї—Г–ї–∞), –≥–µ–љ–µ—В–Є—З–љ–∞ —Б—Е–Њ–ґ—Ц—Б—В—М –Ј —Ц–љ—И–Є–Љ–Є –≤—Ц—А—Г—Б–∞–Љ–Є, –љ–∞—П–≤–љ—Ц—Б—В—М –ї—Ц–њ—Ц–і–љ–Њ—Ч –Њ–±–Њ–ї–Њ–љ–Ї–Є, —В–∞–Ї—Б–Њ–љ–Њ–Љ—Ц—З–љ–∞ –љ–∞–ї–µ–ґ–љ—Ц—Б—В—М –Њ—А–≥–∞–љ—Ц–Ј–Љ—Г-—Е–∞–Ј—П—Ч–љ—Г —В–Њ—Й–Њ.
–Ю—Б–љ–Њ–≤–љ—Ц –≤—Ц—А—Г—Б–љ—Ц —Ц–љ—Д–µ–Ї—Ж—Ц—Ч –ї—О–і–Є–љ–Є —В–∞ —Ч—Е–љ—Ц –Ј–±—Г–і–љ–Є–Ї–Є –Я—А–Є–Ї–ї–∞–і–∞–Љ–Є –љ–∞–є–≤—Ц–і–Њ–Љ—Ц—И–Є—Е –≤—Ц—А—Г—Б–љ–Є—Е –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ—М –ї—О–і–Є–љ–Є —Ф –Ј–∞—Б—В—Г–і–∞ (–≤–Њ–љ–∞ –Љ–Њ–ґ–µ –Љ–∞—В–Є –є –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ—Г –µ—В—Ц–Њ–ї–Њ–≥—Ц—О ), –≥—А–Є–њ , –≤—Ц—В—А—П–љ–∞ –≤—Ц—Б–њ–∞ —Ц –њ—А–Њ—Б—В–Є–є –≥–µ—А–њ–µ—Б . –С–∞–≥–∞—В–Њ —В—П–ґ–Ї–Є—Е —Е–≤–Њ—А–Њ–±, –љ–∞–њ—А–Є–Ї–ї–∞–і, —Е–≤–Њ—А–Њ–±–∞, —П–Ї—Г —Б–њ—А–Є—З–Є–љ—О—Ф –≤—Ц—А—Г—Б –Х–±–Њ–ї–∞ , –Т–Ж–Ы/–°–Э–Ж–Ф , –њ—В–∞—И–Є–љ–Є–є –≥—А–Є–њ —Ц —В—П–ґ–Ї–Є–є –≥–Њ—Б—В—А–Є–є —А–µ—Б–њ—Ц—А–∞—В–Њ—А–љ–Є–є —Б–Є–љ–і—А–Њ–Љ —Б–њ—А–Є—З–Є–љ—П—О—В—М—Б—П –≤—Ц—А—Г—Б–∞–Љ–Є. –Т—Ц–і–љ–Њ—Б–љ–∞ –Ј–і–∞—В–љ—Ц—Б—В—М –≤—Ц—А—Г—Б—Г —Б–њ—А–Є—З–Є–љ—П—В–Є –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—Ф—В—М—Б—П —В–µ—А–Љ—Ц–љ–Њ–Љ –≤—Ц—А—Г–ї–µ–љ—В–љ—Ц—Б—В—М . –Ф–µ—П–Ї—Ц –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П –і–Њ—Б–ї—Ц–і–ґ—Г—О—В—М –љ–∞ –љ–∞—П–≤–љ—Ц—Б—В—М –≤—Ц—А—Г—Б—Ц–≤ —Б–µ—А–µ–і —З–Є–љ–љ–Є–Ї—Ц–≤, –љ–∞–њ—А–Є–Ї–ї–∞–і, –Љ–Њ–ґ–ї–Є–≤–Є–є –Ј–≤'—П–Ј–Њ–Ї –Љ—Ц–ґ –ї—О–і—Б—М–Ї–Є–Љ –≥–µ—А–њ–µ—Б–≤—Ц—А—Г—Б–Њ–Љ 6-–≥–Њ —В–Є–њ—Г [en] –љ–µ–є—А–Њ–ї–Њ–≥—Ц—З–љ–Є–Љ–Є –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П–Љ–Є, —П–Ї-–Њ—В —А–Њ–Ј—Б—Ц—П–љ–Є–є —Б–Ї–ї–µ—А–Њ–Ј —Ц —Б–Є–љ–і—А–Њ–Љ —Е—А–Њ–љ—Ц—З–љ–Њ—Ч –≤—В–Њ–Љ–Є [ 143] –±–Њ—А–љ–∞–≤—Ц—А—Г—Б [en] [ 144]
–Т—Ц—А—Г—Б–Є –Љ–∞—О—В—М —А—Ц–Ј–љ—Ц –Љ–µ—Е–∞–љ—Ц–Ј–Љ–Є, —Й–Њ —Б–њ—А–Є—З–Є–љ—О—О—В—М —Е–≤–Њ—А–Њ–±—Г —Г —Е–∞–Ј—П—Ч–љ–∞, —Ц —Ж—Ц –Љ–µ—Е–∞–љ—Ц–Ј–Љ–Є —Б–Є–ї—М–љ–Њ –Ј–∞–ї–µ–ґ–∞—В—М –≤—Ц–і –≤–Є–і—Г. –Ґ–∞–Ї–Є–є –Љ–µ—Е–∞–љ—Ц–Ј–Љ –љ–∞ –Ї–ї—Ц—В–Є–љ–љ–Њ–Љ—Г —А—Ц–≤–љ—Ц –≤–Ї–ї—О—З–∞—Ф –љ–∞—Б–∞–Љ–њ–µ—А–µ–і –ї—Ц–Ј–Є—Б –Ї–ї—Ц—В–Є–љ, —Й–Њ –њ—А–Є–Ј–≤–Њ–і–Є—В—М –і–Њ —Ч—Е–љ—М–Њ—Ч —Б–Љ–µ—А—В—Ц. –£ –±–∞–≥–∞—В–Њ–Ї–ї—Ц—В–Є–љ–љ–Є—Е –Њ—А–≥–∞–љ—Ц–Ј–Љ—Ц–≤ –њ—Ц—Б–ї—П –Ј–∞–≥–Є–±–µ–ї—Ц –Ј–љ–∞—З–љ–Њ—Ч –Ї—Ц–ї—М–Ї–Њ—Б—В—Ц –Ї–ї—Ц—В–Є–љ –њ–Њ—З–Є–љ–∞—Ф —Б—В—А–∞–ґ–і–∞—В–Є –Њ—А–≥–∞–љ—Ц–Ј–Љ —Г —Ж—Ц–ї–Њ–Љ—Г. –•–Њ—З–∞ –≤—Ц—А—Г—Б–Є –њ—Ц–і—А–Є–≤–∞—О—В—М –љ–Њ—А–Љ–∞–ї—М–љ–Є–є –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј , –њ—А–Є–Ј–≤–Њ–і—П—З–Є –і–Њ –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П, –≤–Њ–љ–Є –Љ–Њ–ґ—Г—В—М —Ц—Б–љ—Г–≤–∞—В–Є –≤—Б–µ—А–µ–і–Є–љ—Ц –Њ—А–≥–∞–љ—Ц–Ј–Љ—Г —Ц –≤—Ц–і–љ–Њ—Б–љ–Њ –љ–µ—И–Ї—Ц–і–ї–Є–≤–Њ. –ѓ–Ї –њ—А–Є–Ї–ї–∞–і –Љ–Њ–ґ–љ–∞ –љ–∞–≤–µ—Б—В–Є –Ј–і–∞—В–љ—Ц—Б—В—М –≤—Ц—А—Г—Б—Г –њ—А–Њ—Б—В–Њ–≥–Њ –≥–µ—А–њ–µ—Б—Г –њ–µ—А—И–Њ–≥–Њ —В–Є–њ—Г –њ–µ—А–µ–±—Г–≤–∞—В–Є –≤ —Б—В–∞–љ—Ц —Б–њ–Њ–Ї–Њ—О –≤—Б–µ—А–µ–і–Є–љ—Ц —В—Ц–ї–∞ –ї—О–і–Є–љ–Є. –Ґ–∞–Ї–Є–є —Б—В–∞–љ –љ–∞–Ј–Є–≤–∞—О—В—М –ї–∞—В–µ–љ—В–љ—Ц—Б—В—О [ 145] –≤—Ц—А—Г—Б—Ц–≤ –≥–µ—А–њ–µ—Б—Г , —Г —В–Њ–Љ—Г —З–Є—Б–ї—Ц –≤—Ц—А—Г—Б—Г –Х–њ—И—В–µ–є–љ–∞ вАФ –С–∞—А—А , —Й–Њ —Б–њ—А–Є—З–Є–љ—О—Ф —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є–є –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–Њ–Ј , –∞ —В–∞–Ї–Њ–ґ –≤—Ц—А—Г—Б—Г, —П–Ї–Є–є —Б–њ—А–Є—З–Є–љ—П—Ф –≤—Ц—В—А—П–љ–Ї—Г —Ц –Њ–њ–µ—А—Ц–Ј—Г–≤–∞–ї—М–љ–Є–є –≥–µ—А–њ–µ—Б . –С—Ц–ї—М—И—Ц—Б—В—М –ї—О–і–µ–є –њ–µ—А–µ—Е–≤–Њ—А—Ц–ї–Є –њ—А–Є–љ–∞–є–Љ–љ—Ц –Њ–і–љ–Є–Љ –Ј —Ж–Є—Е —В–Є–њ—Ц–≤ –≤—Ц—А—Г—Б—Г –≥–µ—А–њ–µ—Б—Г[ 146] –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Є—Е –њ–∞—В–Њ–≥–µ–љ—Ц–≤ , –љ–∞–њ—А–Є–Ї–ї–∞–і, —З—Г–Љ–љ–Њ—Ч –њ–∞–ї–Є—З–Ї–Є Yersinia pestis [ 147]
–Ф–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є –Љ–Њ–ґ—Г—В—М —Б–њ—А–Є—З–Є–љ–Є—В–Є –і–Њ–≤—Ц—З–љ—Ц –∞–±–Њ —Е—А–Њ–љ—Ц—З–љ—Ц —Ц–љ—Д–µ–Ї—Ж—Ц—Ч , –Ї–Њ–ї–Є –≤—Ц—А—Г—Б —Ц –і–∞–ї—Ц —А–Њ–Ј–Љ–љ–Њ–ґ—Г—Ф—В—М—Б—П –≤ —В—Ц–ї—Ц –Њ—А–≥–∞–љ—Ц–Ј–Љ—Г, –њ–Њ–њ—А–Є –є–Њ–≥–Њ –Ј–∞—Е–Є—Б–љ—Ц –Љ–µ—Е–∞–љ—Ц–Ј–Љ–Є[ 148] –≥–µ–њ–∞—В–Є—В—Г B —Ц C . –•—А–Њ–љ—Ц—З–љ–Њ —Е–≤–Њ—А–Є—Е –ї—О–і–µ–є –љ–∞–Ј–Є–≤–∞—О—В—М –љ–Њ—Б—Ц—П–Љ–Є, –Њ—Б–Ї—Ц–ї—М–Ї–Є –≤–Њ–љ–Є –≤–Є—Б—В—Г–њ–∞—О—В—М —Г —А–Њ–ї—Ц —А–µ–Ј–µ—А–≤—Г–∞—А–∞ –і–ї—П –Ј–∞—А–∞–Ј–љ–Њ–≥–Њ –≤—Ц—А—Г—Б—Г[ 149] –њ–Њ–њ—Г–ї—П—Ж—Ц—Ч —Ф –≤–Є—Б–Њ–Ї–∞ —З–∞—Б—В–Ї–∞ –љ–Њ—Б—Ц—Ч–≤, —В–Њ —Г —Ж—М–Њ–Љ—Г –≤–Є–њ–∞–і–Ї—Г –Ї–∞–ґ—Г—В—М –њ—А–Њ –µ–њ—Ц–і–µ–Љ—Ц—О [ 150]
–Т—Ц—А—Г—Б–љ–∞ –µ–њ—Ц–і–µ–Љ—Ц–Њ–ї–Њ–≥—Ц—П —Ф —З–∞—Б—В–Є–љ–Њ—О –Љ–µ–і–Є—З–љ–Њ—Ч –љ–∞—Г–Ї–Є, —П–Ї–∞ –≤–Є–≤—З–∞—Ф –њ–µ—А–µ–і–∞–≤–∞–љ–љ—П —В–∞ –Ї–Њ–љ—В—А–Њ–ї—М –≤—Ц—А—Г—Б–љ–Є—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є —Б–µ—А–µ–і –ї—О–і–µ–є. –Я–µ—А–µ–і–∞–≤–∞–љ–љ—П –≤—Ц—А—Г—Б—Ц–≤ –Љ–Њ–ґ–µ –Ј–і—Ц–є—Б–љ—О–≤–∞—В–Є—Б—П –≤–µ—А—В–Є–Ї–∞–ї—М–љ–Њ, —В–Њ–±—В–Њ –≤—Ц–і –Љ–∞—В–µ—А—Ц –і–Њ –і–Є—В–Є–љ–Є, –∞–±–Њ –≥–Њ—А–Є–Ј–Њ–љ—В–∞–ї—М–љ–Њ, —В–Њ–±—В–Њ –≤—Ц–і –ї—О–і–Є–љ–Є –і–Њ –ї—О–і–Є–љ–Є. –Я—А–Є–Ї–ї–∞–і–∞–Љ–Є –≤–µ—А—В–Є–Ї–∞–ї—М–љ–Њ—Ч –њ–µ—А–µ–і–∞—З—Ц —Ф –≤—Ц—А—Г—Б –≥–µ–њ–∞—В–Є—В—Г B —Ц –Т–Ж–Ы , –Ї–Њ–ї–Є –Љ–∞–ї—О–Ї –љ–∞—А–Њ–і–ґ—Г—Ф—В—М—Б—П –≤–ґ–µ –Ј–∞—А–∞–ґ–µ–љ–Є–Љ[ 151] [ 152]
–У–Њ—А–Є–Ј–Њ–љ—В–∞–ї—М–љ–∞ –њ–µ—А–µ–і–∞—З–∞ [en] –љ–Њ—А–Њ–≤—Ц—А—Г—Б—Г ; –Ї–Њ–ї–Є –≤–і–Є—Е–∞—Ф—В—М—Б—П –њ–Њ–≤—Ц—В—А—П, –≤ —П–Ї–Њ–Љ—Г —Ф –≤—Ц—А—Ц–Њ–љ–Є , –љ–∞–њ—А–Є–Ї–ї–∞–і, –≤—Ц—А—Г—Б –≥—А–Є–њ—Г; –Ї–Њ–Љ–∞—Е–∞–Љ–Є, –љ–∞–њ—А–Є–Ї–ї–∞–і, –Ї–Њ–Љ–∞—А–∞–Љ–Є, —П–Ї—Ц —Г—И–Ї–Њ–і–ґ—Г—О—В—М —И–Ї—Ц—А—Г —Е–∞–Ј—П—Ч–љ–∞, –љ–∞–њ—А–Є–Ї–ї–∞–і, –≥–∞—А—П—З–Ї–∞ –і–µ–љ–≥–µ . –®–≤–Є–і–Ї—Ц—Б—В—М –њ–µ—А–µ–і–∞—З—Ц –≤—Ц—А—Г—Б–љ–Њ—Ч —Ц–љ—Д–µ–Ї—Ж—Ц—Ч –Ј–∞–ї–µ–ґ–Є—В—М –≤—Ц–і –Ї—Ц–ї—М–Ї–Њ—Е —Д–∞–Ї—В–Њ—А—Ц–≤, –і–Њ —П–Ї–Є—Е –≤—Ц–і–љ–Њ—Б—П—В—М —Й—Ц–ї—М–љ—Ц—Б—В—М –њ–Њ–њ—Г–ї—П—Ж—Ц—Ч, –Ї—Ц–ї—М–Ї—Ц—Б—В—М —З—Г—В–ї–Є–≤–Є—Е –ї—О–і–µ–є (—В–Њ–±—В–Њ —В–∞–Ї–Є—Е, —Й–Њ –љ–µ –Љ–∞—О—В—М —Ц–Љ—Г–љ—Ц—В–µ—В—Г )[ 153] [ 154]
–Х–њ—Ц–і–µ–Љ—Ц–Њ–ї–Њ–≥—Ц—О –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М, –∞–±–Є –њ—А–Є–Ј—Г–њ–Є–љ–Є—В–Є –њ–Њ—И–Є—А–µ–љ–љ—П —Ц–љ—Д–µ–Ї—Ж—Ц—Ч –≤ –њ–Њ–њ—Г–ї—П—Ж—Ц—Ч –њ—Ц–і —З–∞—Б —Б–њ–∞–ї–∞—Е—Г –≤—Ц—А—Г—Б–љ–Њ–≥–Њ –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П. –†–Њ–±–ї—П—В—М –Ї–Њ–љ—В—А–Њ–ї—М–љ—Ц –Ј–∞—Е–Њ–і–Є, –Њ—Б–љ–Њ–≤–∞–љ—Ц –љ–∞ –Ј–љ–∞–љ–љ—Ц —В–Њ–≥–Њ, —П–Ї –њ–Њ—И–Є—А—О—Ф—В—М—Б—П –≤—Ц—А—Г—Б. –Т–∞–ґ–ї–Є–≤–Њ –Ј–љ–∞–є—В–Є –і–ґ–µ—А–µ–ї–Њ (–∞–±–Њ –і–ґ–µ—А–µ–ї–∞) —Б–њ–∞–ї–∞—Е—Г —В–∞ —Ц–і–µ–љ—В–Є—Д—Ц–Ї—Г–≤–∞—В–Є –≤—Ц—А—Г—Б. –Ъ–Њ–ї–Є –≤—Ц—А—Г—Б –≤–Є–Ј–љ–∞—З–µ–љ–Њ, –±—Г–≤–∞—Ф –Љ–Њ–ґ–ї–Є–≤–Є–Љ –Ј—Г–њ–Є–љ–Є—В–Є —Ц–љ—Д–µ–Ї—Ж—Ц—О –Ј–∞ –і–Њ–њ–Њ–Љ–Њ–≥–Њ—О –≤–∞–Ї—Ж–Є–љ . –ѓ–Ї—Й–Њ –≤–∞–Ї—Ж–Є–љ–Є –љ–µ–і–Њ—Б—В—Г–њ–љ—Ц, –Љ–Њ–ґ—Г—В—М –±—Г—В–Є –µ—Д–µ–Ї—В–Є–≤–љ–Є–Љ–Є —Б–∞–љ–∞—Ж—Ц—П —В–∞ –і–µ–Ј—Ц–љ—Д–µ–Ї—Ж—Ц—П . –І–∞—Б—В–Њ –Ј–∞—А–∞–ґ–µ–љ–Є—Е –ї—О–і–µ–є —Ц–Ј–Њ–ї—О—О—В—М –≤—Ц–і —А–µ—И—В–Є —Б—Г—Б–њ—Ц–ї—М—Б—В–≤–∞, —В–Њ–±—В–Њ –≤—Ц—А—Г—Б –њ–Њ–Љ—Ц—Й–∞—О—В—М —Г –Ї–∞—А–∞–љ—В–Є–љ. –©–Њ–± –≤–Ј—П—В–Є –њ—Ц–і –Ї–Њ–љ—В—А–Њ–ї—М —Б–њ–∞–ї–∞—Е —П—Й—Г—А—Г —Г –Т–µ–ї–Є–Ї—Ц–є –С—А–Є—В–∞–љ—Ц—Ч 2001 —А–Њ–Ї—Г [en] —Ц–љ–Ї—Г–±–∞—Ж—Ц–є–љ–Є–є –њ–µ—А—Ц–Њ–і , –њ—А–Њ—В—П–≥–Њ–Љ —П–Ї–Њ–≥–Њ –љ–µ –≤–Є—П–≤–ї—П—Ф—В—М—Б—П –ґ–Њ–і–љ–Є—Е —Б–Є–Љ–њ—В–Њ–Љ—Ц–≤ —Ц–љ—Д–µ–Ї—Ж—Ц—Ч. –Ж–љ–Ї—Г–±–∞—Ж—Ц–є–љ–Є–є –њ–µ—А—Ц–Њ–і –≤—Ц—А—Г—Б–љ–Є—Е –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ—М –Љ–Њ–ґ–µ —В—А–Є–≤–∞—В–Є –≤—Ц–і –Ї—Ц–ї—М–Ї–Њ—Е –і–љ—Ц–≤ –і–Њ —В–Є–ґ–љ—Ц–≤. –І–∞—Б—В–Њ –њ–µ—А–µ–Ї—А–Є–≤–∞—Ф—В—М—Б—П –Ј –љ–Є–Љ, –∞–ї–µ –њ–µ—А–µ–≤–∞–ґ–љ–Њ –є–і–µ –њ—Ц—Б–ї—П —Ц–љ–Ї—Г–±–∞—Ж—Ц–є–љ–Њ–≥–Њ –њ–µ—А—Ц–Њ–і—Г вАФ –њ–µ—А—Ц–Њ–і –њ–µ—А–µ–і–∞–≤–∞–љ–љ—П —Ц–љ—Д–µ–Ї—Ж—Ц—Ч, –Ї–Њ–ї–Є –Ј–∞—А–∞–ґ–µ–љ–∞ –ї—О–і–Є–љ–∞ —З–Є —В–≤–∞—А–Є–љ–∞ —Ф –Ј–∞—А–∞–Ј–љ–Њ—О –є –Љ–Њ–ґ–µ –Ј–∞—А–∞–Ј–Є—В–Є —Ц–љ—И–Є—Е –ї—О–і–µ–є –∞–±–Њ —В–≤–∞—А–Є–љ. –¶–µ–є –њ–µ—А—Ц–Њ–і —В–∞–Ї–Њ–ґ –≤—Ц–і–Њ–Љ–Є–є –і–ї—П –±–∞–≥–∞—В—М–Њ—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є, —Ц –Ј–љ–∞–љ–љ—П —В—А–Є–≤–∞–ї–Њ—Б—В—Ц –Њ–±–Њ—Е –њ–µ—А—Ц–Њ–і—Ц–≤ —Ф –≤–∞–ґ–ї–Є–≤–Є–Љ –і–ї—П –Ї–Њ–љ—В—А–Њ–ї—О –љ–∞–і —Б–њ–∞–ї–∞—Е–∞–Љ–Є. –ѓ–Ї—Й–Њ —Б–њ–∞–ї–∞—Е –њ—А–Є–Ј–≤–Њ–і–Є—В—М –і–Њ –љ–µ–Ј–≤–Є—З–∞–є–љ–Њ –≤–Є—Б–Њ–Ї–Њ—Ч –Ї—Ц–ї—М–Ї–Њ—Б—В—Ц –≤–Є–њ–∞–і–Ї—Ц–≤ –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П –≤ –њ–Њ–њ—Г–ї—П—Ж—Ц—Ч –∞–±–Њ —А–µ–≥—Ц–Њ–љ—Ц, —В–Њ –є–Њ–≥–Њ –љ–∞–Ј–Є–≤–∞—О—В—М –µ–њ—Ц–і–µ–Љ—Ц—Ф—О. –ѓ–Ї—Й–Њ —Б–њ–∞–ї–∞—Е–Є –њ–Њ—И–Є—А—О—О—В—М—Б—П –≤ –≥–ї–Њ–±–∞–ї—М–љ–Њ–Љ—Г –Љ–∞—Б—И—В–∞–±—Ц, —В–Њ –Ї–∞–ґ—Г—В—М –њ—А–Њ –њ–∞–љ–і–µ–Љ—Ц—О .
–Ґ—А–∞–љ—Б–Љ—Ц—Б—Ц–є–љ–∞ –µ–ї–µ–Ї—В—А–Њ–љ–љ–∞ –Љ—Ц–Ї—А–Њ—Б–Ї–Њ–њ—Ц—П –≤—Ц–і—В–≤–Њ—А–µ–љ–Њ–≥–Њ –≤—Ц—А—Г—Б—Г —Ц—Б–њ–∞–љ—Б—М–Ї–Њ–≥–Њ –≥—А–Є–њ—Г –І–Є—Б–µ–ї—М–љ—Ц—Б—В—М –Ї–Њ—А—Ц–љ–љ–Њ–≥–Њ –љ–∞—Б–µ–ї–µ–љ–љ—П –Р–Љ–µ—А–Є–Ї–Є —Б–Є–ї—М–љ–Њ –Ј–Љ–µ–љ—И–Є–ї–∞—Б—М –≤–љ–∞—Б–ї—Ц–і–Њ–Ї –Ј–∞—А–∞–Ј–љ–Є—Е –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ—М, –Ј–Њ–Ї—А–µ–Љ–∞, –≤—Ц—Б–њ–Є , —Й–Њ —Ч—Е –Ј–∞–≤–µ–Ј–ї–Є –≤ –Р–Љ–µ—А–Є–Ї—Г —Ф–≤—А–Њ–њ–µ–є—Б—М–Ї—Ц –Ї–Њ–ї–Њ–љ—Ц–Ј–∞—В–Њ—А–Є. –Ч–∞ –і–µ—П–Ї–Є–Љ–Є –Њ—Ж—Ц–љ–Ї–∞–Љ–Є, —Ц–љ–Њ–Ј–µ–Љ–љ—Ц —Е–≤–Њ—А–Њ–±–Є –њ—Ц—Б–ї—П –њ—А–Є–±—Г—В—В—П –Ъ–Њ–ї—Г–Љ–±–∞ –≤ –Р–Љ–µ—А–Є–Ї—Г, –≤–±–Є–ї–Є –±–ї–Є–Ј—М–Ї–Њ 70 % –≤—Ц–і –≤—Б—М–Њ–≥–Њ –Ї–Њ—А—Ц–љ–љ–Њ–≥–Њ –љ–∞—Б–µ–ї–µ–љ–љ—П. –Ч–±–Є—В–Ї–Є, –Ј–∞–≤–і–∞–љ—Ц —Ж–Є–Љ–Є —Е–≤–Њ—А–Њ–±–∞–Љ–Є –∞–±–Њ—А–Є–≥–µ–љ–∞–Љ, –і–Њ–њ–Њ–Љ–Њ–≥–ї–Є —Ф–≤—А–Њ–њ–µ–є—Ж—П–Љ –≤–Є—В—Ц—Б–љ–Є—В–Є —Ц –њ—Ц–і–Ї–Њ—А–Є—В–Є —Ч—Е[ 162]
–Я–∞–љ–і–µ–Љ—Ц—П вАФ —Ж–µ –µ–њ—Ц–і–µ–Љ—Ц—П —Б–≤—Ц—В–Њ–≤–Њ–≥–Њ –Љ–∞—Б—И—В–∞–±—Г. –Х–њ—Ц–і–µ–Љ—Ц—П —Ц—Б–њ–∞–љ—Б—М–Ї–Њ–≥–Њ –≥—А–Є–њ—Г 1918 —А–Њ–Ї—Г, —Й–Њ —В—А–Є–≤–∞–ї–∞ –і–Њ 1919 —А–Њ–Ї—Г, –љ–∞–ї–µ–ґ–Є—В—М –і–Њ 5-—Ч –Ї–∞—В–µ–≥–Њ—А—Ц—Ч –њ–∞–љ–і–µ–Љ—Ц–є –≤—Ц—А—Г—Б—Г –≥—А–Є–њ—Г . –З—Ч —Б–њ—А–Є—З–Є–љ–Є–≤ –љ–∞–і–Ј–≤–Є—З–∞–є–љ–Њ –∞–≥—А–µ—Б–Є–≤–љ–Є–є —Ц —Б–Љ–µ—А—В–Њ–љ–Њ—Б–љ–Є–є –≤—Ц—А—Г—Б –≥—А–Є–њ—Г A . –Щ–Њ–≥–Њ –ґ–µ—А—В–≤–∞–Љ–Є —З–∞—Б—В–Њ —Б—В–∞–≤–∞–ї–Є –Ј–і–Њ—А–Њ–≤—Ц –і–Њ—А–Њ—Б–ї—Ц –ї—О–і–Є, –љ–∞ –≤—Ц–і–Љ—Ц–љ—Г –≤—Ц–і –±—Ц–ї—М—И–Њ—Б—В—Ц —Б–њ–∞–ї–∞—Е—Ц–≤ –≥—А–Є–њ—Г, —П–Ї—Ц –≤—А–∞–ґ–∞–ї–Є –њ–µ—А–µ–≤–∞–ґ–љ–Њ –і—Ц—В–µ–є —Ц –њ—Ц–і–ї—Ц—В–Ї—Ц–≤, –ї—О–і–µ–є —Б—В–∞—А—И–Њ–≥–Њ –њ–Њ–Ї–Њ–ї—Ц–љ–љ—П —В–∞ —Ц–љ—И–Є—Е –Њ—Б–ї–∞–±–ї–µ–љ–Є—Е –ї—О–і–µ–є. –Ч–∞ —Б—В–∞—А–Є–Љ–Є –Њ—Ж—Ц–љ–Ї–∞–Љ–Є, —Ц—Б–њ–∞–љ—Б—М–Ї–Є–є –≥—А–Є–њ –Ј–∞–±—А–∞–≤ 40-50 –Љ–ї–љ –ґ–Є—В—В—Ц–≤[ 164] [ 165]
–С—Ц–ї—М—И—Ц—Б—В—М –і–Њ—Б–ї—Ц–і–љ–Є–Ї—Ц–≤ –≤–≤–∞–ґ–∞—О—В—М, —Й–Њ –Т–Ж–Ы –Ј'—П–≤–Є–≤—Б—П –≤ –°—Г–±—Б–∞—Е–∞—А—Б—М–Ї—Ц–є –Р—Д—А–Є—Ж—Ц —Г XX —Б—В–Њ–ї—Ц—В—В—Ц[ 166] –Ю–±'—Ф–і–љ–∞–љ–Њ—Ч –њ—А–Њ–≥—А–∞–Љ–Є –Ю—А–≥–∞–љ—Ц–Ј–∞—Ж—Ц—Ч –Ю–±'—Ф–і–љ–∞–љ–Є—Е –Э–∞—Ж—Ц–є –Ј –Т–Ж–Ы/–°–Э–Ж–Ф —В–∞ –Т—Б–µ—Б–≤—Ц—В–љ—М–Њ—Ч –Њ—А–≥–∞–љ—Ц–Ј–∞—Ж—Ц—Ч –Њ—Е–Њ—А–Њ–љ–Є –Ј–і–Њ—А–Њ–≤'—П , –≤—Ц–і –°–Э–Ж–Ф—Г (–Њ—Б—В–∞–љ–љ—М–Њ—Ч —Б—В–∞–і—Ц—Ч –Т–Ж–Ы-—Ц–љ—Д–µ–Ї—Ж—Ц—Ч) –њ–Њ–Љ–µ—А–ї–Њ –њ–Њ–љ–∞–і 25 –Љ—Ц–ї—М–є–Њ–љ—Ц–≤ –Њ—Б—Ц–± –Ј –Љ–Њ–Љ–µ–љ—В—Г —А–µ—Ф—Б—В—А–∞—Ж—Ц—Ч –њ–µ—А—И–Њ–≥–Њ –≤–Є–њ–∞–і–Ї—Г –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П 5 —З–µ—А–≤–љ—П 1981 —А–Њ–Ї—Г, —Й–Њ —А–Њ–±–Є—В—М –є–Њ–≥–Њ –Њ–і–љ—Ц—Ф—О –Ј –љ–∞–є–±—Ц–ї—М—И —А—Г–є–љ—Ц–≤–љ–Є—Е –µ–њ—Ц–і–µ–Љ—Ц–є –Ј–∞ –≤—Б—О –і–Њ–Ї—Г–Љ–µ–љ—В–Њ–≤–∞–љ—Г —Ц—Б—В–Њ—А—Ц—О. 2007 —А–Њ–Ї—Г –Ј–∞—А–µ—Ф—Б—В—А–Њ–≤–∞–љ–Њ 2,7 –Љ–ї–љ –≤–Є–њ–∞–і–Ї—Ц–≤ –Ј–∞—А–∞–ґ–µ–љ–љ—П –Т–Ж–Ы —Ц 2 –Љ–ї–љ —Б–Љ–µ—А—В–µ–є –≤—Ц–і –њ–Њ–≤'—П–Ј–∞–љ–Є—Е –Ј –Т–Ж–Ы –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ—М[ 168]
–Ъ—Ц–ї—М–Ї–∞ –≤–Є—Б–Њ–Ї–Њ–ї–µ—В–∞–ї—М–љ–Є—Е –≤—Ц—А—Г—Б–љ–Є—Е –њ–∞—В–Њ–≥–µ–љ—Ц–≤ –љ–∞–ї–µ–ґ–∞—В—М –і–Њ —А–Њ–і–Є–љ–Є —Д—Ц–ї–Њ–≤—Ц—А—Г—Б—Ц–≤. –§—Ц–ї–Њ–≤—Ц—А—Г—Б–Є —Ф —Д—Ц–ї–∞–Љ–µ–љ—В–Њ–њ–Њ–і—Ц–±–љ–Є–Љ–Є –≤—Ц—А—Г—Б–∞–Љ–Є, —Й–Њ —Б–њ—А–Є—З–Є–љ—П—О—В—М –≥–µ–Љ–Њ—А–∞–≥—Ц—З–љ—Г –≥–∞—А—П—З–Ї—Г , –і–Њ –љ–Є—Е —В–∞–Ї–Њ–ґ –≤—Ц–і–љ–Њ—Б—П—В—М –Ј–±—Г–і–љ–Є–Ї–∞ –≥–µ–Љ–Њ—А–∞–≥—Ц—З–љ–Њ—Ч –≥–∞—А—П—З–Ї–Є –Х–±–Њ–ї–∞ —Ц –≤—Ц—А—Г—Б –Ь–∞—А–±—Г—А–≥ . –Т—Ц—А—Г—Б –Ь–∞—А–±—Г—А–≥ –њ—А–Є–≤–µ—А–љ—Г–≤ —И–Є—А–Њ–Ї—Г —Г–≤–∞–≥—Г –њ—А–µ—Б–Є —Г –Ї–≤—Ц—В–љ—Ц 2005 —А–Њ–Ї—Г —З–µ—А–µ–Ј —Б–њ–∞–ї–∞—Е –≤ –Р–љ–≥–Њ–ї—Ц . –¶–µ–є —Б–њ–∞–ї–∞—Е —В—А–Є–≤–∞–≤ –Ј –ґ–Њ–≤—В–љ—П 2004 —А–Њ–Ї—Г —Ц –∞–ґ –і–Њ 2005 —А–Њ–Ї—Г –є —Г–≤—Ц–є—И–Њ–≤ –≤ —Ц—Б—В–Њ—А—Ц—О —П–Ї –љ–∞–є–ґ–∞—Е–ї–Є–≤—Ц—И–∞ –µ–њ—Ц–і–µ–Љ—Ц—П –±—Г–і—М-—П–Ї–Њ—Ч –≥–µ–Љ–Њ—А–∞–≥—Ц—З–љ–Њ—Ч –≥–∞—А—П—З–Ї–Є[ 169]
–Т—Ц—А—Г—Б –Ь–∞—А–±—Г—А–≥
–Т—Ц—А—Г—Б–Є –Љ–Њ–ґ—Г—В—М —Б–њ—А–Є—З–Є–љ—П—В–Є –Ј–ї–Њ—П–Ї—Ц—Б–љ—Ц –љ–Њ–≤–Њ—Г—В–≤–Њ—А–µ–љ–љ—П (–Ј–Њ–Ї—А–µ–Љ–∞, —А–∞–Ї –њ–µ—З—Ц–љ–Ї–Є –∞–±–Њ —Б–∞—А–Ї–Њ–Љ—Г –Ъ–∞–њ–Њ—И—Ц ) —Г –ї—О–і–Є–љ–Є —В–∞ —Ц–љ—И–Є—Е –≤–Є–і—Ц–≤, —Е–Њ—З–∞ –≤–Њ–љ–Є –≤–Є–љ–Є–Ї–∞—О—В—М –ї–Є—И–µ —Г –љ–µ–Ј–љ–∞—З–љ–Њ—Ч —З–∞—Б—В–Є–љ–Є —Ц–љ—Д—Ц–Ї–Њ–≤–∞–љ–Є—Е. –Я—Г—Е–ї–Є–љ–Њ—А–Њ–і–љ—Ц –≤—Ц—А—Г—Б–Є –љ–∞–ї–µ–ґ–∞—В—М –і–Њ —А—Ц–Ј–љ–Є—Е —А–Њ–і–Є–љ; —Б–µ—А–µ–і –љ–Є—Е —Ц –†–Э–Ъ-, —Ц –Ф–Э–Ъ-–≤–Љ—Ц—Б–љ—Ц –≤—Ц—А—Г—Б–Є, —В–Њ–Љ—Г —Ф–і–Є–љ–Њ–≥–Њ —В–Є–њ—Г ¬Ђ–Њ–љ–Ї–Њ–≤—Ц—А—Г—Б¬ї –љ–µ —Ц—Б–љ—Г—Ф (–Ј–∞—Б—В–∞—А—Ц–ї–Є–є —В–µ—А–Љ—Ц–љ, —Б–њ–Њ—З–∞—В–Ї—Г –Ј–∞—Б—В–Њ—Б–Њ–≤—Г–≤–∞–љ–Є–є –і–Њ —А–µ—В—А–Њ–≤—Ц—А—Г—Б—Ц–≤ , —Й–Њ —И–≤–Є–і–Ї–Њ —В—А–∞–љ—Б—Д–Њ—А–Љ—Г—О—В—М—Б—П). –†–Њ–Ј–≤–Є—В–Њ–Ї —А–∞–Ї—Г –≤–Є–Ј–љ–∞—З–∞—Ф—В—М—Б—П –±–∞–≥–∞—В—М–Љ–∞ —Д–∞–Ї—В–Њ—А–∞–Љ–Є, —П–Ї-–Њ—В —Ц–Љ—Г–љ—Ц—В–µ—В —Е–∞–Ј—П—Ч–љ–∞[ 170] –Љ—Г—В–∞—Ж—Ц—Ч [ 171] –њ–∞–њ—Ц–ї–Њ–Љ–∞–≤—Ц—А—Г—Б—Г –ї—О–і–Є–љ–Є , –≤—Ц—А—Г—Б—Г –≥–µ–њ–∞—В–Є—В—Г B —Ц C, –≤—Ц—А—Г—Б—Г –Х–њ—И—В–µ–є–љ–∞ вАФ –С–∞—А—А, –≥–µ—А–њ–µ—Б–≤—Ц—А—Г—Б—Г —Б–∞—А–Ї–Њ–Љ–Є –Ъ–∞–њ–Њ—И—Ц —Ц –ї—О–і—Б—М–Ї–Њ–≥–Њ T-–ї—Ц–Љ—Д–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –≤—Ц—А—Г—Б—Г [en] –њ–Њ–ї—Ц–Њ–Љ–∞–≤—Ц—А—Г—Б –Ї–ї—Ц—В–Є–љ –Ь–µ—А–Ї–µ–ї—П [en] —А–∞–Ї—Г —И–Ї—Ц—А–Є , –Ј–≤–∞–љ–Њ–≥–Њ –Ї–∞—А—Ж–Є–љ–Њ–Љ–Њ—О –Ї–ї—Ц—В–Є–љ –Ь–µ—А–Ї–µ–ї—П[ 172] [ 173] [ 174] —В—А–Њ–њ—Ц—З–љ–Њ–≥–Њ —Б–њ–∞—Б—В–Є—З–љ–Њ–≥–Њ –њ–∞—А–∞–њ–µ—А–µ–Ј—Г [en] –Ј—А—Ц–ї–Њ–≥–Њ –ї–µ–є–Ї–Њ–Ј—Г –Ґ-–Ї–ї—Ц—В–Є–љ [en] [ 175] —А–∞–Ї —И–Є–є–Ї–Є –Љ–∞—В–Ї–Є , —И–Ї—Ц—А–Є, –∞–љ—Г—Б–∞ —Ц —Б—В–∞—В–µ–≤–Њ–≥–Њ —З–ї–µ–љ–∞ [ 176] –ї—Ц–Љ—Д–Њ–Љ—Г –њ–Њ—А–Њ–ґ–љ–Є–љ–Є —В—Ц–ї–∞, –≤—Ц—А—Г—Б –Х–њ—И—В–µ–є–љ–∞ вАФ –С–∞—А—А вАФ –ї—Ц–Љ—Д–Њ–Љ—Г –С–µ—А–Ї—Ц—В—В–∞ , –ї—Ц–Љ—Д–Њ–≥—А–∞–љ—Г–ї–µ–Љ–∞—В–Њ–Ј , –њ–Њ—А—Г—И–µ–љ–љ—П B-–ї—Ц–Љ—Д–Њ–њ—А–Њ–ї—Ц—Д–µ—А–∞—Ж—Ц—Ч —В–∞ –љ–∞–Ј–Њ—Д–∞—А–Є–љ–≥–µ–∞–ї—М–љ—Г –Ї–∞—А—Ж–Є–љ–Њ–Љ—Г [ 177] –Љ–Є—И–µ–є , —П–Ї–Є—Е –њ–Њ–љ–∞–і 50 —А–Њ–Ї—Ц–≤ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞–ї–Є —П–Ї —В–≤–∞—А–Є–љ–љ–Є—Е –Љ–Њ–і–µ–ї–µ–є –і–ї—П –≤–Є–≤—З–µ–љ–љ—П –≤—Ц—А—Г—Б–љ–Њ–≥–Њ —А–∞–Ї—Г[ 178]
–Ф–≤–∞ —А–Њ—В–∞–≤—Ц—А—Г—Б–Є : –њ—А–∞–≤–Є–є –њ–Њ–Ї—А–Є—В–Є–є –∞–љ—В–Є—В—Ц–ї–∞–Љ–Є , —Й–Њ –Ј—Г–њ–Є–љ—П—О—В—М –є–Њ–≥–Њ –њ—А–Є–Ї—А—Ц–њ–ї–µ–љ–љ—П –і–Њ –Ї–ї—Ц—В–Є–љ —Ц –Ј–∞—А–∞–ґ–µ–љ–љ—П —Ч—Е –Я–µ—А—И–Њ—О –Ј–∞—Е–Є—Б–љ–Њ—О –ї—Ц–љ—Ц—Ф—О –Њ—А–≥–∞–љ—Ц–Ј–Љ—Г –њ—А–Њ—В–Є –≤—Ц—А—Г—Б—Г —Ф –≤—А–Њ–і–ґ–µ–љ–Є–є —Ц–Љ—Г–љ—Ц—В–µ—В . –Ф–Њ –љ—М–Њ–≥–Њ –љ–∞–ї–µ–ґ–∞—В—М –Ї–ї—Ц—В–Є–љ–Є —В–∞ —Ц–љ—И—Ц –Љ–µ—Е–∞–љ—Ц–Ј–Љ–Є, —Й–Њ –Ј–∞–±–µ–Ј–њ–µ—З—Г—О—В—М –љ–µ—Б–њ–µ—Ж–Є—Д—Ц—З–љ–Є–є –Ј–∞—Е–Є—Б—В. –¶–µ –Њ–Ј–љ–∞—З–∞—Ф, —Й–Њ –Ї–ї—Ц—В–Є–љ–Є –≤—А–Њ–і–ґ–µ–љ–Њ–≥–Њ —Ц–Љ—Г–љ—Ц—В–µ—В—Г —А–Њ–Ј–њ—Ц–Ј–љ–∞—О—В—М —Ц —А–µ–∞–≥—Г—О—В—М –љ–∞ –њ–∞—В–Њ–≥–µ–љ–Є –Ј–∞–≥–∞–ї—М–љ–Є–Љ–Є —Б–њ–Њ—Б–Њ–±–∞–Љ–Є, –Њ–і–љ–∞–Ї–Њ–≤–Њ —Й–Њ–і–Њ –≤—Б—Ц—Е –њ–∞—В–Њ–≥–µ–љ—Ц–≤, –∞–ї–µ, –љ–∞ –≤—Ц–і–Љ—Ц–љ—Г –≤—Ц–і –љ–∞–±—Г—В–Њ–≥–Њ —Ц–Љ—Г–љ—Ц—В–µ—В—Г , –≤—А–Њ–і–ґ–µ–љ–Є–є —Ц–Љ—Г–љ—Ц—В–µ—В –љ–µ –і–∞—Ф —Е–∞–Ј—П—Ч–љ—Г —В—А–Є–≤–∞–ї–Њ–≥–Њ –є –љ–∞–і—Ц–є–љ–Њ–≥–Њ –Ј–∞—Е–Є—Б—В—Г[ 179]
–Т–∞–ґ–ї–Є–≤–Є–Љ –њ—А–Є—А–Њ–і–љ–Є–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –Ј–∞—Е–Є—Б—В—Г –Њ—А–≥–∞–љ—Ц–Ј–Љ—Г –µ—Г–Ї–∞—А—Ц–Њ—В—Ц–≤ –њ—А–Њ—В–Є –≤—Ц—А—Г—Б—Ц–≤ —Ф –†–Э–Ъ-—Ц–љ—В–µ—А—Д–µ—А–µ–љ—Ж—Ц—П [ 180] —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—Ч –±–∞–≥–∞—В—М–Њ—Е –≤—Ц—А—Г—Б—Ц–≤ –њ–µ—А–µ–і–±–∞—З–∞—Ф –љ–∞—П–≤–љ—Ц—Б—В—М —Б—В–∞–і—Ц—Ч –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Њ—Ч –†–Э–Ъ. –Ф–ї—П –±–Њ—А–Њ—В—М–±–Є –Ј –њ–Њ–і—Ц–±–љ–Є–Љ–Є –≤—Ц—А—Г—Б–∞–Љ–Є, –Ї–ї—Ц—В–Є–љ–∞ –Љ–∞—Ф —Б–Є—Б—В–µ–Љ—Г –љ–µ—Б–њ–µ—Ж–Є—Д—Ц—З–љ–Њ—Ч –і–µ–≥—А–∞–і–∞—Ж—Ц—Ч –Њ–і–љ–Њ вАФ —Ц –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Є—Е –†–Э–Ъ. –Ъ–Њ–ї–Є –њ–Њ–і—Ц–±–љ–Є–є –≤—Ц—А—Г—Б –њ—А–Њ—Е–Њ–і–Є—В—М —Г –Ї–ї—Ц—В–Є–љ—Г —Ц –≤–Є–≤—Ц–ї—М–љ—П—Ф –≥–µ–љ–Њ–Љ–љ—Г –†–Э–Ъ –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ—Г, –±—Ц–ї–Ї–Њ–≤–Є–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б –і–∞–є—Б–µ—А RISC , —П–Ї–Є–є —А—Г–є–љ—Г—Ф –≤—Ц—А—Г—Б–љ—Г –†–Э–Ъ, —Ц –њ–µ—А–µ—И–Ї–Њ–і–ґ–∞—Ф —А–Њ–Ј–Љ–љ–Њ–ґ–µ–љ–љ—О –≤—Ц—А—Г—Б—Г. –†–Њ—В–∞–≤—Ц—А—Г—Б–Є –Ј–і–∞—В–љ—Ц —Г–љ–Є–Ї–љ—Г—В–Є –†–Э–Ъ-—Ц–љ—В–µ—А—Д–µ—А–µ–љ—Ж—Ц—Ч, –Ј–±–µ—А—Ц–≥–∞—О—З–Є —З–∞—Б—В–Є–љ—Г –Ї–∞–њ—Б–Є–і—Г –љ–∞–≤—Ц—В—М –≤—Б–µ—А–µ–і–Є–љ—Ц –Ї–ї—Ц—В–Є–љ–Є —Ц –≤–Є–њ—Г—Б–Ї–∞—О—З–Є –љ–Њ–≤–Њ—Б—В–≤–Њ—А–µ–љ—Ц –Љ–†–Э–Ъ —З–µ—А–µ–Ј —И–њ–∞—А–Є–љ–Є —Г –≤–љ—Г—В—А—Ц—И–љ—М–Њ–Љ—Г –Ї–∞–њ—Б–Є–і—Ц. –У–µ–љ–Њ–Љ–љ–∞ –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–∞ –†–Э–Ъ –ґ –Ј–∞–ї–Є—И–∞—Ф—В—М—Б—П –≤—Б–µ—А–µ–і–Є–љ—Ц –љ—М–Њ–≥–Њ[ 181] [ 182]
–Ъ–Њ–ї–Є —Б–Є—Б—В–µ–Љ–∞ –љ–∞–±—Г—В–Њ–≥–Њ —Ц–Љ—Г–љ—Ц—В–µ—В—Г —Г —Е—А–µ–±–µ—В–љ–Є—Е —Б—В–Є–Ї–∞—Ф—В—М—Б—П –Ј –≤—Ц—А—Г—Б–Њ–Љ, –≤–Њ–љ–∞ —Г—В–≤–Њ—А—О—Ф —Б–њ–µ—Ж–Є—Д—Ц—З–љ—Ц –∞–љ—В–Є—В—Ц–ї–∞ , —Й–Њ –њ—А–Є—Ф–і–љ—Г—О—В—М—Б—П –і–Њ –≤—Ц—А—Г—Б—Г —Ц —З–∞—Б—В–Њ —А–Њ–±–ї—П—В—М –є–Њ–≥–Њ –±–µ–Ј–њ–µ—З–љ–Є–Љ. –¶–µ –љ–∞–Ј–Є–≤–∞—Ф—В—М—Б—П –≥—Г–Љ–Њ—А–∞–ї—М–љ–Є–Љ —Ц–Љ—Г–љ—Ц—В–µ—В–Њ–Љ [en] IgM , –і—Г–ґ–µ –µ—Д–µ–Ї—В–Є–≤–љ–Њ –љ–µ–є—В—А–∞–ї—Ц–Ј—Г—Ф –≤—Ц—А—Г—Б–Є, –∞–ї–µ –є–Њ–≥–Њ —Г—В–≤–Њ—А—О—О—В—М –Ї–ї—Ц—В–Є–љ–Є —Ц–Љ—Г–љ–љ–Њ—Ч —Б–Є—Б—В–µ–Љ–Є –ї–Є—И–µ –њ—А–Њ—В—П–≥–Њ–Љ –Ї—Ц–ї—М–Ї–Њ—Е —В–Є–ґ–љ—Ц–≤. –°–Є–љ—В–µ–Ј –і—А—Г–≥–Њ–≥–Њ вАФ IgG вАФ —В—А–Є–≤–∞—Ф –љ–µ–≤–Є–Ј–љ–∞—З–µ–љ–Њ –і–Њ–≤–≥–Њ. –Я—А–Є—Б—Г—В–љ—Ц—Б—В—М IgM —Г –Ї—А–Њ–≤—Ц –≥–Њ—Б–њ–Њ–і–∞—А—П —Б–≤—Ц–і—З–Є—В—М –њ—А–Њ –љ–∞—П–≤–љ—Ц—Б—В—М –≥–Њ—Б—В—А–Њ—Ч —Ц–љ—Д–µ–Ї—Ж—Ц—Ч, —В–Њ–і—Ц —П–Ї IgG —Б–≤—Ц–і—З–Є—В—М –њ—А–Њ —Ц–љ—Д–µ–Ї—Ж—Ц—О, –њ–µ—А–µ–љ–µ—Б–µ–љ—Г –≤ –Љ–Є–љ—Г–ї–Њ–Љ—Г[ 183] —Ц–Љ—Г–љ—Ц—В–µ—В [ 184] TRIM21 –Љ–Њ–ґ–µ –њ—А–Є–Ї—А—Ц–њ–ї—О–≤–∞—В–Є –∞–љ—В–Є—В—Ц–ї–∞ –і–Њ –њ–Њ–≤–µ—А—Е–љ—Ц –≤—Ц—А—Г—Б–љ–Є—Е —З–∞—Б—В–Є–љ–Њ–Ї. –¶–µ —Б–њ—А–Є—З–Є–љ—О—Ф –њ–Њ–і–∞–ї—М—И–µ —А—Г–є–љ—Г–≤–∞–љ–љ—П –≤—Ц—А—Г—Б–љ–Њ—Ч —З–∞—Б—В–Є–љ–Ї–Є —Д–µ—А–Љ–µ–љ—В–∞–Љ–Є –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч –њ—А–Њ—В–µ–∞—Б–Њ–Љ–љ–Њ—Ч —Б–Є—Б—В–µ–Љ–Є[ 185]
–Ф—А—Г–≥–Є–є –Ј–∞—Е–Є—Б–љ–Є–є –Љ–µ—Е–∞–љ—Ц–Ј–Љ —Е—А–µ–±–µ—В–љ–Є—Е –њ—А–Њ—В–Є –≤—Ц—А—Г—Б—Ц–≤ –љ–∞–Ј–Є–≤–∞—Ф—В—М—Б—П –Ї–ї—Ц—В–Є–љ–љ–Є–Љ —Ц–Љ—Г–љ—Ц—В–µ—В–Њ–Љ —Ц –≤–Ї–ї—О—З–∞—Ф —Ц–Љ—Г–љ–љ—Ц –Ї–ї—Ц—В–Є–љ–Є, –≤—Ц–і–Њ–Љ—Ц —П–Ї T-–ї—Ц–Љ—Д–Њ—Ж–Є—В–Є . –Ъ–ї—Ц—В–Є–љ–Є —В—Ц–ї–∞ –њ–Њ—Б—В—Ц–є–љ–Њ –љ–µ—Б—Г—В—М –Ї–Њ—А–Њ—В–Ї—Ц —Д—А–∞–≥–Љ–µ–љ—В–Є –≤–ї–∞—Б–љ–Є—Е –±—Ц–ї–Ї—Ц–≤ –љ–∞ —Б–≤–Њ—Ч—Е –њ–Њ–≤–µ—А—Е–љ—П—Е, —Ц, —П–Ї—Й–Њ –Ґ-–ї—Ц–Љ—Д–Њ—Ж–Є—В–Є —А–Њ–Ј–њ—Ц–Ј–љ–∞—О—В—М —В—Г—В –њ—Ц–і–Њ–Ј—А—Ц–ї—Ц –≤—Ц—А—Г—Б–љ—Ц —Д—А–∞–≥–Љ–µ–љ—В–Є, –Ї–ї—Ц—В–Є–љ–∞-—Е–∞–Ј—П—Ч–љ —А—Г–є–љ—Г—Ф—В—М—Б—П –Ї–ї—Ц—В–Є–љ–∞–Љ–Є, —Й–Њ –љ–∞–Ј–Є–≤–∞—О—В—М—Б—П –Ґ-–Ї—Ц–ї–µ—А–∞–Љ–Є , —Ц –њ–Њ—З–Є–љ–∞—Ф—В—М—Б—П —Г—В–≤–Њ—А–µ–љ–љ—П —Б–њ–µ—Ж–Є—Д—Ц—З–љ–Є—Е –і–Њ –≤—Ц—А—Г—Б—Г T-–ї—Ц–Љ—Д–Њ—Ж–Є—В—Ц–≤. –Ґ–∞–Ї—Ц –Ї–ї—Ц—В–Є–љ–Є, —П–Ї –Љ–∞–Ї—А–Њ—Д–∞–≥–Є , —Б–њ–µ—Ж—Ц–∞–ї—Ц–Ј—Г—О—В—М—Б—П –љ–∞ –њ—А–µ–Ј–µ–љ—В–∞—Ж—Ц—Ч –∞–љ—В–Є–≥–µ–љ—Ц–≤ [en] [ 186]
–Т–∞–ґ–ї–Є–≤–Њ—О –Ј–∞—Е–Є—Б–љ–Њ—О —А–µ–∞–Ї—Ж—Ц—Ф—О —Е–∞–Ј—П—Ч–љ–∞ —Ф –≤–Є—А–Њ–±–ї–µ–љ–љ—П —Ц–љ—В–µ—А—Д–µ—А–Њ–љ—Г . –Ж–љ—В–µ—А—Д–µ—А–Њ–љ вАФ —Ж–µ –±—Ц–ї–Њ–Ї. –Щ–Њ–≥–Њ —А–Њ–ї—М –≤ —Ц–Љ—Г–љ—Ц—В–µ—В—Ц вАФ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–∞, –Ј—А–µ—И—В–Њ—О –≤—Ц–љ –Ј—Г–њ–Є–љ—П—Ф –≤—Ц—А—Г—Б, –њ—А–Є–њ–Є–љ—П—О—З–Є —Г—В–≤–Њ—А–µ–љ–љ—П –љ–Њ–≤–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Г—А–∞–ґ–µ–љ–Є–Љ–Є –Ї–ї—Ц—В–Є–љ–∞–Љ–Є, –≤–±–Є–≤–∞—О—З–Є —Ч—Е —В–∞ —Ч—Е–љ—Ц—Е –±–ї–Є–Ј—М–Ї–Є—Е —Б—Г—Б—Ц–і—Ц–≤[ 187] [–і–ґ–µ—А–µ–ї–Њ? .
–Э–µ –њ—А–Њ—В–Є –≤—Б—Ц—Е –≤—Ц—А—Г—Б—Ц–≤ —Г—В–≤–Њ—А—О—Ф—В—М—Б—П —В–∞–Ї–∞ –Ј–∞—Е–Є—Б–љ–∞ —Ц–Љ—Г–љ–љ–∞ –≤—Ц–і–њ–Њ–≤—Ц–і—М. –Т–Ж–Ы –≤–і–∞—Ф—В—М—Б—П —Г–љ–Є–Ї–љ—Г—В–Є —Ц–Љ—Г–љ–љ–Њ—Ч –≤—Ц–і–њ–Њ–≤—Ц–і—Ц, –њ–Њ—Б—В—Ц–є–љ–Њ –Ј–Љ—Ц–љ—О—О—З–Є –њ–Њ—Б–ї—Ц–і–Њ–≤–љ—Ц—Б—В—М –∞–Љ—Ц–љ–Њ–Ї–Є—Б–ї–Њ—В –њ–Њ–≤–µ—А—Е–љ–µ–≤–Є—Е –±—Ц–ї–Ї—Ц–≤ –≤—Ц—А—Ц–Њ–љ–∞. –Ґ–∞–Ї—Ц —Б—В—Ц–є–Ї—Ц –≤—Ц—А—Г—Б–Є –њ—А–Њ—Б–Ї–Њ—З—Г—О—В—М –њ–Њ–≤–Ј —Ц–Љ—Г–љ–љ—Г —Б–Є—Б—В–µ–Љ—Г, —Ц–Ј–Њ–ї—О—О—З–Є—Б—М –≤—Ц–і —Ц–Љ—Г–љ–љ–Є—Е –Ї–ї—Ц—В–Є–љ, –±–ї–Њ–Ї—Г—О—З–Є –њ—А–µ–Ј–µ–љ—В–∞—Ж—Ц—О –∞–љ—В–Є–≥–µ–љ—Ц–≤, –Ј–∞–≤–і—П–Ї–Є —Б—В—Ц–є–Ї–Њ—Б—В—Ц –і–Њ —Ж–Є—В–Њ–Ї—Ц–љ—Ц–≤ , —Г—Е–Є–ї—П—О—З–Є—Б—М –≤—Ц–і –њ—А–Є—А–Њ–і–љ–Є—Е –Ї—Ц–ї–µ—А—Ц–≤ , –Ј—Г–њ–Є–љ—П—О—З–Є –∞–њ–Њ–њ—В–Њ–Ј –Ї–ї—Ц—В–Є–љ-–≥–Њ—Б–њ–Њ–і–∞—А—Ц–≤, –∞ —В–∞–Ї–Њ–ґ –Ј–∞ —А–∞—Е—Г–љ–Њ–Ї –∞–љ—В–Є–≥–µ–љ–љ–Њ—Ч –Љ—Ц–љ–ї–Є–≤–Њ—Б—В—Ц [ 188] –љ–µ–є—А–Њ—В—А–Њ–њ–љ–Є–Љ–Є –≤—Ц—А—Г—Б–∞–Љ–Є , –њ–Њ—И–Є—А—О—О—В—М—Б—П —Б–µ—А–µ–і –љ–µ—А–≤–Њ–≤–Є—Е –Ї–ї—Ц—В–Є–љ , —В–Њ–±—В–Њ —В–∞–Љ, –і–µ —Ц–Љ—Г–љ–љ–∞ —Б–Є—Б—В–µ–Љ–∞ –љ–µ –≤ –Ј–Љ–Њ–Ј—Ц –і—Ц—Б—В–∞—В–Є—Б—П –і–Њ –љ–Є—Е[–і–ґ–µ—А–µ–ї–Њ? .
–Ю—Б–Ї—Ц–ї—М–Ї–Є –≤—Ц—А—Г—Б–Є –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М –і–ї—П —А–Њ–Ј–Љ–љ–Њ–ґ–µ–љ–љ—П –њ—А–Є—А–Њ–і–љ—Ц –Љ–µ—В–∞–±–Њ–ї—Ц—З–љ—Ц —И–ї—П—Е–Є –Ї–ї—Ц—В–Є–љ-–≥–Њ—Б–њ–Њ–і–∞—А—Ц–≤, —В–Њ —Ч—Е —Б–Ї–ї–∞–і–љ–Њ –Ј–љ–Є—Й–Є—В–Є –±–µ–Ј –Ј–∞—Б—В–Њ—Б—Г–≤–∞–љ–љ—П –њ—А–µ–њ–∞—А–∞—В—Ц–≤, —В–Њ–Ї—Б–Є—З–љ–Є—Е –і–ї—П —Б–∞–Љ–Є—Е –Ї–ї—Ц—В–Є–љ-–≥–Њ—Б–њ–Њ–і–∞—А—Ц–≤. –Э–∞–є–µ—Д–µ–Ї—В–Є–≤–љ—Ц—И–Є–Љ–Є –Љ–µ–і–Є—З–љ–Є–Љ–Є –Ј–∞—Е–Њ–і–∞–Љ–Є –њ—А–Њ—В–Є –≤—Ц—А—Г—Б–љ–Є—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є —Ф –≤–∞–Ї—Ж–Є–љ–∞—Ж—Ц—Ч , —Й–Њ —Б—В–≤–Њ—А—О—О—В—М —Ц–Љ—Г–љ—Ц—В–µ—В –і–Њ —Ц–љ—Д–µ–Ї—Ж—Ц—Ч, —Ц –њ—А–Њ—В–Є–≤—Ц—А—Г—Б–љ—Ц –њ—А–µ–њ–∞—А–∞—В–Є , —Й–Њ –≤–Є–±—Ц—А–Ї–Њ–≤–Њ —Ц–љ–≥—Ц–±—Г—О—В—М —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—О –≤—Ц—А—Г—Б—Ц–≤.
–Т–∞–Ї—Ж–Є–љ–∞—Ж—Ц—П —Ф –і–µ—И–µ–≤–Є–Љ —Ц –µ—Д–µ–Ї—В–Є–≤–љ–Є–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –Ј–∞–њ–Њ–±—Ц–≥–∞–љ–љ—П –≤—Ц—А—Г—Б–љ–Є—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є. –Т–∞–Ї—Ж–Є–љ–Є –і–ї—П –Ј–∞–њ–Њ–±—Ц–≥–∞–љ–љ—П –≤—Ц—А—Г—Б–љ–Є—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є –Ј–∞—Б—В–Њ—Б–Њ–≤—Г–≤–∞–ї–Є —Й–µ –Ј–∞–і–Њ–≤–≥–Њ –і–Њ –≤—Ц–і–Ї—А–Є—В—В—П —Б–∞–Љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤. –З—Е –Ј–∞—Б—В–Њ—Б—Г–≤–∞–љ–љ—П –і–Њ–њ–Њ–Љ–Њ–≥–ї–Њ —А—Ц–Ј–Ї–Њ –Ј–љ–Є–Ј–Є—В–Є –њ—А–Њ—В—Ц–Ї–∞–љ–љ—П —В–∞ —Б–Љ–µ—А—В–љ—Ц—Б—В—О –≤—Ц–і –≤—Ц—А—Г—Б–љ–Є—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є, —П–Ї-–Њ—В –њ–Њ–ї—Ц–Њ–Љ—Ц—Ф–ї—Ц—В , –Ї—Ц—А , —Б–≤–Є–љ–Ї–∞ —Ц –Ї—А–∞—Б–љ—Г—Е–∞ [ 189] [ 190] [ 191] [ 192] –∞–љ—В–Є–≥–µ–љ–Є )[ 193] —Ц–Љ—Г–љ–Њ–і–µ—Д—Ц—Ж–Є—В ), –±–Њ –љ–∞–≤—Ц—В—М –Њ—Б–ї–∞–±–ї–µ–љ–Є–є –≤—Ц—А—Г—Б —Г –љ–Є—Е –Љ–Њ–ґ–µ —Б–њ—А–Є—З–Є–љ–Є—В–Є –≤–Є—Е—Ц–і–љ–µ –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П[ 194] –±—Ц–Њ—В–µ—Е–љ–Њ–ї–Њ–≥—Ц—Ч —В–∞ –≥–µ–љ–µ—В–Є—З–љ—Г —Ц–љ–ґ–µ–љ–µ—А—Ц—О . –£ —В–∞–Ї–Є—Е –≤–∞–Ї—Ж–Є–љ–∞—Е –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М —В—Ц–ї—М–Ї–Є –Ї–∞–њ—Б–Є–і–љ—Ц –±—Ц–ї–Ї–Є –≤—Ц—А—Г—Б—Ц–≤. –Я—А–Є–Ї–ї–∞–і–Њ–Љ —В–∞–Ї–Є—Е –≤–∞–Ї—Ж–Є–љ —Ф –≤–∞–Ї—Ж–Є–љ–∞ –њ—А–Њ—В–Є –≤—Ц—А—Г—Б—Г –≥–µ–њ–∞—В–Є—В—Г B[ 195] [ 196] –Т–∞–Ї—Ж–Є–љ–∞ –њ—А–Њ—В–Є –ґ–Њ–≤—В–Њ—Ч –≥–∞—А—П—З–Ї–Є [en] [ 197]
–У—Г–∞–љ–Њ–Ј–Є–љ –Э—Г–Ї–ї–µ–Њ–Ј–Є–і–љ–Є–є –∞–љ–∞–ї–Њ–≥ [en] –∞—Ж–Є–Ї–ї–Њ–≤—Ц—А –Я—А–Њ—В–Є–≤—Ц—А—Г—Б–љ—Ц –њ—А–µ–њ–∞—А–∞—В–Є —З–∞—Б—В–Њ —Ф –∞–љ–∞–ї–Њ–≥–∞–Љ–Є –љ—Г–Ї–ї–µ–Њ–Ј–Є–і—Ц–≤ . –Т–Њ–љ–Є –≤–±—Г–і–Њ–≤—Г—О—В—М—Б—П –≤ –≥–µ–љ–Њ–Љ –≤—Ц—А—Г—Б—Г –њ—Ц–і —З–∞—Б —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—Ч, —Ц –љ–∞ —Ж—М–Њ–Љ—Г –ґ–Є—В—В—Ф–≤–Є–є —Ж–Є–Ї–ї –≤—Ц—А—Г—Б—Г –Ј—Г–њ–Є–љ—П—Ф—В—М—Б—П, –Њ—Б–Ї—Ц–ї—М–Ї–Є –љ–Њ–≤–Њ—Б–Є–љ—В–µ–Ј–Њ–≤–∞–љ–∞ –Ф–Э–Ъ –љ–µ–і—Ц—П–ї—М–љ–∞. –¶–µ –≤–Є–Ї–ї–Є–Ї–∞–љ–Њ —В–Є–Љ, —Й–Њ –≤ –∞–љ–∞–ї–Њ–≥—Ц–≤ –≤—Ц–і—Б—Г—В–љ—Ц –≥—Ц–і—А–Њ–Ї—Б–Є–ї—М–љ—Ц –≥—А—Г–њ–Є , —П–Ї—Ц —А–∞–Ј–Њ–Љ –Ј –∞—В–Њ–Љ–∞–Љ–Є —Д–Њ—Б—Д–Њ—А—Г –Ј'—Ф–і–љ—Г—О—В—М—Б—П —Ц —Д–Њ—А–Љ—Г—О—В—М –ґ–Њ—А—Б—В–Ї–Є–є ¬Ђ–Ї—Ц—Б—В—П–Ї¬ї –Љ–Њ–ї–µ–Ї—Г–ї–Є –Ф–Э–Ъ. –¶–µ –љ–∞–Ј–Є–≤–∞—Ф—В—М—Б—П –ї–∞–љ—Ж—О–≥–Њ–≤–Њ—О —В–µ—А–Љ—Ц–љ–∞—Ж—Ц—Ф—О –Ф–Э–Ъ[ 198] –∞—Ж–Є–Ї–ї–Њ–≤—Ц—А , —Й–Њ –Ј–∞—Б—В–Њ—Б–Њ–≤—Г—Ф—В—М—Б—П –њ—А–Њ—В–Є —Ц–љ—Д–µ–Ї—Ж—Ц–є, —П–Ї—Ц —Б–њ—А–Є—З–Є–љ—О—О—В—М –≤—Ц—А—Г—Б –њ—А–Њ—Б—В–Њ–≥–Њ –≥–µ—А–њ–µ—Б—Г, —Ц –ї–∞–Љ—Ц–≤—Г–і–Є–љ (–њ—А–Њ—В–Є –Т–Ж–Ы —В–∞ –≤—Ц—А—Г—Б—Г –≥–µ–њ–∞—В–Є—В—Г B). –Р—Ж–Є–Ї–ї–Њ–≤—Ц—А вАФ –Њ–і–Є–љ –Ј –љ–∞–є—Б—В–∞—А—Ц—И–Є—Е —Ц –љ–∞–є—З–∞—Б—В—Ц—И–µ –њ—А–Є–Ј–љ–∞—З—Г–≤–∞–љ–Є—Е –њ—А–Њ—В–Є–≤—Ц—А—Г—Б–љ–Є—Е –њ—А–µ–њ–∞—А–∞—В—Ц–≤[ 199]
–Ж–љ—И—Ц –Ј–∞—Б—В–Њ—Б–Њ–≤—Г–≤–∞–љ—Ц –њ—А–Њ—В–Є–≤—Ц—А—Г—Б–љ—Ц –њ—А–µ–њ–∞—А–∞—В–Є –Љ–∞—О—В—М –Љ—Ц—И–µ–љ–љ—О —А—Ц–Ј–љ—Ц —Б—В–∞–і—Ц—Ч –ґ–Є—В—В—Ф–≤–Њ–≥–Њ —Ж–Є–Ї–ї—Г –≤—Ц—А—Г—Б—Ц–≤. –Т–Ж–Ы, —Й–Њ–± —Б—В–∞—В–Є –њ–Њ–≤–љ—Ц—Б—В—О –Ј–∞—А–∞–Ј–љ–Є–Љ, –њ–Њ—В—А–µ–±—Г—Ф –њ—А–Њ—В–µ–Њ–ї—Ц—В–Є—З–љ–Њ–≥–Њ —Д–µ—А–Љ–µ–љ—В—Г , –≤—Ц–і–Њ–Љ–Њ–≥–Њ —П–Ї –Т–Ж–Ы-1 –њ—А–Њ—В–µ–∞–Ј–∞ [en] —Ц–љ–≥—Ц–±—Ц—В–Њ—А–∞–Љ–Є –њ—А–Њ—В–µ–∞–Ј–Є [en]
–У–µ–њ–∞—В–Є—В C —Б–њ—А–Є—З–Є–љ—П—Ф—В—М—Б—П –†–Э–Ъ-–≤–Љ—Ц—Б–љ–Є–Љ –≤—Ц—А—Г—Б–Њ–Љ. –£ 80 % —Ц–љ—Д—Ц–Ї–Њ–≤–∞–љ–Є—Е –ї—О–і–µ–є —Ц–љ—Д–µ–Ї—Ж—Ц—П –Љ–∞—Ф —Е—А–Њ–љ—Ц—З–љ–Є–є —Е–∞—А–∞–Ї—В–µ—А, —Ц –±–µ–Ј –ї—Ц–Ї—Г–≤–∞–љ–љ—П –≤–Њ–љ–Є –Ј–∞–ї–Є—И–∞—В—М—Б—П –Ј–∞—А–∞–ґ–µ–љ–Є–Љ–Є –і–Њ –Ї—Ц–љ—Ж—П —Б–≤–Њ—Ч—Е –і–љ—Ц–≤. –Ю–і–љ–∞–Ї –љ–∞ –њ–Њ—З–∞—В–Ї—Г XXI —Б—В–Њ–ї—Ц—В—В—П –Ј–∞—Б—В–Њ—Б–Њ–≤—Г—О—В—М –µ—Д–µ–Ї—В–Є–≤–љ—Ц –ї—Ц–Ї–Є, —Й–Њ —Б–Ї–ї–∞–і–∞—О—В—М—Б—П –Ј –љ—Г–Ї–ї–µ–Њ–Ј–Є–і–љ–Њ–≥–Њ –∞–љ–∞–ї–Њ–≥–∞ —А–Є–±–∞–≤—Ц—А–Є–љ—Г , –Ї–Њ–Љ–±—Ц–љ–Њ–≤–∞–љ–Њ–≥–Њ –Ј —Ц–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–Љ [ 200] [ 201]
–Т—Ц—А—Г—Б–Є –≤—А–∞–ґ–∞—О—В—М —Г—Б–µ –Ї–ї—Ц—В–Є–љ–љ–µ –ґ–Є—В—В—П, –∞–ї–µ, –њ–Њ–њ—А–Є –њ–Њ–≤—Б—О–і–љ–µ –њ–Њ—И–Є—А–µ–љ–љ—П –≤—Ц—А—Г—Б—Ц–≤, –Ї–Њ–ґ–µ–љ –≤–Є–і –Ї–ї—Ц—В–Є–љ–љ–Є—Е –Њ—А–≥–∞–љ—Ц–Ј–Љ—Ц–≤ –Љ–∞—Ф —Б–≤–Њ—О –љ–Є–Ј–Ї—Г –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –≤—А–∞–ґ–∞—О—В—М, —З–∞—Б—В–Њ —В—Ц–ї—М–Ї–Є —Ж–µ–є –≤–Є–і. –Ф–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є, –Ј–≤–∞–љ—Ц —Б–∞—В–µ–ї—Ц—В–∞–Љ–Є , –Љ–Њ–ґ—Г—В—М —А–Њ–Ј–Љ–љ–Њ–ґ—Г–≤–∞—В–Є—Б—П –ї–Є—И–µ –≤ –Ї–ї—Ц—В–Є–љ–∞—Е, –≤–ґ–µ –Ј–∞—А–∞–ґ–µ–љ–Є—Е —Ц–љ—И–Є–Љ –≤—Ц—А—Г—Б–Њ–Љ[ 48]
–£ —В–≤–∞—А–Є–љ –≤—Ц—А—Г—Б–љ—Ц —Ц–љ—Д–µ–Ї—Ж—Ц—Ч –њ–Њ—А–Њ–і–ґ—Г—О—В—М —Ц–Љ—Г–љ–љ—Г –≤—Ц–і–њ–Њ–≤—Ц–і—М , —П–Ї–∞ –љ–∞–є—З–∞—Б—В—Ц—И–µ –њ—А–Є–Ј–≤–Њ–і–Є—В—М –і–Њ –Ј–љ–Є—Й–µ–љ–љ—П —Е–≤–Њ—А–Њ–±–Њ—В–≤–Њ—А–љ–Њ–≥–Њ –≤—Ц—А—Г—Б—Г. –Ж–Љ—Г–љ–љ—Г –≤—Ц–і–њ–Њ–≤—Ц–і—М —В–∞–Ї–Њ–ґ –Љ–Њ–ґ–љ–∞ —Б–њ—А–Є—З–Є–љ–Є—В–Є –≤–∞–Ї—Ж–Є–љ–∞–Љ–Є, —Й–Њ –і–∞—О—В—М –і—Ц—П–ї—М–љ–Є–є –љ–∞–±—Г—В–Є–є —Ц–Љ—Г–љ—Ц—В–µ—В –њ—А–Њ—В–Є —Б–∞–Љ–µ —Ж—Ц—Ф—Ч –≤—Ц—А—Г—Б–љ–Њ—Ч —Ц–љ—Д–µ–Ї—Ж—Ц—Ч. –Ю–і–љ–∞–Ї –і–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є, –Ј–Њ–Ї—А–µ–Љ–∞ –Т–Ж–Ы —Ц –Ј–±—Г–і–љ–Є–Ї–Є –≤—Ц—А—Г—Б–љ–Є—Е –≥–µ–њ–∞—В–Є—В—Ц–≤ , –Ј–і–∞—В–љ—Ц –њ—А–Њ—Б–Ї–Њ—З–Є—В–Є –њ–Њ–≤–Ј —Ц–Љ—Г–љ–љ—Г –≤—Ц–і–њ–Њ–≤—Ц–і—М, –њ–Њ—А–Њ–і–ґ—Г—О—З–Є —Е—А–Њ–љ—Ц—З–љ—Г —Е–≤–Њ—А–Њ–±—Г. –Р–љ—В–Є–±—Ц–Њ—В–Є–Ї–Є –љ–µ –і—Ц—О—В—М –љ–∞ –≤—Ц—А—Г—Б–Є, –њ—А–Њ—В–µ –±—Г–ї–Њ —А–Њ–Ј—А–Њ–±–ї–µ–љ–Њ –і–µ–Ї—Ц–ї—М–Ї–∞ –њ—А–Њ—В–Є–≤—Ц—А—Г—Б–љ–Є—Е –њ—А–µ–њ–∞—А–∞—В—Ц–≤ (–і–Є–≤. –≤–Є—Й–µ).
–Т—Ц—А—Г—Б–Є —Ф –≤–∞–ґ–ї–Є–≤–Є–Љ–Є –њ–∞—В–Њ–≥–µ–љ–∞–Љ–Є –і–Њ–Љ–∞—И–љ—М–Њ—Ч —Е—Г–і–Њ–±–Є. –Т–Њ–љ–Є —Б–њ—А–Є—З–Є–љ—П—О—В—М, –љ–∞–њ—А–Є–Ї–ї–∞–і, —П—Й—Г—А —Ц ¬Ђ—Б–Є–љ—Ц–є —П–Ј–Є–Ї¬ї [ 203] –°–Њ–±–∞—З–Є–є –њ–∞—А–≤–Њ–≤—Ц—А—Г—Б [en] [ 204]
–Э–∞ —З–∞—Б—В–Ї—Г –±–µ–Ј—Е—А–µ–±–µ—В–љ–Є—Е –њ—А–Є–њ–∞–і–∞—Ф –±–ї–Є–Ј—М–Ї–Њ 80 % –≤—Б—Ц—Е –≤—Ц–і–Њ–Љ–Є—Е –≤–Є–і—Ц–≤ —В–≤–∞—А–Є–љ, —В–Њ–Љ—Г –љ–µ–Љ–∞—Ф –љ—Ц—З–Њ–≥–Њ –і–Є–≤–љ–Њ–≥–Њ –≤ —В–Њ–Љ—Г, —Й–Њ –≤–Њ–љ–Є –њ—А–Є—Е–Њ–≤—Г—О—В—М —Г —Б–Њ–±—Ц –≤–µ–ї–Є—З–µ–Ј–љ—Г –Ї—Ц–ї—М–Ї—Ц—Б—В—М –≤—Ц—А—Г—Б—Ц–≤ —А—Ц–Ј–љ–Є—Е —В–Є–њ—Ц–≤. –Э–∞–є–±—Ц–ї—М—И –≤–Є–≤—З–µ–љ—Ц –≤—Ц—А—Г—Б–Є, —Й–Њ –≤—А–∞–ґ–∞—О—В—М –Ї–Њ–Љ–∞—Е , –∞–ї–µ –љ–∞–≤—Ц—В—М —В—Г—В –і–Њ—Б—В—Г–њ–љ–∞ –њ—А–Њ –љ–Є—Е —Ц–љ—Д–Њ—А–Љ–∞—Ж—Ц—П –Љ–∞—Ф —Д—А–∞–≥–Љ–µ–љ—В–∞—А–љ–Є–є —Е–∞—А–∞–Ї—В–µ—А. –Т—В—Ц–Љ, –Њ—Б—В–∞–љ–љ—Ц–Љ —З–∞—Б–Њ–Љ –Њ–њ–Є—Б–∞–љ–Њ –≤—Ц—А—Г—Б–љ—Ц –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П —Ц –≤ —Ц–љ—И–Є—Е –±–µ–Ј—Е—А–µ–±–µ—В–љ–Є—Е. –¶—Ц –≤—Ц—А—Г—Б–Є –є –і–∞–ї—Ц –Љ–∞–ї–Њ–≤–Є–≤—З–µ–љ—Ц, —Ц –і–µ—П–Ї—Ц –њ–Њ–≤—Ц–і–Њ–Љ–ї–µ–љ–љ—П –њ—А–Њ –≤—Ц–і–Ї—А–Є—В—В—П —Б–ї—Ц–і –њ—А–Є–є–Љ–∞—В–Є –Њ–±–µ—А–µ–ґ–љ–Њ, –њ–Њ–Ї–Є –≤—Ц—А—Г—Б–љ–∞ –њ—А–Є—А–Њ–і–∞ —Ж–Є—Е —Е–≤–Њ—А–Њ–± –љ–µ –±—Г–і–µ –Њ—Б—В–∞—В–Њ—З–љ–Њ –і–Њ–≤–µ–і–µ–љ–∞. –Ъ—А—Ц–Љ —В–Њ–≥–Њ, –љ–µ–Њ–±—Е—Ц–і–љ–Њ —В–∞–Ї–Њ–ґ –њ–µ—А–µ–≤—Ц—А–Є—В–Є —Ц–љ—Д–µ–Ї—В–Є–≤–љ—Ц—Б—В—М —Ц–Ј–Њ–ї—М–Њ–≤–∞–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Й–Њ–і–Њ –љ–µ—Ц–љ—Д—Ц–Ї–Њ–≤–∞–љ–Є—Е –≥–Њ—Б–њ–Њ–і–∞—А—Ц–≤ —В–Њ–≥–Њ –ґ –≤–Є–і—Г, —Г —П–Ї–Њ–≥–Њ —Ж—Ц –≤—Ц—А—Г—Б–Є –≤–Є—П–≤–ї–µ–љ–Њ[ 205]
–Э–Є–љ—Ц –≤–Є–і—Ц–ї–µ–љ–Њ –Њ–Ї—А–µ–Љ–∞ —А–Њ–і–Є–љ–∞ –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –≤—А–∞–ґ–∞—О—В—М –≥–Њ–ї–Њ–≤–љ–Є–Љ —З–Є–љ–Њ–Љ —З–ї–µ–љ–Є—Б—В–Њ–љ–Њ–≥–Є—Е, –Њ—Б–Њ–±–ї–Є–≤–Њ –Ї–Њ–Љ–∞—Е, —П–Ї—Ц –ґ–Є–≤—Г—В—М —Г –≤–Њ–і–љ–Є—Е —Ц –≤–Њ–ї–Њ–≥–Є—Е —Б–µ—А–µ–і–Њ–≤–Є—Й–∞—Е: —Ц—А–Є–і–Њ–≤—Ц—А—Г—Б–Є [en] –∞–љ–≥–ї. Invertebrate iridescent viruses вАФ ¬Ђ–≤–µ—Б–µ–ї–Ї–Њ–≤—Ц –≤—Ц—А—Г—Б–Є –±–µ–Ј—Е—А–µ–±–µ—В–љ–Є—Е¬ї; —В–∞–Ї–Њ–≥–Њ –Ї–Њ–ї—М–Њ—А—Г –Ј—А–∞–Ј–Ї–Є —Г—А–∞–ґ–µ–љ–Є—Е –Ї–Њ–Љ–∞—Е). –¶–µ —Ц–Ї–Њ—Б–∞–µ–і—А–Є—З–љ—Ц —З–∞—Б—В–Є–љ–Ї–Є –і—Ц–∞–Љ–µ—В—А–Њ–Љ 120вАФ180 –љ–Љ , —Й–Њ –Љ—Ц—Б—В—П—В—М –≤–љ—Г—В—А—Ц—И–љ—О –ї—Ц–њ—Ц–і–љ—Г –Љ–µ–Љ–±—А–∞–љ—Г —Ц –≥–µ–љ–Њ–Љ —Г –≤–Є–≥–ї—П–і—Ц –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Њ—Ч –Ф–Э–Ъ , —Й–Њ –Љ—Ц—Б—В–Є—В—М 130вАФ210 —В–Є—Б. –њ–∞—А –љ—Г–Ї–ї–µ–Њ—В–Є–і—Ц–≤ [ 206]
–Ж–љ—И—Ц –≤—Ц—А—Г—Б–Є, —Й–Њ –≤—А–∞–ґ–∞—О—В—М –Ї–Њ–Љ–∞—Е: —А–Њ–і–Є–љ–∞ Baculoviridae Entomopoxvirinae [en] –Я–Њ–Ї—Б–≤—Ц—А—Г—Б–Є Densovirus [en] Parvoviridae [en] –†–∞–±–і–Њ–≤—Ц—А—Г—Б–Є –†–µ–Њ–≤—Ц—А—Г—Б–Є –Я—Ц–Ї–Њ—А–љ–∞–≤—Ц—А—Г—Б [ 207]
–ѓ–Ї —Ц –≤—Б—Ц –±–µ–Ј—Е—А–µ–±–µ—В–љ—Ц, –Љ–µ–і–Њ–љ–Њ—Б–љ–∞ –±–і–ґ–Њ–ї–∞ —З—Г—В–ї–Є–≤–∞ –і–Њ –±–∞–≥–∞—В—М–Њ—Е –≤—Ц—А—Г—Б–љ–Є—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є[ 208]
–Я–µ—А—Ж—Ц , —Г—А–∞–ґ–µ–љ—Ц –≤—Ц—А—Г—Б–Њ–Љ –њ–ї—П–Љ–Є—Б—В–Њ—Б—В—Ц–Ж—Б–љ—Г—Ф –±–∞–≥–∞—В–Њ —В–Є–њ—Ц–≤ –≤—Ц—А—Г—Б—Ц–≤ —А–Њ—Б–ї–Є–љ . –І–∞—Б—В–Њ –≤–Њ–љ–Є —Б–њ—А–Є—З–Є–љ—П—О—В—М –Ј–љ–Є–ґ–µ–љ–љ—П –≤—А–Њ–ґ–∞–є–љ–Њ—Б—В—Ц , –Ј–∞–≤–і–∞—О—З–Є –Ј–љ–∞—З–љ–Є—Е –Ј–±–Є—В–Ї—Ц–≤ —Б—Ц–ї—М—Б—М–Ї–Њ–Љ—Г –≥–Њ—Б–њ–Њ–і–∞—А—Б—В–≤—Г, —В–Њ–Љ—Г –Ї–Њ–љ—В—А–Њ–ї—М —В–∞–Ї–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Ф –і—Г–ґ–µ –≤–∞–ґ–ї–Є–≤–Є–Љ –Ј –µ–Ї–Њ–љ–Њ–Љ—Ц—З–љ–Њ–≥–Њ –њ–Њ–≥–ї—П–і—Г[ 209] –њ–µ—А–µ–љ–Њ—Б–љ–Є–Ї–Є . –Ч–∞–Ј–≤–Є—З–∞–є —Ж–µ –Ї–Њ–Љ–∞—Е–Є, –∞–ї–µ –љ–Є–Љ–Є –Љ–Њ–ґ—Г—В—М –±—Г—В–Є —В–∞–Ї–Њ–ґ –≥—А–Є–±–Є, —З–µ—А–≤–Є-–љ–µ–Љ–∞—В–Њ–і–Є —Ц –Њ–і–љ–Њ–Ї–ї—Ц—В–Є–љ–љ—Ц –Њ—А–≥–∞–љ—Ц–Ј–Љ–Є . –ѓ–Ї—Й–Њ –Ї–Њ–љ—В—А–Њ–ї—М –≤—Ц—А—Г—Б—Г —А–Њ—Б–ї–Є–љ –≤–Є–Ј–љ–∞—О—В—М –µ–Ї–Њ–љ–Њ–Љ—Ц—З–љ–Њ –≤–Є–≥—Ц–і–љ–Є–Љ, –љ–∞–њ—А–Є–Ї–ї–∞–і, —Г –≤–Є–њ–∞–і–Ї—Г –±–∞–≥–∞—В–Њ—А—Ц—З–љ–Є—Е —Д—А—Г–Ї—В–Њ–≤–Є—Е –і–µ—А–µ–≤, –Ј—Г—Б–Є–ї–ї—П —Б–њ—А—П–Љ–Њ–≤—Г—О—В—М –љ–∞ —Г—Б—Г–љ–µ–љ–љ—П –њ–µ—А–µ–љ–Њ—Б–љ–Є–Ї—Ц–≤ –∞–±–Њ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ–Є—Е –≥–Њ—Б–њ–Њ–і–∞—А—Ц–≤, –љ–∞–њ—А–Є–Ї–ї–∞–і, –±—Г—А'—П–љ—Ц–≤. –Т—Ц—А—Г—Б–Є —А–Њ—Б–ї–Є–љ –љ–µ –Љ–Њ–ґ—Г—В—М –≤—А–∞–ґ–∞—В–Є –ї—О–і–Є–љ—Г —В–∞ —Ц–љ—И–Є—Е —В–≤–∞—А–Є–љ, –±–Њ –≤–Њ–љ–Є –Љ–Њ–ґ—Г—В—М —А–Њ–Ј–Љ–љ–Њ–ґ—Г–≤–∞—В–Є—Б—П –ї–Є—И–µ —Г –ґ–Є–≤–Є—Е —А–Њ—Б–ї–Є–љ–љ–Є—Е –Ї–ї—Ц—В–Є–љ–∞—Е.
–†–Њ—Б–ї–Є–љ–Є –Љ–∞—О—В—М —Б–Ї–ї–∞–і–љ—Ц —В–∞ –µ—Д–µ–Ї—В–Є–≤–љ—Ц –Љ–µ—Е–∞–љ—Ц–Ј–Љ–Є –Ј–∞—Е–Є—Б—В—Г –≤—Ц–і –≤—Ц—А—Г—Б—Ц–≤. –Э–∞–є–µ—Д–µ–Ї—В–Є–≤–љ—Ц—И–Є–Љ –Љ–µ—Е–∞–љ—Ц–Ј–Љ–Њ–Љ —Ф –љ–∞—П–≤–љ—Ц—Б—В—М —В–∞–Ї –Ј–≤–∞–љ–Њ–≥–Њ –≥–µ–љ–∞ —Б—В—Ц–є–Ї–Њ—Б—В—Ц (R –≤—Ц–і –∞–љ–≥–ї. resistance вАФ ¬Ђ—Б—В—Ц–є–Ї—Ц—Б—В—М¬ї). –Ъ–Њ–ґ–µ–љ R-–≥–µ–љ –≤—Ц–і–њ–Њ–≤—Ц–і–∞—Ф –Ј–∞ —Б—В—Ц–є–Ї—Ц—Б—В—М –і–Њ –Њ–Ї—А–µ–Љ–Њ–≥–Њ –≤—Ц—А—Г—Б—Г —Ц —Б–њ—А–Є—З–Є–љ—О—Ф –Ј–∞–≥–Є–±–µ–ї—М –Ї–ї—Ц—В–Є–љ, —Б—Г—Б—Ц–і–љ—Ц—Е –Ј —Г—А–∞–ґ–µ–љ–Њ—Ч, —Й–Њ –љ–µ–Њ–Ј–±—А–Њ—Ф–љ–Є–Љ –Њ–Ї–Њ–Љ –≤–Є–і–љ–Њ —П–Ї –≤–µ–ї–Є–Ї–∞ –њ–ї—П–Љ–∞. –¶–µ –Ј—Г–њ–Є–љ—П—Ф —А–Њ–Ј–≤–Є—В–Њ–Ї —Е–≤–Њ—А–Њ–±–Є –≤–љ–∞—Б–ї—Ц–і–Њ–Ї –Ј—Г–њ–Є–љ–Ї–Є –њ–Њ—И–Є—А–µ–љ–љ—П –≤—Ц—А—Г—Б—Г[ 212] –†–Э–Ъ-—Ц–љ—В–µ—А—Д–µ—А–µ–љ—Ж—Ц—П . –£—А–∞–ґ–µ–љ—Ц –≤—Ц—А—Г—Б–Њ–Љ —А–Њ—Б–ї–Є–љ–Є —З–∞—Б—В–Њ –њ–Њ—З–Є–љ–∞—О—В—М –≤–Є—А–Њ–±–ї—П—В–Є –њ—А–Є—А–Њ–і–љ—Ц –њ—А–Њ—В–Є–≤—Ц—А—Г—Б–љ—Ц —А–µ—З–Њ–≤–Є–љ–Є, —П–Ї-–Њ—В —Б–∞–ї—Ц—Ж–Є–ї–Њ–≤–∞ –Ї–Є—Б–ї–Њ—В–∞ , –Њ–Ї—Б–Є–і –∞–Ј–Њ—В—Г —В–∞ –∞–Ї—В–Є–≤–љ—Ц —Д–Њ—А–Љ–Є –Ї–Є—Б–љ—О [ 214]
–Т—Ц—А—Г—Б–Є —А–Њ—Б–ї–Є–љ —Ц —Б—В–≤–Њ—А–µ–љ—Ц –љ–∞ —Ч—Е –Њ—Б–љ–Њ–≤—Ц –≤—Ц—А—Г—Б–Њ–њ–Њ–і—Ц–±–љ—Ц —З–∞—Б—В–Є–љ–Ї–Є (VLPs) –Ј–љ–∞–є—И–ї–Є –Ј–∞—Б—В–Њ—Б—Г–≤–∞–љ–љ—П –≤ –±—Ц–Њ—В–µ—Е–љ–Њ–ї–Њ–≥—Ц—Ч —В–∞ –љ–∞–љ–Њ—В–µ—Е–љ–Њ–ї–Њ–≥—Ц—Ч . –Ъ–∞–њ—Б–Є–і–Є –±—Ц–ї—М—И–Њ—Б—В—Ц –≤—Ц—А—Г—Б—Ц–≤ —А–Њ—Б–ї–Є–љ –Љ–∞—О—В—М –њ—А–Њ—Б—В—Г —Ц —Б—В—Ц–є–Ї—Г —Б—В—А—Г–Ї—В—Г—А—Г, —Ц –≤—Ц—А—Г—Б–љ—Ц —З–∞—Б—В–Є–љ–Ї–Є –Љ–Њ–ґ—Г—В—М –≤–Є—А–Њ–±–ї—П—В–Є—Б—П —Г –≤–µ–ї–Є—З–µ–Ј–љ–Є—Е –Ї—Ц–ї—М–Ї–Њ—Б—В—П—Е —П–Ї —Г—А–∞–ґ–µ–љ–Њ—О —А–Њ—Б–ї–Є–љ–Њ—О, —В–∞–Ї —Ц —А—Ц–Ј–љ–Є–Љ–Є –≥–µ—В–µ—А–Њ–ї–Њ–≥—Ц—З–љ–Є–Љ–Є —Б–Є—Б—В–µ–Љ–∞–Љ–Є. –Т—Ц—А—Г—Б–Є —А–Њ—Б–ї–Є–љ –Љ–Њ–ґ—Г—В—М –Ј–Љ—Ц–љ—О–≤–∞—В–Є—Б—П —Е—Ц–Љ—Ц—З–љ–Њ —Ц –≥–µ–љ–µ—В–Є—З–љ–Њ, –Њ—В–Њ—З—Г—О—З–Є –Њ–±–Њ–ї–Њ–љ–Ї–Њ—О —З—Г–ґ–Њ—А—Ц–і–љ—Ц —З–∞—Б—В–Є–љ–Ї–Є, –∞ —В–∞–Ї–Њ–ґ –Ј–і–∞—В–љ—Ц –≤–±—Г–і–Њ–≤—Г–≤–∞—В–Є—Б—П –≤ –љ–∞–і–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Ц —Б—В—А—Г–Ї—В—Г—А–Є, —Й–Њ –≤–Љ–Њ–ґ–ї–Є–≤–ї—О—Ф —Ч—Е –Ј–∞—Б—В–Њ—Б—Г–≤–∞–љ–љ—П –≤ –±—Ц–Њ—В–µ—Е–љ–Њ–ї–Њ–≥—Ц—П—Е[ 215]
–Т—Ц—А—Г—Б–Є –≥—А–Є–±—Ц–≤ –љ–∞–Ј–Є–≤–∞—О—В—М –Љ—Ц–Ї–Њ–≤—Ц—А—Г—Б–∞–Љ–Є . –Э–Є–љ—Ц –≤—Ц—А—Г—Б–Є –≤–Є–і—Ц–ї–µ–љ–Њ –≤ 73 –≤–Є–і—Ц–≤ –Ј 57 —А–Њ–і—Ц–≤, —Й–Њ –љ–∞–ї–µ–ґ–∞—В—М –і–Њ 5 –Ї–ї–∞—Б—Ц–≤[ 216] [ 217] –†–Э–Ъ . –Ч–∞–Ј–≤–Є—З–∞–є, –≤—Ц—А—Г—Б–Є –≥—А–Є–±—Ц–≤ –≤—Ц–і–љ–Њ—Б–љ–Њ –љ–µ—И–Ї—Ц–і–ї–Є–≤—Ц. –Ф–µ—П–Ї—Ц –≥—А–Є–±–љ—Ц —И—В–∞–Љ–Є –Љ–Њ–ґ—Г—В—М –≤—А–∞–ґ–∞—В–Є—Б—П –±–∞–≥–∞—В—М–Љ–∞ –≤—Ц—А—Г—Б–∞–Љ–Є, –∞–ї–µ –±—Ц–ї—М—И—Ц—Б—В—М –Љ—Ц–Ї–Њ–≤—Ц—А—Г—Б—Ц–≤ —В—Ц—Б–љ–Њ –њ–Њ–≤'—П–Ј–∞–љ—Ц –Ј—Ц —Б–≤–Њ—Ч–Љ —Ф–і–Є–љ–Є–Љ —Е–∞–Ј—П—Ч–љ–Њ–Љ, –≤—Ц–і —П–Ї–Њ–≥–Њ –њ–µ—А–µ–і–∞—О—В—М—Б—П –є–Њ–≥–Њ –љ–∞—Й–∞–і–Ї–∞–Љ. –Э–∞–і –Ї–ї–∞—Б–Є—Д—Ц–Ї–∞—Ж—Ц—Ф—О –≤—Ц—А—Г—Б—Ц–≤ –≥—А–Є–±—Ц–≤ –љ–Є–љ—Ц –њ—А–∞—Ж—О—Ф —Б–њ–µ—Ж—Ц–∞–ї—М–љ–Њ —Б—В–≤–Њ—А–µ–љ–Є–є –≤—Ц–і–і—Ц–ї —Г —Б–Ї–ї–∞–і—Ц ICTV . –Э–Є–љ—Ц –≤—Ц–љ –≤–Є–Ј–љ–∞—Ф 3 —А–Њ–і–Є–љ–Є –≤—Ц—А—Г—Б—Ц–≤ –≥—А–Є–±—Ц–≤, –∞ –љ–∞–є–±—Ц–ї—М—И –≤–Є–≤—З–µ–љ—Ц –Љ—Ц–Ї–Њ–≤—Ц—А—Г—Б–Є –љ–∞–ї–µ–ґ–∞—В—М –і–Њ —А–Њ–і–Є–љ–Є Totiviridae [ 218]
–Т—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —Й–Њ –∞–љ—В–Є–≤—Ц—А—Г—Б–љ–∞ –∞–Ї—В–Є–≤–љ—Ц—Б—В—М –њ–µ–љ—Ц—Ж–Є–ї—Ц–љ–Њ–≤–Є—Е –≥—А–Є–±—Ц–≤ –Ј—Г–Љ–Њ–≤–ї–µ–љ–∞ —Ц–љ–і—Г–Ї—Ж—Ц—Ф—О —Ц–љ—В–µ—А—Д–µ—А–Њ–љ—Г –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤–Њ—Ч –†–Э–Ъ –≤—Ц–і –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –≤—А–∞–ґ–∞—О—В—М –≥—А–Є–±–Є[ 216]
–ѓ–Ї—Й–Њ –ґ –≤—Ц—А—Г—Б, –њ–Њ—В—А–∞–њ–ї—П—О—З–Є –≤ –≥—А–Є–±, –њ—А–Њ—П–≤–ї—П—Ф —Б–≤–Њ—О –≤—Ц—А—Г–ї–µ–љ—В–љ—Ц—Б—В—М , —В–Њ —А–µ–∞–Ї—Ж—Ц—П –≥—А–Є–±–∞ –љ–∞ —Ж–µ –Љ–Њ–ґ–µ –±—Г—В–Є —А—Ц–Ј–љ–Њ—О: –Ј–љ–Є–ґ–µ–љ–љ—П –∞–±–Њ –њ—Ц–і–≤–Є—Й–µ–љ–љ—П –≤—Ц—А—Г–ї–µ–љ—В–љ–Њ—Б—В—Ц —Г –њ–∞—В–Њ–≥–µ–љ–љ–Є—Е –≤–Є–і—Ц–≤, –і–µ–≥–µ–љ–µ—А–∞—Ж—Ц—П –≥—А–Є–±–љ–Є—Ж—Ц —В–∞ –њ–ї–Њ–і–Њ–≤–Є—Е —В—Ц–ї , –Ј–Љ—Ц–љ–∞ –Ј–∞–±–∞—А–≤–ї–µ–љ–љ—П, –њ—А–Є–і—Г—И–µ–љ–љ—П —Б–њ–Њ—А–Њ–љ–Њ—И–µ–љ–љ—П . –Э–µ–Ї–∞–њ—Б–Є–і–Њ–≤–∞–љ—Ц –≤—Ц—А—Г—Б–љ—Ц –†–Э–Ъ –њ–µ—А–µ–і–∞—О—В—М—Б—П —З–µ—А–µ–Ј –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј–Є –љ–µ–Ј–∞–ї–µ–ґ–љ–Њ –≤—Ц–і –Љ—Ц—В–Њ—Е–Њ–љ–і—А—Ц–є .
–Т—Ц—А—Г—Б–љ—Ц –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П –Љ–Њ–ґ—Г—В—М –Ј–∞–≤–і–∞–≤–∞—В–Є —И–Ї–Њ–і–Є –≥—А–Є–±—Ц–≤–љ–Є—З–Є–Љ –њ—Ц–і–њ—А–Є—Ф–Љ—Б—В–≤–∞–Љ, –љ–∞–њ—А–Є–Ї–ї–∞–і, —Б–њ—А–Є—З–Є–љ–Є—В–Є –њ–Њ—А—Г–і—Ц–љ–љ—П –њ–ї–Њ–і–Њ–≤–Є—Е —В—Ц–ї –њ–µ—З–µ—А–Є—Ж—Ц , –Ј–Љ—Ц–љ—Г –Ј–∞–±–∞—А–≤–ї–µ–љ–љ—П —Г –Ј–Є–Љ–Њ–≤–Њ–≥–Њ –Њ–њ–µ–љ—М–Ї–∞ , —Й–Њ –Ј–љ–Є–ґ—Г—Ф —Ч—Е –Ї–Њ–Љ–µ—А—Ж—Ц–є–љ—Г —Ж—Ц–љ–љ—Ц—Б—В—М. –Т—Ц—А—Г—Б–Є, —Й–Њ –њ–Њ—А–Њ–і–ґ—Г—О—В—М –≥—Ц–њ–Њ–≤—Ц—А—Г–ї–µ–љ—В–љ—Ц—Б—В—М –≥—А–Є–±—Ц–≤-–њ–∞—В–Њ–≥–µ–љ—Ц–≤, –Љ–Њ–ґ–љ–∞ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞—В–Є –і–ї—П –±–Њ—А–Њ—В—М–±–Є —Ц–Ј –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ–љ—П–Љ–Є —А–Њ—Б–ї–Є–љ[ 219] [ 220]
–Ф–Њ –≤—Ц—А—Г—Б—Ц–≤ –њ—А–Њ—В–Є—Б—В—Ц–≤ –≤—Ц–і–љ–Њ—Б—П—В—М –≤—Ц—А—Г—Б–Є, —Й–Њ –≤—А–∞–ґ–∞—О—В—М –Њ–і–љ–Њ–Ї–ї—Ц—В–Є–љ–љ–Є—Е –µ—Г–Ї–∞—А—Ц–Њ—В—Ц–≤ , –љ–µ –≤–Ї–ї—О—З–µ–љ–Є—Е —Г —Ж–∞—А—Б—В–≤–Њ —В–≤–∞—А–Є–љ–Є , —А–Њ—Б–ї–Є–љ–Є –∞–±–Њ –≥—А–Є–±–Є . –Ф–µ—П–Ї—Ц –Ј –≤—Ц–і–Њ–Љ–Є—Е –љ–Є–љ—Ц –≤—Ц—А—Г—Б—Ц–≤ –њ—А–Њ—В–Є—Б—В—Ц–≤[ 221]
–Э–∞–Ј–≤–∞ –≤—Ц—А—Г—Б—Г (—А—Ц–і)
–°–Є—Б—В–µ–Љ–∞—В–Є—З–љ–µ –њ–Њ–ї–Њ–ґ–µ–љ–љ—П
–£—А–∞–ґ–µ–љ–Є–є –њ—А–Њ—В–Є—Б—В
Dinornavirus
Alvernaviridae
Heterocapsa circularisquama
Endornavirus
Endornaviridae
–§—Ц—В–Њ—Д—В–Њ—А–∞
Labyrnavirus
Labyrnaviridae
Aurantiochytrium
Marnavirus
Marnaviridae
Heterosigma akashiwo
Marseillevirus
Marseilleviridae
–Р–Љ–µ–±–∞
–Ь—Ц–Љ—Ц–≤—Ц—А—Г—Б Mimiviridae
Acanthamoeba polyphaga
Chlorovirus
Phycodnaviridae
Paramecium bursaria
Coccolithovirus
Phycodnaviridae
Emiliania huxleyi
Prasinovirus
Phycodnaviridae
Micromonas pusilla
Prymnesiovirus
Phycodnaviridae
Chrysochromulina brevifilum
Raphidovirus
Phycodnaviridae
Heterosigma akashiwo
Cryspovirus
Partitiviridae
Cryptosporidium parvum
Hemivirus
Pseudoviridae
Volvox carteri
Pseudovirus
Pseudoviridae
Physarum polycephalum
Mimoreovirus
–†–µ–Њ–≤—Ц—А—Г—Б–Є Micromonas pusilla
Giardiavirus
Totiviridae
Giardia lamblia
Leishmaniavirus
Totiviridae
–Ы–µ–є—И–Љ–∞–љ—Ц—П
Trichomonasvirus
Totiviridae
–Ґ—А–Є—Е–Њ–Љ–Њ–љ–∞–і–∞ –≤–∞–≥—Ц–љ–∞–ї—М–љ–∞
Bacilladnavirus
–Э–µ –≤–Є–Ј–љ–∞—З–µ–љ–Њ
Chaetoceros salsugineum Rhizosolenia setigera
Dinodnavirus
–Э–µ –≤–Є–Ј–љ–∞—З–µ–љ–Њ
Heterocapsa circularisquama
Rhizidiovirus
–Э–µ –≤–Є–Ј–љ–∞—З–µ–љ–Њ
Rhizidiomyces
–С–∞–≥–∞—В–Њ –≤—Ц—А—Г—Б—Ц–≤ –љ–∞–є–њ—А–Њ—Б—В—Ц—И–Є—Е –Љ–∞—О—В—М –љ–µ–Ј–≤–Є—З–∞–є–љ–Њ –≤–µ–ї–Є–Ї—Ц —А–Њ–Ј–Љ—Ц—А–Є. –Э–∞–њ—А–Є–Ї–ї–∞–і, –≥–µ–љ–Њ–Љ Marseillevirus [en] –∞–Љ–µ–±–Є , –Љ–∞—Ф –≥–µ–љ–Њ–Љ —А–Њ–Ј–Љ—Ц—А–Њ–Љ 368 –Ъ–С, –∞ Mamavirus [en] Acanthamoeba –Љ—Ц–Љ—Ц–≤—Ц—А—Г—Б (–∞ –є–Њ–≥–Њ –Ї–∞–њ—Б–Є–і —Б—П–≥–∞—Ф –±–ї–Є–Ј—М–Ї–Њ 500 –љ–Љ –≤ –і—Ц–∞–Љ–µ—В—А—Ц) —В–∞ –і–µ—П–Ї—Ц –±–∞–Ї—В–µ—А—Ц—Ч . –Ґ–∞–Ї–Њ–ґ –і–Њ –≥—Ц–≥–∞–љ—В—Б—М–Ї–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –љ–∞–ї–µ–ґ–Є—В—М –≤—Ц—А—Г—Б, —Й–Њ –≤—А–∞–ґ–∞—Ф –њ–Њ—И–Є—А–µ–љ–Њ–≥–Њ –Љ–Њ—А—Б—М–Ї–Њ–≥–Њ –њ—А–Њ—В–Є—Б—В–∞ Cafeteria roenbergensis [en] –∞–љ–≥–ї. Cafeteria roenbergensis virus, CroV )[ 222]
–Х–ї–µ–Ї—В—А–Њ–љ–љ–∞ –Љ—Ц–Ї—А–Њ—Д–Њ—В–Њ–≥—А–∞—Д—Ц—П –±–µ–Ј–ї—Ц—З—Ц –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥—Ц–≤, —Й–Њ –њ—А–Є–Ї—А—Ц–њ–ї—О—О—В—М—Б—П –і–Њ –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Њ—Ч –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч —Б—В—Ц–љ–Ї–Є –С–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥–Є —Ф –њ–Њ—И–Є—А–µ–љ–Њ—О –є —А—Ц–Ј–љ–Њ–Љ–∞–љ—Ц—В–љ–Њ—О –≥—А—Г–њ–Њ—О –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ —З–Є—Б–µ–ї—М–љ—Ц—И–∞ —Г –≤–Њ–і–љ–Є—Е —Б–µ—А–µ–і–Њ–≤–Є—Й–∞—Е –њ—А–Њ–ґ–Є–≤–∞–љ–љ—П вАФ –≤ –Њ–Ї–µ–∞–љ–∞—Е —Ж–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Г –њ–Њ–љ–∞–і 10 —А–∞–Ј—Ц–≤ –±—Ц–ї—М—И–µ, –љ—Ц–ґ –±–∞–Ї—В–µ—А—Ц–є [ 223] [ 224] –Ї–ї—Ц—В–Є–љ–љ–Є–Љ–Є —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –љ–∞ –њ–Њ–≤–µ—А—Е–љ—Ц –Ї–ї—Ц—В–Є–љ–Є —Ц –њ–Њ—В—Ц–Љ –њ—А–Њ—Е–Њ–і—П—З–Є –≤—Б–µ—А–µ–і–Є–љ—Г –љ–µ—Ч. –Я—А–Њ—В—П–≥–Њ–Љ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ –њ—А–Њ–Љ—Ц–ґ–Ї—Г —З–∞—Б—Г (—Ц–љ–Њ–і—Ц –ї—Ц—З–µ–љ–Є—Е —Е–≤–Є–ї–Є–љ) –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–∞ –њ–Њ–ї—Ц–Љ–µ—А–∞–Ј–∞ –њ–Њ—З–Є–љ–∞—Ф —В—А–∞–љ—Б–ї—О–≤–∞—В–Є –≤—Ц—А—Г—Б–љ—Г –Љ–†–Э–Ъ –≤ –±—Ц–ї–Ї–Є. –¶—Ц –±—Ц–ї–Ї–Є –∞–±–Њ –≤—Е–Њ–і—П—В—М –і–Њ —Б–Ї–ї–∞–і—Г –≤—Ц—А—Ц–Њ–љ—Ц–≤, —Й–Њ –љ–∞–Ї–Њ–њ–Є—З—Г—О—В—М—Б—П –≤—Б–µ—А–µ–і–Є–љ—Ц –Ї–ї—Ц—В–Є–љ–Є, –∞–±–Њ —Ф –і–Њ–њ–Њ–Љ—Ц–ґ–љ–Є–Љ–Є –±—Ц–ї–Ї–∞–Љ–Є, —Й–Њ –і–Њ–њ–Њ–Љ–∞–≥–∞—О—В—М —Б–Ї–ї–∞–і–∞–љ–љ—О –љ–Њ–≤–Є—Е –≤—Ц—А—Ц–Њ–љ—Ц–≤, –∞–±–Њ —Б–њ—А–Є—З–Є–љ—О—О—В—М –ї—Ц–Ј–Є—Б –Ї–ї—Ц—В–Є–љ–Є. –Т—Ц—А—Г—Б–љ—Ц —Д–µ—А–Љ–µ–љ—В–Є —Б–њ—А–Є—З–Є–љ—О—О—В—М —А—Г–є–љ—Г–≤–∞–љ–љ—П –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч –Љ–µ–Љ–±—А–∞–љ–Є , —Ц, —П–Ї —Г –≤–Є–њ–∞–і–Ї—Г —Д–∞–≥–∞ –Ґ4 , –ї–Є—И–µ —З–µ—А–µ–Ј 20 —Е–≤–Є–ї–Є–љ –њ—Ц—Б–ї—П –њ—А–Њ–љ–Є–Ї–љ–µ–љ–љ—П –≤ –Ї–ї—Ц—В–Є–љ—Г –≤–Є–љ–Є–Ї–∞—О—В—М –њ–Њ–љ–∞–і —В—А–Є—Б—В–∞ –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥—Ц–≤.
–У–Њ–ї–Њ–≤–љ–Є–Љ –Љ–µ—Е–∞–љ—Ц–Ј–Љ–Њ–Љ –Ј–∞—Е–Є—Б—В—Г –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Є—Е –Ї–ї—Ц—В–Є–љ –≤—Ц–і –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥—Ц–≤ —Ф —Г—В–≤–Њ—А–µ–љ–љ—П —Д–µ—А–Љ–µ–љ—В—Ц–≤, —Й–Њ —А—Г–є–љ—Г—О—В—М —З—Г–ґ–Њ—А—Ц–і–љ—Г –Ф–Э–Ъ . –¶—Ц —Д–µ—А–Љ–µ–љ—В–Є, –Ј–≤–∞–љ—Ц –µ–љ–і–Њ–љ—Г–Ї–ї–µ–∞–Ј–∞–Љ–Є —А–µ—Б—В—А–Є–Ї—Ж—Ц—Ч , ¬Ђ—А–Њ–Ј—А—Ц–Ј–∞—О—В—М¬ї –≤—Ц—А—Г—Б–љ—Г –Ф–Э–Ъ, –≤–њ–Њ—А—Б–љ—Г—В—Г –≤—Б–µ—А–µ–і–Є–љ—Г –Ї–ї—Ц—В–Є–љ–Є[ 226] CRISPR , —П–Ї–∞ –Ј–±–µ—А—Ц–≥–∞—Ф —Ц–љ—Д–Њ—А–Љ–∞—Ж—Ц—О –њ—А–Њ –≥–µ–љ–Њ–Љ–Є –≤—Ц—А—Г—Б—Ц–≤, –Ј —П–Ї–Є–Љ–Є –±–∞–Ї—В–µ—А—Ц—П —Б—В–Є–Ї–∞–ї–∞—Б—П —А–∞–љ—Ц—И–µ, —Ц —Ж–µ –і–Њ–Ј–≤–Њ–ї—П—Ф –Ї–ї—Ц—В–Є–љ—Ц –±–ї–Њ–Ї—Г–≤–∞—В–Є —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—О –≤—Ц—А—Г—Б—Г –Ј–∞ –і–Њ–њ–Њ–Љ–Њ–≥–Њ—О —Ц–љ—В–µ—А—Д–µ—А–µ–љ—Ж—Ц—Ч –†–Э–Ъ [ 227] [ 228] —Ц–Љ—Г–љ—Ц—В–µ—В –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Њ—Ч –Ї–ї—Ц—В–Є–љ–Є.
–С–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥–Є –Љ–Њ–ґ—Г—В—М –≤–Є–Ї–Њ–љ—Г–≤–∞—В–Є —Ц –Ї–Њ—А–Є—Б–љ—Г –і–ї—П –±–∞–Ї—В–µ—А—Ц–є —Д—Г–љ–Ї—Ж—Ц—О, –њ—А–Є–Љ—Ц—А–Њ–Љ, —Б–∞–Љ–µ –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥, —Й–Њ –Ј–∞—А–∞–ґ–∞—Ф –і–Є—Д—В–µ—А—Ц–є–љ—Ц –њ–∞–ї–Є—З–Ї–Є , –Ї–Њ–і—Г—Ф –≥–µ–љ —Ч—Е–љ—М–Њ–≥–Њ —В–Њ–Ї—Б–Є–љ—Г, –њ–Њ—В—А—Ц–±–љ–Њ–≥–Њ —Ж–Є–Љ –±–∞–Ї—В–µ—А—Ц—П–Љ —Ц —В–∞–Ї–Њ–≥–Њ –љ–µ–±–µ–Ј–њ–µ—З–љ–Њ–≥–Њ –і–ї—П –ї—О–і–Є–љ–Є[ 229] :45
Sulfolobus Sulfolobus tengchongensis spindle-shaped virus 1 [ 230] [ 231] [ 232] [ 233] [ 234] –Љ–Ї–Љ –Ф–µ—П–Ї—Ц –≤—Ц—А—Г—Б–Є —А–Њ–Ј–Љ–љ–Њ–ґ—Г—О—В—М—Б—П –≤—Б–µ—А–µ–і–Є–љ—Ц –∞—А—Е–µ–є : —Ж–µ –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Ц –Ф–Э–Ъ-–≤–Љ—Ц—Б–љ—Ц –≤—Ц—А—Г—Б–Є –љ–µ–Ј–≤–Є—З–∞–є–љ–Њ—Ч, —З–∞—Б–Њ–Љ —Г–љ—Ц–Ї–∞–ї—М–љ–Њ—Ч —Д–Њ—А–Љ–Є[ 5] [ 235] —В–µ—А–Љ–Њ—Д—Ц–ї—М–љ–Є—Е –∞—А—Е–µ–є, –Ј–Њ–Ї—А–µ–Љ–∞, –њ–Њ—А—П–і–Ї—Ц–≤ Sulfolobales Thermoproteales [ 236] –†–Э–Ъ-—Ц–љ—В–µ—А—Д–µ—А–µ–љ—Ж—Ц—П –≤—Ц–і –њ–Њ–≤—В–Њ—А—О–≤–∞–љ–Є—Е –њ–Њ—Б–ї—Ц–і–Њ–≤–љ–Њ—Б—В–µ–є –Ф–Э–Ъ [en] [ 237] [ 238]
–Т—Ц—А–Њ—Д–∞–≥ –°—Г–њ—Г—В–љ–Є–Ї –Я—Ц–і —З–∞—Б –≤–Є–≤—З–µ–љ–љ—П –≤—Ц—А—Г—Б–љ–Є—Е —Д–∞–±—А–Є–Ї –Љ—Ц–Љ—Ц–≤—Ц—А—Г—Б—Г –≤–Є—П–≤–ї–µ–љ–Њ, —Й–Њ –љ–∞ –љ–Є—Е –Ј–±–Є—А–∞—О—В—М—Б—П –љ–µ–≤–µ–ї–Є–Ї—Ц –≤—Ц—А—Ц–Њ–љ–Є –є —Ц–љ—И–Њ–≥–Њ –≤—Ц—А—Г—Б—Г, —П–Ї–Њ–≥–Њ –љ–∞–Ј–≤–∞–ї–Є –°—Г–њ—Г—В–љ–Є–Ї–Њ–Љ [ 239] –≤—Ц—А—Г—Б-—Б–∞—В–µ–ї—Ц—В . –°—Г–њ—Г—В–љ–Є–Ї —Б—В–∞–≤ –њ–µ—А—И–Є–Љ –≤—Ц–і–Њ–Љ–Є–Љ –≤—Ц—А—Г—Б–Њ–Љ-—Б–∞—В–µ–ї—Ц—В–Њ–Љ, —Й–Њ –Љ—Ц—Б—В–Є—В—М –і–≤–Њ–ї–∞–љ—Ж—О–≥–Њ–≤—Г –Ф–Э–Ъ —Ц —А–Њ–Ј–Љ–љ–Њ–ґ—Г—Ф—В—М—Б—П –≤ –µ—Г–Ї–∞—А—Ц–Њ—В–Є—З–љ–Є—Е –Ї–ї—Ц—В–Є–љ–∞—Е. –Ю–і–љ–∞–Ї –∞–≤—В–Њ—А–Є —А–Њ–±–Њ—В–Є –њ—А–Њ–њ–Њ–љ—Г—О—В—М —А–Њ–Ј–≥–ї—П–і–∞—В–Є –є–Њ–≥–Њ –љ–µ –њ—А–Њ—Б—В–Њ —П–Ї —Б–∞—В–µ–ї—Ц—В, –∞ —П–Ї –≤—Ц—А–Њ—Д–∞–≥ (–≤—Ц—А—Г—Б –≤—Ц—А—Г—Б—Г) –Ј–∞ –∞–љ–∞–ї–Њ–≥—Ц—Ф—О –Ј –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥–∞–Љ–Є (–≤—Ц—А—Г—Б–∞–Љ–Є –±–∞–Ї—В–µ—А—Ц–є)[ 240] [ 241] [ 242] [ 243] [ 244] [ 245] [ 246] [ 247]
–Т—Ц—А—Г—Б–Є —Ф –љ–∞–є–њ–Њ—И–Є—А–µ–љ—Ц—И–Њ—О –Ј–∞ —З–Є—Б–µ–ї—М–љ—Ц—Б—В—О —Д–Њ—А–Љ–Њ—О —Ц—Б–љ—Г–≤–∞–љ–љ—П –Њ—А–≥–∞–љ—Ц—З–љ–Њ—Ч –Љ–∞—В–µ—А—Ц—Ч –љ–∞ –њ–ї–∞–љ–µ—В—Ц. –Т–Њ–љ–Є –≤—Ц–і—Ц–≥—А–∞—О—В—М –≤–∞–ґ–ї–Є–≤—Г —А–Њ–ї—М —Г —А–µ–≥—Г–ї—П—Ж—Ц—Ч —З–Є—Б–µ–ї—М–љ–Њ—Б—В—Ц –њ–Њ–њ—Г–ї—П—Ж—Ц–є –і–µ—П–Ї–Є—Е –≤–Є–і—Ц–≤ –ґ–Є–≤–Є—Е –Њ—А–≥–∞–љ—Ц–Ј–Љ—Ц–≤ (–љ–∞–њ—А–Є–Ї–ї–∞–і, –≤—Ц—А—Г—Б –і–Є–Ї—Г–≤–∞–љ–љ—П –Ј –њ–µ—А—Ц–Њ–і–Њ–Љ —Г –і–µ–Ї—Ц–ї—М–Ї–∞ —А–Њ–Ї—Ц–≤ —Б–Ї–Њ—А–Њ—З—Г—Ф —З–Є—Б–µ–ї—М–љ—Ц—Б—В—М –њ–µ—Б—Ж—Ц–≤ —Г –Ї—Ц–ї—М–Ї–∞ —А–∞–Ј—Ц–≤).
–Ж–љ–Њ–і—Ц –≤—Ц—А—Г—Б–Є —Г—В–≤–Њ—А—О—О—В—М –Ј —В–≤–∞—А–Є–љ–∞–Љ–Є —Б–Є–Љ–±—Ц–Њ–Ј [ 248] [ 249] –њ–∞—А–∞–Ј–Є—В–Є—З–љ–Є—Е –Њ—Б –Љ—Ц—Б—В–Є—В—М —Б—В—А—Г–Ї—В—Г—А–Є, –Ј–≤–∞–љ—Ц –њ–Њ–ї—Ц-–Ф–Э–Ъ-–≤—Ц—А—Г—Б–∞–Љ–Є (Polydnavirus [en]
–Ю–і–љ–∞–Ї –Њ—Б–љ–Њ–≤–љ–∞ —А–Њ–ї—М –≤—Ц—А—Г—Б—Ц–≤ —Г –±—Ц–Њ—Б—Д–µ—А—Ц –њ–Њ–≤'—П–Ј–∞–љ–∞ –Ј —Ч—Е –і—Ц—П–ї—М–љ—Ц—Б—В—О —Г –≤–Њ–і–∞—Е –Њ–Ї–µ–∞–љ—Ц–≤ —Ц –Љ–Њ—А—Ц–≤.
–Т—Ц—А—Г—Б–Є вАФ —Ж–µ –љ–∞–є–њ–Њ—И–Є—А–µ–љ—Ц—И–∞ —Д–Њ—А–Љ–∞ –ґ–Є—В—В—П –≤ –Њ–Ї–µ–∞–љ—Ц, —Ч—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж—Ц—П —Б—П–≥–∞—Ф 10 –Љ–ї–љ –≤—Ц—А—Г—Б—Ц–≤ –љ–∞ 1 –Љ–Љ2 –њ–Њ–≤–µ—А—Е–љ—Ц –Љ–Њ—А—П[ 250] –µ–Ї–Њ—Б–Є—Б—В–µ–Љ . –Ч–љ–∞—З–љ–∞ —З–∞—Б—В–Є–љ–∞ —Ж–Є—Е –≤—Ц—А—Г—Б—Ц–≤ —Ф –±–∞–Ї—В–µ—А—Ц–Њ—Д–∞–≥–∞–Љ–Є , –љ–µ—И–Ї—Ц–і–ї–Є–≤–Є–Љ–Є –і–ї—П —А–Њ—Б–ї–Є–љ —Ц —В–≤–∞—А–Є–љ. –Т–Њ–љ–Є –≤—А–∞–ґ–∞—О—В—М —Ц —А—Г–є–љ—Г—О—В—М –±–∞–Ї—В–µ—А—Ц—Ч —Г –≤–Њ–і–љ–Њ–Љ—Г –Љ—Ц–Ї—А–Њ–±–љ–Њ–Љ—Г —Б–њ—Ц–≤—В–Њ–≤–∞—А–Є—Б—В–≤—Ц, —В–∞–Ї–Є–Љ —З–Є–љ–Њ–Љ, –±–µ—А—Г—З–Є —Г—З–∞—Б—В—М —Г –≤–∞–ґ–ї–Є–≤–Њ–Љ—Г –њ—А–Њ—Ж–µ—Б—Ц –Ї—А—Г–≥–Њ–Њ–±—Ц–≥—Г –≤—Г–≥–ї–µ—Ж—О –≤ –Љ–Њ—А—Б—М–Ї–Њ–Љ—Г —Б–µ—А–µ–і–Њ–≤–Є—Й—Ц. –Ю—А–≥–∞–љ—Ц—З–љ—Ц –Љ–Њ–ї–µ–Ї—Г–ї–Є, —П–Ї—Ц –Ј–≤—Ц–ї—М–љ–Є–ї–Є—Б—П –Ј –±–∞–Ї—В–µ—А—Ц–∞–ї—М–љ–Є—Е –Ї–ї—Ц—В–Є–љ –Ј–∞–≤–і—П–Ї–Є –≤—Ц—А—Г—Б–∞–Љ, —Б—В–Є–Љ—Г–ї—О—О—В—М —А—Ц—Б—В –љ–Њ–≤–Є—Е –±–∞–Ї—В–µ—А—Ц–є —Ц –≤–Њ–і–Њ—А–Њ—Б—В–µ–є .
–Ь—Ц–Ї—А–Њ–Њ—А–≥–∞–љ—Ц–Ј–Љ–Є —Б—В–∞–љ–Њ–≤–ї—П—В—М –њ–Њ–љ–∞–і 90 % –±—Ц–Њ–Љ–∞—Б–Є –≤ –Љ–Њ—А—Ц. –Ч–∞ –Њ—Ж—Ц–љ–Ї–∞–Љ–Є, –Ї–Њ–ґ–µ–љ –і–µ–љ—М –≤—Ц—А—Г—Б–Є –≤–±–Є–≤–∞—О—В—М –±–ї–Є–Ј—М–Ї–Њ 20 % —Ж—Ц—Ф—Ч –±—Ц–Њ–Љ–∞—Б–Є, –∞ –Ї—Ц–ї—М–Ї—Ц—Б—В—М –≤—Ц—А—Г—Б—Ц–≤ –≤ –Њ–Ї–µ–∞–љ–∞—Е —Г 15 —А–∞–Ј—Ц–≤ –њ–µ—А–µ–≤–Є—Й—Г—Ф –Ї—Ц–ї—М–Ї—Ц—Б—В—М –±–∞–Ї—В–µ—А—Ц–є —Ц –∞—А—Е–µ–є . –Т—Ц—А—Г—Б–Є —Ф –≥–Њ–ї–Њ–≤–љ–Є–Љ–Є –∞–≥–µ–љ—В–∞–Љ–Є, —Й–Њ —Б–њ—А–Є—З–Є–љ—П—О—В—М —И–≤–Є–і–Ї–µ –њ—А–Є–њ–Є–љ–µ–љ–љ—П —Ж–≤—Ц—В—Ц–љ–љ—П –≤–Њ–і–Є [ 254] [ 255] [ 256]
–Ч–љ–∞—З–µ–љ–љ—П –Љ–Њ—А—Б—М–Ї–Є—Е –≤—Ц—А—Г—Б—Ц–≤ –і—Г–ґ–µ –≤–µ–ї–Є–Ї–µ. –†–µ–≥—Г–ї—О—О—З–Є –њ—А–Њ—Ж–µ—Б —Д–Њ—В–Њ—Б–Є–љ—В–µ–Ј—Г , –≤–Њ–љ–Є –≤—Ц–і—Ц–≥—А–∞—О—В—М –і—А—Г–≥–Њ—А—П–і–љ—Г —А–Њ–ї—М —Г —Б–Ї–Њ—А–Њ—З–µ–љ–љ—Ц –Ї—Ц–ї—М–Ї–Њ—Б—В—Ц –≤—Г–≥–ї–µ–Ї–Є—Б–ї–Њ–≥–Њ –≥–∞–Ј—Г –≤ –∞—В–Љ–Њ—Б—Д–µ—А—Ц –њ—А–Є–±–ї–Є–Ј–љ–Њ –љ–∞ 3 –≥—Ц–≥–∞—В–Њ–љ–љ–Є –≤—Г–≥–ї–µ—Ж—О –Ј–∞ —А—Ц–Ї[ 256]
–ѓ–Ї —Ц —Ц–љ—И—Ц –Њ—А–≥–∞–љ—Ц–Ј–Љ–Є, –Љ–Њ—А—Б—М–Ї—Ц —Б—Б–∞–≤—Ж—Ц —Б–њ—А–Є–є–љ—П—В–ї–Є–≤—Ц –і–Њ –≤—Ц—А—Г—Б–љ–Є—Е —Ц–љ—Д–µ–Ї—Ж—Ц–є . –£ 1988 —Ц 2002 —А–Њ–Ї–∞—Е —В–Є—Б—П—З—Ц –Ј–≤–Є—З–∞–є–љ–Є—Е —В—О–ї–µ–љ—Ц–≤ –±—Г–ї–Є –≤–±–Є—В—Ц –њ–∞—А–∞–Љ—Ц–Ї—Б–Њ–≤—Ц—А—Г—Б–Њ–Љ Phocine distemper virus [ 257] –њ–Њ–њ—Г–ї—П—Ж—Ц—П—Е –Љ–Њ—А—Б—М–Ї–Є—Е —Б—Б–∞–≤—Ж—Ц–≤ —Ж–Є—А–Ї—Г–ї—О—Ф –±–µ–Ј–ї—Ц—З —Ц–љ—И–Є—Е –≤—Ц—А—Г—Б—Ц–≤, —Г —В–Њ–Љ—Г —З–Є—Б–ї—Ц –Ї–∞–ї—Ц—Ж–Є–≤—Ц—А—Г—Б–Є [en] –≥–µ—А–њ–µ—Б–≤—Ц—А—Г—Б–Є , –∞–і–µ–љ–Њ–≤—Ц—А—Г—Б–Є —В–∞ –њ–∞—А–≤–Њ–≤—Ц—А—Г—Б–Є [ 258]
–Т—Ц—А—Г—Б–Є —Ф –≤–∞–ґ–ї–Є–≤–Є–Љ –њ—А–Є—А–Њ–і–љ–Є–Љ –Ј–∞—Б–Њ–±–Њ–Љ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—П –≥–µ–љ—Ц–≤ –Љ—Ц–ґ —А—Ц–Ј–љ–Є–Љ–Є –≤–Є–і–∞–Љ–Є , —Й–Њ –њ–Њ—А–Њ–і–ґ—Г—Ф –≥–µ–љ–µ—В–Є—З–љ–µ —А—Ц–Ј–љ–Њ–Љ–∞–љ—Ц—В—В—П —Ц –љ–∞–њ—А–∞–≤–ї—П—Ф –µ–≤–Њ–ї—О—Ж—Ц—О [ 259] –±–∞–Ї—В–µ—А—Ц–є , –∞—А—Е–µ–є —Ц –µ—Г–Ї–∞—А—Ц–Њ—В—Ц–≤ , —Г —З–∞—Б–Є –Њ—Б—В–∞–љ–љ—М–Њ–≥–Њ —Г–љ—Ц–≤–µ—А—Б–∞–ї—М–љ–Њ–≥–Њ –Ј–∞–≥–∞–ї—М–љ–Њ–≥–Њ –њ—А–µ–і–Ї–∞ –ґ–Є—В—В—П –љ–∞ –Ч–µ–Љ–ї—Ц[ 260] [ 256]
–Э–∞—Г–Ї–Њ–≤–µ—Ж—М, —Й–Њ –≤–Є–≤—З–∞—Ф –≤—Ц—А—Г—Б –≥—А–Є–њ—Г H5N1 –Т—Ц—А—Г—Б–Є –Љ–∞—О—В—М –≤–∞–ґ–ї–Є–≤–µ –Ј–љ–∞—З–µ–љ–љ—П –і–ї—П –і–Њ—Б–ї—Ц–і–ґ–µ–љ—М –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ—Ч —Ц –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч –±—Ц–Њ–ї–Њ–≥—Ц—Ч , –±–Њ –≤–Њ–љ–Є —Ф –њ—А–Њ—Б—В–Є–Љ–Є —Б–Є—Б—В–µ–Љ–∞–Љ–Є, —П–Ї—Ц –Љ–Њ–ґ–љ–∞ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞—В–Є –і–ї—П —Г–њ—А–∞–≤–ї—Ц–љ–љ—П —Ц –≤–Є–≤—З–µ–љ–љ—П —Д—Г–љ–Ї—Ж—Ц–Њ–љ—Г–≤–∞–љ–љ—П –Ї–ї—Ц—В–Є–љ . –Т–Є–≤—З–µ–љ–љ—П —Ц –≤–Є–Ї–Њ—А–Є—Б—В–∞–љ–љ—П –≤—Ц—А—Г—Б—Ц–≤ –і–∞–ї–Њ —Ж—Ц–љ–љ—Г —Ц–љ—Д–Њ—А–Љ–∞—Ж—Ц—О –њ—А–Њ —А—Ц–Ј–љ—Ц –∞—Б–њ–µ–Ї—В–Є –Ї–ї—Ц—В–Є–љ–љ–Њ—Ч –±—Ц–Њ–ї–Њ–≥—Ц—Ч[ 262] –≥–µ–љ–µ—В–Є—З–љ–Є—Е –і–Њ—Б–ї—Ц–і–ґ–µ–љ–љ—П—Е, —Ц –≤–Њ–љ–Є –і–Њ–њ–Њ–Љ–Њ–≥–ї–Є –і—Ц–є—В–Є —А–Њ–Ј—Г–Љ—Ц–љ–љ—П –Ї–ї—О—З–Њ–≤–Є—Е –Љ–µ—Е–∞–љ—Ц–Ј–Љ—Ц–≤ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ—Ч –≥–µ–љ–µ—В–Є–Ї–Є , —В–∞–Ї–Є—Е —П–Ї —А–µ–њ–ї—Ц–Ї–∞—Ж—Ц—П –Ф–Э–Ъ , —В—А–∞–љ—Б–Ї—А–Є–њ—Ж—Ц—П , –њ—А–Њ—Ж–µ—Б–Є–љ–≥ –†–Э–Ъ , —В—А–∞–љ—Б–ї—П—Ж—Ц—П , —В—А–∞–љ—Б–њ–Њ—А—В –±—Ц–ї–Ї—Ц–≤ .
–У–µ–љ–µ—В–Є–Ї–Є —З–∞—Б—В–Њ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М –≤—Ц—А—Г—Б–Є —П–Ї –≤–µ–Ї—В–Њ—А–Є –і–ї—П –≤–≤–µ–і–µ–љ–љ—П –≥–µ–љ—Ц–≤ —Г –і–Њ—Б–ї—Ц–і–ґ—Г–≤–∞–љ—Ц –Ї–ї—Ц—В–Є–љ–Є. –¶–µ –і–Њ–Ј–≤–Њ–ї—П—Ф –Ј–Љ—Г—Б–Є—В–Є –Ї–ї—Ц—В–Є–љ—Г –≤–Є—А–Њ–±–ї—П—В–Є —З—Г–ґ—Ц —А–µ—З–Њ–≤–Є–љ–Є, –∞ —В–∞–Ї–Њ–ґ –≤–Є–≤—З–Є—В–Є –µ—Д–µ–Ї—В –≤—Ц–і –≤–≤–µ–і–µ–љ–љ—П –љ–Њ–≤–Њ–≥–Њ –≥–µ–љ–∞ –≤ –≥–µ–љ–Њ–Љ . –Р–љ–∞–ї–Њ–≥—Ц—З–љ–Њ —Г –≤—Ц—А–Њ—В–µ—А–∞–њ—Ц—Ч –≤—Ц—А—Г—Б–Є –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М —П–Ї –≤–µ–Ї—В–Њ—А–Є –і–ї—П –ї—Ц–Ї—Г–≤–∞–љ–љ—П —А—Ц–Ј–љ–Є—Е —Е–≤–Њ—А–Њ–±, —В–Њ–Љ—Г —Й–Њ –≤–Њ–љ–Є –≤–Є–±—Ц—А–Ї–Њ–≤–Њ –і—Ц—О—В—М –љ–∞ –Ї–ї—Ц—В–Є–љ–Є —Ц –Ф–Э–Ъ . –¶–µ –і–∞—Ф –љ–∞–і—Ц—Ч, —Й–Њ –≤—Ц—А—Г—Б–Є –Ј–Љ–Њ–ґ—Г—В—М –і–Њ–њ–Њ–Љ–Њ–≥—В–Є –≤ –±–Њ—А–Њ—В—М–±—Ц –Ј —А–∞–Ї–Њ–Љ —Ц –Ј–љ–∞–є–і—Г—В—М —Б–≤–Њ—Ф –Ј–∞—Б—В–Њ—Б—Г–≤–∞–љ–љ—П —Г –≥–µ–љ–Њ—В–µ—А–∞–њ—Ц—Ч . –Ф–µ—П–Ї–Є–є —З–∞—Б —Б—Е—Ц–і–љ–Њ—Ф–≤—А–Њ–њ–µ–є—Б—М–Ї—Ц –≤—З–µ–љ—Ц –Ј–∞—Б—В–Њ—Б–Њ–≤—Г–≤–∞–ї–Є —Д–∞–≥–Њ–≤–Њ—Ч —В–µ—А–∞–њ—Ц—Ч [en] –∞–љ—В–Є–±—Ц–Њ—В–Є–Ї—Ц–≤ , —Ц —Ц–љ—В–µ—А–µ—Б –і–Њ —В–∞–Ї–Є—Е –Љ–µ—В–Њ–і—Ц–≤ –Ј—А–Њ—Б—В–∞—Ф, –Њ—Б–Ї—Ц–ї—М–Ї–Є –љ–Є–љ—Ц —Г –і–µ—П–Ї–Є—Е –њ–∞—В–Њ–≥–µ–љ–љ–Є—Е –±–∞–Ї—В–µ—А—Ц–є –≤–Є—П–≤–ї–µ–љ–Њ –≤–Є—Б–Њ–Ї—Г —Б—В—Ц–є–Ї—Ц—Б—В—М –і–Њ –∞–љ—В–Є–±—Ц–Њ—В–Є–Ї—Ц–≤[ 263]
–С—Ц–Њ—Б–Є–љ—В–µ–Ј –Ј–∞—А–∞–ґ–µ–љ–Є–Љ–Є –Ї–ї—Ц—В–Є–љ–∞–Љ–Є —З—Г–ґ–Њ—А—Ц–і–љ–Є—Е –±—Ц–ї–Ї—Ц–≤ –ї–µ–ґ–Є—В—М –≤ –Њ—Б–љ–Њ–≤—Ц –і–µ—П–Ї–Є—Е —Б—Г—З–∞—Б–љ–Є—Е –њ—А–Њ–Љ–Є—Б–ї–Њ–≤–Є—Е —Б–њ–Њ—Б–Њ–±—Ц–≤ –Њ—В—А–Є–Љ–∞–љ–љ—П –±—Ц–ї–Ї—Ц–≤, –љ–∞–њ—А–Є–Ї–ї–∞–і, –∞–љ—В–Є–≥–µ–љ—Ц–≤ . –Э–µ—Й–Њ–і–∞–≤–љ–Њ –њ—А–Њ–Љ–Є—Б–ї–Њ–≤–Є–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –Њ—В—А–Є–Љ–∞–љ–Њ –і–µ—П–Ї—Ц –≤—Ц—А—Г—Б–љ—Ц –≤–µ–Ї—В–Њ—А–Є —Ц –ї—Ц–Ї–∞—А—Б—М–Ї—Ц –±—Ц–ї–Ї–Є, –љ–Є–љ—Ц –≤–Њ–љ–Є –њ—А–Њ—Е–Њ–і—П—В—М –Ї–ї—Ц–љ—Ц—З–љ—Ц —В–∞ –і–Њ–Ї–ї—Ц–љ—Ц—З–љ—Ц –≤–Є–њ—А–Њ–±—Г–≤–∞–љ–љ—П[ 264]
–°—Г—З–∞—Б–љ—Ц –љ–∞–њ—А—П–Љ–Ї–Є –≤ –љ–∞–љ–Њ—В–µ—Е–љ–Њ–ї–Њ–≥—Ц—Ч –Њ–±—Ц—Ж—П—О—В—М –Ј–љ–∞—З–љ–Њ —Г—А—Ц–Ј–љ–Њ–Љ–∞–љ—Ц—В–љ–Є—В–Є –Ј–∞—Б—В–Њ—Б—Г–≤–∞–љ–љ—П –≤—Ц—А—Г—Б—Ц–≤. –Ч –њ–Њ–≥–ї—П–і—Г –Љ–∞—В–µ—А—Ц–∞–ї–Њ–Ј–љ–∞–≤—Ж—Ц–≤, –≤—Ц—А—Г—Б–Є –Љ–Њ–ґ–љ–∞ —А–Њ–Ј–≥–ї—П–і–∞—В–Є —П–Ї –Њ—А–≥–∞–љ—Ц—З–љ—Ц –љ–∞–љ–Њ—З–∞—Б—В–Є–љ–Ї–Є . –З—Е–љ—П –њ–Њ–≤–µ—А—Е–љ—П –љ–µ—Б–µ —Б–њ–µ—Ж—Ц–∞–ї—М–љ—Ц –њ—А–Є—Б—В–Њ—Б—Г–≤–∞–љ–љ—П –і–ї—П –њ–Њ–і–Њ–ї–∞–љ–љ—П –±—Ц–Њ–ї–Њ–≥—Ц—З–љ–Є—Е –±–∞—А'—Ф—А—Ц–≤ –Ї–ї—Ц—В–Є–љ–Є -—Е–∞–Ј—П—Ч–љ–∞. –Ґ–Њ—З–љ–Њ –≤–Є–Ј–љ–∞—З–µ–љ–Њ —Д–Њ—А–Љ—Г —Ц —А–Њ–Ј–Љ—Ц—А –≤—Ц—А—Г—Б—Ц–≤, –∞ —В–∞–Ї–Њ–ґ –Ї—Ц–ї—М–Ї—Ц—Б—В—М —Ц –њ—А–Є—А–Њ–і—Г —Д—Г–љ–Ї—Ж—Ц–Њ–љ–∞–ї—М–љ–Є—Е –≥—А—Г–њ –љ–∞ –њ–Њ–≤–µ—А—Е–љ—Ц. –Я–Њ —Б—Г—В—Ц, –≤—Ц—А—Г—Б–Є —З–∞—Б—В–Њ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М –≤ –Љ–∞—В–µ—А—Ц–∞–ї–Њ–Ј–љ–∞–≤—Б—В–≤—Ц —П–Ї ¬Ђ—А–Є—И—В—Г–≤–∞–љ–љ—П¬ї –і–ї—П –Ї–Њ–≤–∞–ї–µ–љ—В–љ–Њ –њ–Њ–≤'—П–Ј–∞–љ–Є—Е –њ–Њ–≤–µ—А—Е–љ–µ–≤–Є—Е –Љ–Њ–і–Є—Д—Ц–Ї–∞—Ж—Ц–є. –Ю–і–љ–∞ –Ј –≤—Ц–і–Љ—Ц–љ–љ–Є—Е —П–Ї–Њ—Б—В–µ–є –≤—Ц—А—Г—Б—Ц–≤ вАФ —В–µ, —Й–Њ –≤–Њ–љ–Є —Б–њ–µ—Ж—Ц–∞–ї—М–љ–Њ ¬Ђ–њ—Ц–і—Ц–≥–љ–∞–љ—Ц¬ї —Б–њ—А—П–Љ–Њ–≤–∞–љ–Њ—О –µ–≤–Њ–ї—О—Ж—Ц—Ф—О –њ—Ц–і –Ї–ї—Ц—В–Є–љ–Є, —Й–Њ —Ф —Е–∞–Ј—П—П–Љ–Є. –Я–Њ—В—Г–ґ–љ—Ц –Љ–µ—В–Њ–і–Є, —А–Њ–Ј—А–Њ–±–ї–µ–љ—Ц –±—Ц–Њ–ї–Њ–≥–∞–Љ–Є, –ї—П–≥–ї–Є –≤ –Њ—Б–љ–Њ–≤—Г —Ц–љ–ґ–µ–љ–µ—А–љ–Є—Е –њ—А–Є–є–Њ–Љ—Ц–≤ —Г –љ–∞–љ–Њ–Љ–∞—В–µ—А—Ц–∞–ї–∞—Е , –≤—Ц–і–Ї—А–Є–≤—И–Є —В–Є–Љ —Б–∞–Љ–Є–Љ —И–Є—А–Њ–Ї—Г —Б—Д–µ—А—Г –Ј–∞—Б—В–Њ—Б—Г–≤–∞–љ–љ—П –≤—Ц—А—Г—Б—Ц–≤, —Й–Њ –≤–Є—Е–Њ–і–Є—В—М –і–∞–ї–µ–Ї–Њ –Ј–∞ –Љ–µ–ґ—Ц –±—Ц–Њ–ї–Њ–≥—Ц—Ч —В–∞ –Љ–µ–і–Є—Ж–Є–љ–Є[ 265]
–Ч–∞–≤–і—П–Ї–Є —Ч—Е–љ—Ц–Љ —А–Њ–Ј–Љ—Ц—А–∞–Љ, —Д–Њ—А–Љ—Ц –є –і–Њ–±—А–µ –≤–Є–≤—З–µ–љ—Ц–є —Е—Ц–Љ—Ц—З–љ—Ц–є —Б—В—А—Г–Ї—В—Г—А—Ц –≤—Ц—А—Г—Б–Є –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞–ї–Є —П–Ї —И–∞–±–ї–Њ–љ–Є –і–ї—П –Њ—А–≥–∞–љ—Ц–Ј–∞—Ж—Ц—Ч –Љ–∞—В–µ—А—Ц–∞–ї—Ц–≤ –љ–∞ –љ–∞–љ–Њ—А—Ц–≤–љ—Ц. –Я—А–Є–Ї–ї–∞–і–Њ–Љ —В–∞–Ї–Њ—Ч –љ–µ—Й–Њ–і–∞–≤–љ—М–Њ—Ч —А–Њ–±–Њ—В–Є –Љ–Њ–ґ—Г—В—М –±—Г—В–Є –і–Њ—Б–ї—Ц–і–ґ–µ–љ–љ—П, –њ—А–Њ–≤–µ–і–µ–љ—Ц –Ф–Њ—Б–ї—Ц–і–љ–Є—Ж—М–Ї–Њ—О –ї–∞–±–Њ—А–∞—В–Њ—А—Ц—Ф—О –Э–∞–≤–∞–ї—О —Г –Т–∞—И–Є–љ–≥—В–Њ–љ—Ц (–Њ–Ї—А—Г–≥ –Ъ–Њ–ї—Г–Љ–±—Ц—П) –Ј –≤–Є–Ї–Њ—А–Є—Б—В–∞–љ–љ—П–Љ –≤—Ц—А—Г—Б—Г –Љ–Њ–Ј–∞—Ч–Ї–Є –Ї–Њ—А–Њ–≤'—П—З–Њ–≥–Њ –≥–Њ—А–Њ—Е—Г [en] –∞–љ–≥–ї. Cowpea Mosaic Virus (CPMV) ) –і–ї—П –њ–Њ—Б–Є–ї–µ–љ–љ—П —Б–Є–≥–љ–∞–ї—Ц–≤ —Г —Б–µ–љ—Б–Њ—А–∞—Е –Ј –Ф–Э–Ъ-–Љ—Ц–Ї—А–Њ—З–Є–њ–∞–Љ–Є . –Т —Ж—М–Њ–Љ—Г –≤–Є–њ–∞–і–Ї—Г –≤—Ц—А—Г—Б–љ—Ц —З–∞—Б—В–Є–љ–Ї–Є –њ–Њ–і—Ц–ї—П–ї–Є —З–∞—Б—В–Є–љ–Ї–Є —Д–ї—Г–Њ—А–µ—Б—Ж–µ–љ—В–љ–Є—Е –±–∞—А–≤–љ–Є–Ї—Ц–≤, —П–Ї—Ц –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г–≤–∞–ї–Є—Б—П –і–ї—П –њ–µ—А–µ–і–∞—З—Ц —Б–Є–≥–љ–∞–ї—Г, –Ј–∞–њ–Њ–±—Ц–≥–∞—О—З–Є, —В–∞–Ї–Є–Љ —З–Є–љ–Њ–Љ, —Б–Ї—Г–њ—З–µ–љ–љ—О –љ–µ—Д–ї—Г–Њ—А–µ—Б—Ж–µ–љ—В–љ–Є—Е –і–Є–Љ–µ—А—Ц–≤ , —П–Ї—Ц –≤–Є—Б—В—Г–њ–∞—О—В—М —П–Ї –≥–∞—Б–Є—В–µ–ї—Ц —Б–Є–≥–љ–∞–ї—Г[ 266] CPMV —Ф –Ј–∞—Б—В–Њ—Б—Г–≤–∞–љ–љ—П –є–Њ–≥–Њ —П–Ї –љ–∞–љ–Њ—А–Њ–Ј–Љ—Ц—А–љ–Њ–≥–Њ –Ј—А–∞–Ј–Ї–∞ –і–ї—П –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ—Ч –µ–ї–µ–Ї—В—А–Њ–љ—Ц–Ї–Є[ 267]
–С–∞–≥–∞—В–Њ –≤—Ц—А—Г—Б—Ц–≤ –Љ–Њ–ґ–љ–∞ –Њ—В—А–Є–Љ–∞—В–Є de novo , —В–Њ–±—В–Њ –Ј –љ—Г–ї—П, –∞ –њ–µ—А—И–Є–є —И—В—Г—З–љ–Є–є –≤—Ц—А—Г—Б –Њ—В—А–Є–Љ–∞–ї–Є 2002 —А–Њ–Ї—Г[ 31] –Ф–Э–Ъ-–≤–Љ—Ц—Б–љ–Є—Е –≤—Ц—А—Г—Б—Ц–≤ ) –∞–±–Њ –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞—А–љ–∞ –Ї–Њ–њ—Ц—П –Ф–Э–Ъ –≥–µ–љ–Њ–Љ—Г (—Г —А–∞–Ј—Ц –†–Э–Ъ-–≤—Ц—А—Г—Б—Ц–≤ ). –£ –≤—Ц—А—Г—Б—Ц–≤ –±–∞–≥–∞—В—М–Њ—Е —А–Њ–і–Є–љ —И—В—Г—З–љ–∞ –Ф–Э–Ъ –∞–±–Њ –†–Э–Ъ (–Њ—Б—В–∞–љ–љ—П –≤–Є—Е–Њ–і–Є—В—М —И–ї—П—Е–Њ–Љ –Ј–≤–Њ—А–Њ—В–љ–Њ—Ч —В—А–∞–љ—Б–Ї—А–Є–њ—Ж—Ц—Ч —Б–Є–љ—В–µ—В–Є—З–љ–Њ—Ч –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ—Ч –Ф–Э–Ъ), —П–Ї—Й–Њ —Ч—Ч –≤–≤–µ—Б—В–Є –≤ –Ї–ї—Ц—В–Є–љ—Г , –њ—А–Њ—П–≤–ї—П—Ф —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ—Ц –≤–ї–∞—Б—В–Є–≤–Њ—Б—В—Ц. –Ж–љ—И–Є–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, –≤–Њ–љ–Є –Љ—Ц—Б—В—П—В—М –≤—Б—О –љ–µ–Њ–±—Е—Ц–і–љ—Г —Ц–љ—Д–Њ—А–Љ–∞—Ж—Ц—О –і–ї—П —Г—В–≤–Њ—А–µ–љ–љ—П –љ–Њ–≤–Є—Е –≤—Ц—А—Г—Б—Ц–≤. –¶—О —В–µ—Е–љ–Њ–ї–Њ–≥—Ц—О –љ–Є–љ—Ц –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—В—М –і–ї—П —А–Њ–Ј—А–Њ–±–Ї–Є –≤–∞–Ї—Ж–Є–љ –љ–Њ–≤–Њ–≥–Њ —В–Є–њ—Г[ 268] –≤—Ц—Б–њ–Є [es] –Э–∞—Ж—Ц–Њ–љ–∞–ї—М–љ–Є–Љ–Є —Ц–љ—Б—В–Є—В—Г—В–∞–Љ–Є –Њ—Е–Њ—А–Њ–љ–Є –Ј–і–Њ—А–Њ–≤'—П –°–®–Р [ 269]
–°–њ—А–Њ–Љ–Њ–ґ–љ—Ц—Б—В—М –≤—Ц—А—Г—Б—Ц–≤ —Б–њ—А–Є—З–Є–љ—П—В–Є —Б–њ—Г—Б—В–Њ—И–ї–Є–≤—Ц –µ–њ—Ц–і–µ–Љ—Ц—Ч —Б–µ—А–µ–і –ї—О–і–µ–є –њ–Њ—А–Њ–і–ґ—Г—Ф —В—А–Є–≤–Њ–≥—Г, —Й–Њ –≤—Ц—А—Г—Б–Є –Љ–Њ–ґ–љ–∞ –Ј–∞—Б—В–Њ—Б—Г–≤–∞—В–Є —П–Ї –±—Ц–Њ–ї–Њ–≥—Ц—З–љ—Г –Ј–±—А–Њ—О . –Ф–Њ–і–∞—В–Ї–Њ–≤—Ц –њ–Њ–±–Њ—О–≤–∞–љ–љ—П –≤–Є–Ї–ї–Є–Ї–∞–ї–Њ —Г—Б–њ—Ц—И–љ–µ –≤—Ц–і—В–≤–Њ—А–µ–љ–љ—П –≤—Ц—А—Г—Б—Г —Ц—Б–њ–∞–љ—Б—М–Ї–Њ–≥–Њ –≥—А–Є–њ—Г –≤ –ї–∞–±–Њ—А–∞—В–Њ—А—Ц—Ч. –Ж–љ—И–Є–Љ –њ—А–Є–Ї–ї–∞–і–Њ–Љ –Љ–Њ–ґ–µ –±—Г—В–Є –≤—Ц—А—Г—Б –≤—Ц—Б–њ–Є. –£–њ—А–Њ–і–Њ–≤–ґ —Г—Б—Ц—Ф—Ч —Ц—Б—В–Њ—А—Ц—Ч –≤—Ц–љ —Б–њ—Г—Б—В–Њ—И—Г–≤–∞–≤ –±–µ–Ј–ї—Ц—З –Ї—А–∞—Ч–љ –∞–ґ –і–Њ –є–Њ–≥–Њ –Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ –≤–Є–Ї–Њ—А—Ц–љ–µ–љ–љ—П. –Ю—Д—Ц—Ж—Ц–є–љ–Њ –Ј—А–∞–Ј–Ї–Є –≤—Ц—А—Г—Б—Г –≤—Ц—Б–њ–Є –Ј–±–µ—А—Ц–≥–∞—О—В—М—Б—П –ї–Є—И–µ –≤ –і–≤–Њ—Е –Љ—Ц—Б—Ж—П—Е —Г —Б–≤—Ц—В—Ц вАФ —Г –і–≤–Њ—Е –ї–∞–±–Њ—А–∞—В–Њ—А—Ц—П—Е –≤ –†–Њ—Б—Ц—Ч —Ц –°–®–Р [ 271] –≤–∞–Ї—Ж–Є–љ–∞ –њ—А–Њ—В–Є –≤—Ц—Б–њ–Є —Ц–љ–Њ–і—Ц –Љ–∞—Ф –≤–∞–ґ–Ї—Ц –њ–Њ–±—Ц—З–љ—Ц –µ—Д–µ–Ї—В–Є вАФ –≤ –Њ—Б—В–∞–љ–љ—Ц —А–Њ–Ї–Є –і–Њ –Њ—Д—Ц—Ж—Ц–є–љ–Њ –Њ–≥–Њ–ї–Њ—И–µ–љ–Њ–≥–Њ –≤–Є–Ї–Њ—А—Ц–љ–µ–љ–љ—П –≤—Ц—А—Г—Б—Г –±—Ц–ї—М—И–µ –ї—О–і–µ–є —Б–µ—А–є–Њ–Ј–љ–Њ –Ј–∞—Е–≤–Њ—А—Ц–ї–Є —З–µ—А–µ–Ј –≤–∞–Ї—Ж–Є–љ–Є, –љ—Ц–ґ –≤—Ц–і –≤—Ц—А—Г—Б—Г[ 272] –≤–∞–Ї—Ж–Є–љ–∞—Ж—Ц—О –њ—А–Њ—В–Є –≤—Ц—Б–њ–Є –±—Ц–ї—М—И–µ –љ–µ –њ—А–∞–Ї—В–Є–Ї—Г—О—В—М –њ–Њ–≤—Б—О–і–љ–Њ[ 273] –Ч–µ–Љ–ї—Ц –њ—А–∞–Ї—В–Є—З–љ–Њ –љ–µ –Љ–∞—Ф —Б—В—Ц–є–Ї–Њ—Б—В—Ц –і–Њ –≤—Ц—Б–њ–Є .
–£ —Д—Ц–ї—М–Љ–∞—Е —В–∞ —Ц–љ—И–Є—Е —В–≤–Њ—А–∞—Е —Б–≤—Ц—В —Ц–љ—Д–µ–Ї—Ж—Ц–є–љ–Є—Е –Ј–∞—Е–≤–Њ—А—О–≤–∞–љ—М, –Ј–Њ–Ї—А–µ–Љ–∞ –≤—Ц—А—Г—Б–љ–Є—Е, —А—Ц–і–Ї–Њ –њ–Њ–Ї–∞–Ј—Г—О—В—М –і–Њ—Б—В–Њ–≤—Ц—А–љ–Њ. –Ъ—А—Ц–Љ —Д—Ц–ї—М–Љ—Ц–≤-–±—Ц–Њ–≥—А–∞—Д—Ц–є –≤—З–µ–љ–Є—Е —Ц —Д—Ц–ї—М–Љ—Ц–≤, —Й–Њ —А–Њ–Ј–њ–Њ–≤—Ц–і–∞—О—В—М –њ—А–Њ –≤–µ–ї–Є–Ї—Ц –µ–њ—Ц–і–µ–Љ—Ц—Ч –Љ–Є–љ—Г–ї–Њ–≥–Њ, —Г –±—Ц–ї—М—И–Њ—Б—В—Ц –Ј –љ–Є—Е —Ж–µ–љ—В—А–∞–ї—М–љ–Њ—О –њ–Њ–і—Ц—Ф—О —Ф —Б–њ–∞–ї–∞—Е –љ–µ–≤—Ц–і–Њ–Љ–Њ–≥–Њ —Е–≤–Њ—А–Њ–±–Њ—В–≤–Њ—А–љ–Њ–≥–Њ –∞–≥–µ–љ—В–∞, –њ–Њ—П–≤–∞ —П–Ї–Њ–≥–Њ —Б—В–∞–ї–∞ –љ–∞—Б–ї—Ц–і–Ї–Њ–Љ –∞–Ї—В—Г –±—Ц–Њ—В–µ—А–Њ—А–Є–Ј–Љ—Г , —Ц–љ—Ж–Є–і–µ–љ—В—Г –≤ –ї–∞–±–Њ—А–∞—В–Њ—А—Ц—Ч, –∞–±–Њ –ґ –≤—Ц–љ –њ–Њ—В—А–∞–њ–Є–≤ –Ј –Ї–Њ—Б–Љ–Њ—Б—Г[ 274]
–Т—Ц—А—Г—Б–љ–∞ —Ц–љ—Д–µ–Ї—Ж—Ц—П –Ј–∞–Ї–ї–∞–і–µ–љ–∞ –≤ –Њ—Б–љ–Њ–≤—Г —В–∞–Ї–Є—Е —В–≤–Њ—А—Ц–≤ (—Б–њ–Є—Б–Њ–Ї –љ–µ–њ–Њ–≤–љ–Є–є):
–°–њ–∞–ї–∞—Е –љ–µ–Ј–≤–Є—З–∞–є–љ–Њ—Ч –≤—Ц—А—Г—Б–љ–Њ—Ч —Ц–љ—Д–µ–Ї—Ж—Ц—Ч –ї–µ–ґ–Є—В—М –≤ –Њ—Б–љ–Њ–≤—Ц —Б—О–ґ–µ—В—Г —В–∞–Ї–Є—Е —Е—Г–і–Њ–ґ–љ—Ц—Е —Д—Ц–ї—М–Љ—Ц–≤ —Ц —Б–µ—А—Ц–∞–ї—Ц–≤[ 274]
–Ю—Б—В–∞–љ–љ—Ц–Љ–Є —А–Њ–Ї–∞–Љ–Є[–Ї–Њ–ї–Є? ¬Ђ–Ю—Б–Љ–Њ—Б–Є—Б –Ф–ґ–Њ–љ—Б¬ї (–°–®–Р , 2001), ¬Ђ–Ю–Ј–Ј—Ц —Ц –Ф—А–Є–Ї—Б¬ї (–°–®–Р , 2002вАФ2004) —Ц ¬Ђ–Т—Ц—А—Г—Б –∞—В–∞–Ї—Г—Ф¬ї (–Ж—В–∞–ї—Ц—П , 2011).
вЖС –∞ –± Koonin E. V., Senkevich T. G., Dolja V. V. // Biol. Direct. вАФ 2006. вАФ –°. 29 .вЖС –∞ –± How many viruses on Earth? . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 21 –±–µ—А–µ–Ј–љ—П 2020. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 21 –±–µ—А–µ–Ј–љ—П 2020 .вЖС –∞ –± Lawrence C. M., Menon S., Eilers B. J., et al. // J. Biol. Chem. : journal. вАФ 2009. вАФ Vol. 284 , no. 19 . вАФ P. 12599вАФ12603 . вАФ DOI :10.1074/jbc.R800078200 PMID 19158076 .вЖС Edwards R. A., Rohwer F. Viral metagenomics // Nat. Rev. Microbiol. вАФ 2005. вАФ –Ґ. 3 , вДЦ 6 . вАФ –°. 504вАФ510 . вАФ ISSN 1740-1526 . вАФ DOI :10.1038/nrmicro1163 PMID 15886693 .вЖС Harper D. (2011). virus . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 19 —Б—Ц—З–љ—П 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 23 –≥—А—Г–і–љ—П 2011 . вЖС Harper D. (2011). virion . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 19 —Б—Ц—З–љ—П 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 24 –≥—А—Г–і–љ—П 2011 . вЖС Casjens S. {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}} / Mahy B. W. J. and Van Regenmortel M. H. V. вАФ Boston : Academic Press , 2010. вАФ –°. 167. вАФ ISBN 0-12-375146-2 .вЖС Bordenave G. // Microbes and Infection / Institut Pasteur. вАФ 2003. вАФ вДЦ 6 . вАФ –°. 553вАФ560 .вЖС –У–∞–њ–Њ–љ –Ф. // –Э–∞—Г–Ї–∞ –Є –ґ–Є–Ј–љ—М . вАФ 2015. вАФ вДЦ 6 . вАФ –°. 38вАФ50 .вЖС –∞ –± Fenner F. {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}} / Mahy B. W. J. and Van Regenmortal M. H. V. вАФ 1. вАФ Oxford, UK : Academic Press , 2009. вАФ –°. 15. вАФ ISBN 0-12-375146-2 .вЖС D'Herelle F. // Research in Microbiology : journal. вАФ 2007. вАФ No. 7 . вАФ P. 553вАФ554 .вЖС Steinhardt E., Israeli C., Lambert R. A. // J. Inf Dis. : journal. вАФ 1913. вАФ No. 2 . вАФ P. 294вАФ300 .вЖС Goodpasture E. W., Woodruff A. M., Buddingh G. J. // Science : journal. вАФ 1931. вАФ No. 1919 . вАФ P. 371вАФ372 .вЖС Rosen, F. S. // New England Journal of Medicine : journal. вАФ 2004. вАФ No. 15 . вАФ P. 1481вАФ1483 .вЖС From Nobel Lectures, Physics 1981вАФ1990 , (1993) Editor-in-Charge Tore Fr√§ngsmyr, Editor G√ґsta Eksp√•ng, World Scientific Publishing Co., Singapore.
вЖС Stanley W. M., Loring H. S. // Science : journal. вАФ 1936. вАФ No. 2143 . вАФ P. 85 .вЖС Stanley W. M., Lauffer M. A. // Science : journal. вАФ 1939. вАФ No. 2311 . вАФ P. 345вАФ347 .вЖС Creager A. N., Morgan G. J. // Isis : journal. вАФ 2008. вАФ No. 2 . вАФ P. 239вАФ272 .вЖС Norrby E. // Arch. Virol.. вАФ 2008. вАФ вДЦ 6 . вАФ –°. 1109вАФ1123 .вЖС –∞ –± Temin H. M., Baltimore D. // Adv. Virus Res.. вАФ 1972. вАФ –Ґ. 17 . вАФ –°. 129вАФ186 . вАФ DOI :10.1016/S0065-3527(08)60749-6 PMID 4348509 . –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 2008-09-16.вЖС Barr√©-Sinoussi, F. et al. // Science : journal. вАФ 1983. вАФ No. 4599 . вАФ P. 868вАФ871 .вЖС –∞ –± Cello J., Paul A. V., Wimmer E. // Science : journal. вАФ 2002. вАФ No. 5583 . вАФ P. 1016вАФ1018 .вЖС New virus discovered in Pacific is deepest ever found in Earth's oceans. 21 September 2023 11:25, UK вЖС –£ –≤–Њ–і–∞—Е –Ґ–Є—Е–Њ–≥–Њ –Њ–Ї–µ–∞–љ—Г –Ј–љ–∞–є—И–ї–Є –љ–µ–≤—Ц–і–Њ–Љ–Є–є –љ–∞—Г—Ж—Ц –≤—Ц—А—Г—Б. // –Р–≤—В–Њ—А: –Ф–µ–љ–Є—Б –Ъ–Њ—А–Њ—В–Є–љ—Б—М–Ї–Є–є. 21.09.2023, 21:37 вЖС Iyer L. M., Balaji S., Koonin E. V., Aravind L. // Virus Res. : journal. вАФ 2006. вАФ Vol. 117 , no. 1 . вАФ P. 156вАФ184 . вАФ DOI :10.1016/j.virusres.2006.01.009 PMID 16494962 .вЖС Sanju√°n R., Nebot M. R., Chirico N., Mansky L. M., Belshaw R. // Journal of Virology. вАФ 2010. вАФ –Ґ. 84 , вДЦ 19 (10). вАФ –°. 9733вАФ9748 . вАФ DOI :10.1128/JVI.00694-10 PMID 20660197 .вЖС –∞ –± –≤ Mahy W. J. & Van Regenmortel M. H. V. (eds) . {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Oxford : Academic Press , 2009. вАФ –°. 24. вАФ ISBN 0-12-375146-2 .вЖС McClintock, B. // Proc Natl Acad Sci U S A.. вАФ 1950. вАФ вДЦ 6 . вАФ –°. 344вАФ355 .вЖС Tsagris E. M., de Alba A. E., Gozmanova M., Kalantidis K. // Cell. Microbiol.. вАФ 2008. вАФ вДЦ 11 . вАФ –°. 2168 .вЖС –∞ –± La Scola B., Desnues C., Pagnier I., Robert C., Barrassi L., Fournous G., Merchat M., Suzan-Monti M., Forterre P., Koonin E., Raoult D. // Nature : journal. вАФ 2008. вАФ No. 7209 . вАФ P. 100вАФ104 .вЖС Mahy W. J. & Van Regenmortel M. H. V. (eds) . {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Oxford : Academic Press , 2009. вАФ –°. 28. вАФ ISBN 0-12-375146-2 .вЖС Mahy W. J. & Van Regenmortel M. H. V. (eds) . {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Oxford : Academic Press , 2009. вАФ –°. 26. вАФ ISBN 0-12-375146-2 .вЖС Liberski P. P. // Folia Neuropathol : journal. вАФ 2008. вАФ No. 2 . вАФ P. 93вАФ116 .вЖС Belay E. D. and Schonberger L. B. {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Boston : Academic Press , 2009. вАФ –°. 497вАФ504. вАФ ISBN 0-12-375147-0 .вЖС Lupi O., Dadalti P., Cruz E., Goodheart C. // Med. Hypotheses : journal. вАФ 2007. вАФ No. 4 . вАФ P. 724вАФ730 .вЖС Holmes E. C. // PLoS Biol.. вАФ 2007. вАФ вДЦ 10 . вАФ –°. e278 .вЖС Wimmer E., Mueller S., Tumpey T. M., Taubenberger J. K. // Nature Biotechnology : journal. вАФ Nature Publishing Group , 2009. вАФ No. 12 . вАФ P. 1163вАФ1172 .вЖС Horn M. // Annual Review of Microbiology. вАФ 2008. вАФ –°. 113вАФ131 .вЖС Ammerman N. C., Beier-Sexton M., Azad A. F. // Current Protocols [en] –°. Unit 3A.5 .вЖС Seed K. D., Lazinski D. W., Calderwood S. B., Camilli A. // Nature : journal. вАФ 2013. вАФ No. 7438 . вАФ P. 489вАФ491 .вЖС Stefan Sirucek (3 –±–µ—А–µ–Ј–љ—П 2014). Ancient "Giant Virus" Revived From Siberian Permafrost . National Geographic . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 25 —З–µ—А–≤–љ—П 2018. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 3 –±–µ—А–µ–Ј–љ—П 2014 . вЖС Kiselev N. A., Sherman M. B., Tsuprun V. L. // Electron Microsc. Rev.. вАФ 1990. вАФ вДЦ 1 . вАФ –°. 43вАФ72 .вЖС Caspar D. L., Klug A. // Cold Spring Harb. Symp. Quant. Biol. : journal. вАФ 1962. вАФ P. 1вАФ24 .вЖС Crick F. H., Watson J. D. // Nature. вАФ 1956. вАФ No. 4506 . вАФ P. 473вАФ475 .вЖС Falvo, M.R.; S. Washburn, R. Superfine, M. Finch, F. P. Brooks Jr, V. Chi, R. M. Taylor 2nd. // Biophysical Journal : journal. вАФ 1997. вАФ No. 3 . вАФ P. 1396вАФ1403 .вЖС Kuznetsov, Yu. G.; A. J. Malkin, R. W. Lucas, M. Plomp, A. McPherson. // J Gen Virol. вАФ 2001. вАФ вДЦ 9 . вАФ –°. 2025вАФ2034 .[–љ–µ–і–Њ—Б—В—Г–њ–љ–µ –њ–Њ—Б–Є–ї–∞–љ–љ—П –Ј –Ы–Є–њ–µ–љ—М 2019 ] вЖС Casens, S. {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Boston : Academic Press , 2009. вАФ –°. 167вАФ174. вАФ ISBN 0-12-375146-2 .вЖС Rossmann M. G., Mesyanzhinov V. V., Arisaka F., Leiman P. G. // Curr. Opin. Struct. Biol.. вАФ 2004. вАФ No. 2 . вАФ P. 171вАФ180 .вЖС Long G. W., Nobel J., Murphy F. A., Herrmann K. L., Lourie B. // Appl Microbiol : journal. вАФ 1970. вАФ No. 3 . вАФ P. 497вАФ504 .вЖС Xiao C., Kuznetsov Y. G., Sun S., Hafenstein S. L., Kostyuchenko V. A., Chipman P. R., Suzan-Monti M., Raoult D., McPherson A., Rossmann M. G. // PLoS Biol. вАФ 2009. вАФ –Т–Є–њ. 4 . вАФ –°. e92 .вЖС Klose T., Kuznetsov Y. G., Xiao C., Sun S., McPherson A., Rossmann M. G. // Intervirology. вАФ 2010. вАФ –Т–Є–њ. 5 . вАФ –°. 268вАФ273 .вЖС WorldвАЩs biggest virus discovered in ocean depths near Chile . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 1 –ї—О—В–Њ–≥–Њ 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 12 –ґ–Њ–≤—В–љ—П 2011 .вЖС Saunders, Venetia A.; Carter, John . {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Chichester : John Wiley & Sons , 2007. вАФ –°. 72. вАФ ISBN 0-470-02387-2 .вЖС Van Etten J. L., Lane L. C., Dunigan D. D. // Annual Review of Microbiology. вАФ 2010. вАФ –°. 83вАФ99 .вЖС Sanju√°n R., Nebot M. R., Chirico N., Mansky L. M., Belshaw R. // Journal of Virology. вАФ 2010. вАФ вДЦ 19 (10). вАФ –°. 9733вАФ9748 .вЖС Pressing J., Reanney D. C. // J Mol Evol. вАФ 1984. вАФ вДЦ 2 . вАФ –°. 135вАФ146 .вЖС Duffy S., Holmes E. C. // Journal of General Virology [en] Microbiology Society [en] No. Pt 6 . вАФ P. 1539вАФ1547 .[–љ–µ–і–Њ—Б—В—Г–њ–љ–µ –њ–Њ—Б–Є–ї–∞–љ–љ—П –Ј –Ы–Є–њ–µ–љ—М 2019 ] вЖС Pan X. P., Li L. J., Du W. B., Li M. W., Cao H. C., Sheng J. F. // J. Viral Hepat. : journal. вАФ 2007. вАФ Vol. 14 , no. 11 . вАФ P. 767вАФ774 . вАФ DOI :10.1111/j.1365-2893.2007.00869.x PMID 17927612 .вЖС Hampson A. W., Mackenzie J. S. // Med. J. Aust.. вАФ 2006. вАФ –Ґ. 185 , вДЦ 10 Suppl . вАФ –°. S39вАФ43 . вАФ PMID 17115950 .вЖС Metzner K. J. // J HIV Ther : journal. вАФ 2006. вАФ Vol. 11 , no. 4 . вАФ P. 74вАФ81 . вАФ PMID 17578210 .вЖС Goudsmit, Jaap. Viral Sex. Oxford Univ Press, 1998. ISBN 978-0-19-512496-5 , ISBN 0-19-512496-0 .
вЖС Worobey M., Holmes E. C. // Journal of General Virology [en] Microbiology Society [en] Vol. 80 (Pt 10) . вАФ P. 2535вАФ2543 . вАФ PMID 10573145 .[–љ–µ–і–Њ—Б—В—Г–њ–љ–µ –њ–Њ—Б–Є–ї–∞–љ–љ—П –Ј –Ш—О–ї—М 2019 ] вЖС Lukashev A. N. // Rev. Med. Virol. : journal. вАФ 2005. вАФ Vol. 15 , no. 3 . вАФ P. 157вАФ167 . вАФ PMID 15578739 .вЖС Umene K. // Rev. Med. Virol. : journal. вАФ 1999. вАФ Vol. 9 , no. 3 . вАФ P. 171вАФ182 . вАФ PMID 10479778 .вЖС Boevink P., Oparka K. J. // Plant Physiol.. вАФ 2005. вАФ вДЦ 4 . вАФ –°. 1815вАФ1821 .вЖС Barman S., Ali A., Hui E. K., Adhikary L., Nayak D. P. // Virus Res. : journal. вАФ 2001. вАФ Vol. 77 , no. 1 . вАФ P. 61вАФ69 . вАФ DOI :10.1016/S0168-1702(01)00266-0 PMID 11451488 .вЖС Andronov, Leonid; Han, Mengting; Zhu, Yanyu; Balaji, Ashwin; Roy, Anish R.; Barentine, Andrew E. S.; Patel, Puja; Garhyan, Jaishree; Qi, Lei S. (31 —В—А–∞–≤–љ—П 2024). Nanoscale cellular organization of viral RNA and proteins in SARS-CoV-2 replication organelles . Nature Communications (–∞–љ–≥–ї.) . –Ґ. 15, вДЦ 1. —Б. 4644. doi :10.1038/s41467-024-48991-x . ISSN 2041-1723 . PMC 11143195 PMID 38821943 . –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 11 —З–µ—А–≤–љ—П 2024 . {{cite news }}: –Ю–±—Б–ї—Г–≥–Њ–≤—Г–≤–∞–љ–љ—П CS1: –°—В–Њ—А—Ц–љ–Ї–Є –Ј PMC –Ј —Ц–љ—И–Є–Љ —Д–Њ—А–Љ–∞—В–Њ–Љ (–њ–Њ—Б–Є–ї–∞–љ–љ—П )вЖС Staginnus C., Richert-P√ґggeler K. R. // Trends in Plant Science : journal. вАФ Cell Press , 2006. вАФ No. 10 . вАФ P. 485вАФ491 .вЖС Roulston A., Marcellus R. C., Branton P. E. // Annu. Rev. Microbiol.. вАФ 1999. вАФ –°. 577вАФ628 .вЖС Alwine J. C. // Curr. Top. Microbiol. Immunol. : journal. вАФ 2008. вАФ P. 263вАФ279 .вЖС Sinclair J. // J. Clin. Virol. : journal. вАФ 2008. вАФ Vol. 41 , no. 3 . вАФ P. 180вАФ185 . вАФ DOI :10.1016/j.jcv.2007.11.014 PMID 18164651 .вЖС Jordan M. C., Jordan G. W., Stevens J. G., Miller G. // Ann. Intern. Med.. вАФ 1984. вАФ –Ґ. 100 , вДЦ 6 . вАФ –°. 866вАФ880 . вАФ PMID 6326635 .вЖС Sissons J. G., Bain M., Wills M. R. // J. Infect.. вАФ 2002. вАФ –Ґ. 44 , вДЦ 2 . вАФ –°. 73вАФ77 . вАФ DOI :10.1053/jinf.2001.0948 PMID 12076064 .вЖС Barozzi P., Potenza L., Riva G., Vallerini D., Quadrelli C., Bosco R., Forghieri F., Torelli G., Luppi M. // Autoimmun Rev : journal. вАФ 2007. вАФ Vol. 7 , no. 2 . вАФ P. 132вАФ136 . вАФ DOI :10.1016/j.autrev.2007.02.018 PMID 18035323 .вЖС Subramanya D., Grivas P. D. // Postgrad Med : journal. вАФ 2008. вАФ Vol. 120 , no. 4 . вАФ P. 7вАФ13 . вАФ DOI :10.3810/pgm.2008.11.1928 PMID 19020360 .вЖС Crawford, Dorothy H. {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Oxford University Press , 2011. вАФ –°. 16. вАФ ISBN 0-19-957485-5 .вЖС Baggesen D. L., S√Єrensen G., Nielsen E. M., Wegener H. C. // Eurosurveillance [en] Vol. 15 , no. 4 . вАФ P. 19471 . вАФ PMID 20122382 .вЖС Systema Naturae 2000: Overview . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 26 —Б–µ—А–њ–љ—П 2005. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020 .вЖС Taxonomicon: Aphanobionta . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 14 –±–µ—А–µ–Ј–љ—П 2022. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020 .вЖС Taxonomicon: Acytota . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 7 –±–µ—А–µ–Ј–љ—П 2016. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020 .вЖС –°–Є—Б—В–µ–Љ–∞—В–Є–Ї–∞ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–Є—А–∞: –С–µ—Б–Ї–ї–µ—В–Њ—З–љ—Л–µ (Acellularia) . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 23 –ї—О—В–Њ–≥–Њ 2012. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 17 –±–µ—А–µ–Ј–љ—П 2013 .вЖС NCBI taxonomy . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 6 –Ї–≤—Ц—В–љ—П 2018. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020 .вЖС Lwoff A., Horne R. W., Tournier P. // C. R. Hebd. Seances Acad. Sci.. вАФ 1962. вАФ –°. 4225вАФ4227 .вЖС Lwoff A., Horne R., Tournier P. // Cold Spring Harb. Symp. Quant. Biol.. вАФ 1962. вАФ –°. 51вАФ55 .вЖС Delwart E. L. // Rev. Med. Virol.. вАФ 2007. вАФ вДЦ 2 . вАФ –°. 115вАФ131 .вЖС ICTV: Virus Taxonomy Assignments . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 28 –Ї–≤—Ц—В–љ—П 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 13 —Б—Ц—З–љ—П 2016 .вЖС Colson P., de Lamballerie X., Fournous G., Raoult D. –Р—А—Е—Ц–≤–Њ–≤–∞–љ–∞ –Ї–Њ–њ—Ц—П // Intervirology. вАФ 2012. вАФ –Ґ. 55 , –≤–Є–њ. 5 . вАФ –°. 321вАФ332 . вАФ DOI :10.1159/000336562 PMID 22508375 . –Р—А—Е—Ц–≤–Њ–≤–∞–љ–Њ –Ј –і–ґ–µ—А–µ–ї–∞ 30 –Ї–≤—Ц—В–љ—П 2017. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020.вЖС Taxonomy Release History . International Committee on Taxonomy of Viruses . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 2 —В—А–∞–≤–љ—П 2020. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020 .(–∞–љ–≥–ї.) –њ вЖС King A. M. Q., Lefkowitz E., Adams M. J., Carstens E. B. {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Elsevier , 2011. вАФ –°. 6. вАФ ISBN 0-12-384684-6 .вЖС Baltimore D. // Harvey Lect.. вАФ 1974. вАФ –Ґ. 70 Series . вАФ –°. 57вАФ74 . вАФ PMID 4377923 .вЖС Mayo M. A. // Arch. Virol. : journal. вАФ 1999. вАФ Vol. 144 , no. 8 . вАФ P. 1659вАФ1666 . вАФ DOI :10.1007/s007050050620 PMID 10486120 .вЖС de Villiers E. M., Fauquet C., Broker T. R., Bernard H. U., zur Hausen H. // Virology. вАФ 2004. вАФ –Ґ. 324 , вДЦ 1 . вАФ –°. 17вАФ27 . вАФ DOI :10.1016/j.virol.2004.03.033 PMID 15183049 .вЖС Baltimore D. // Harvey Lect.. вАФ 1974. вАФ –Ґ. 70 Series . вАФ –°. 57вАФ74 . вАФ PMID 4377923 .вЖС Temin H. M., Baltimore D. // Adv. Virus Res.. вАФ 1972. вАФ –Ґ. 17 . вАФ –°. 129вАФ186 . вАФ PMID 4348509 .вЖС Lazarowitz SD (2007) ¬ЂPlant viruses¬ї, in ¬ЂFields' Virology¬ї, 5th edition, volume 1, pp. 679вАФ683, Wolters Kluwer / Lippincott Williams & Wilkins, ISBN 0-7817-6060-7
вЖС Seeger C, Zoulin F, Mason WS (2007) ¬ЂHepadnaviruses¬ї, in ¬ЂFields' Virology¬ї, 5th edition, volume 2, pp. 2977-3029, Wolters Kluwer / Lippincott Williams & Wilkins, ISBN 0-7817-6060-7
вЖС The Big Picture Book of Viruses:Family Groups - The Baltimore Method . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 28 –Ї–≤—Ц—В–љ—П 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 21 —В—А–∞–≤–љ—П 2015 .вЖС Komaroff A. L. // J. Clin. Virol. : journal. вАФ 2006. вАФ P. S39вАФ46 .вЖС Chen C., Chiu Y., Wei F., Koong F., Liu H., Shaw C., Hwu H., Hsiao K. // Mol Psychiatry : journal. вАФ 1999. вАФ No. 1 . вАФ P. 33вАФ8 .вЖС Margolis T. P., Elfman F. L., Leib D., et al. // J. Virol. : journal. вАФ 2007. вАФ Vol. 81 , no. 20 . вАФ P. 11069вАФ11074 . вАФ DOI :10.1128/JVI.00243-07 PMID 17686862 .вЖС Whitley R. J., Roizman B. // The Lancet . вАФ Elsevier , 2001. вАФ Vol. 357 , no. 9267 . вАФ P. 1513вАФ1518 . вАФ DOI :10.1016/S0140-6736(00)04638-9 PMID 11377626 .вЖС Barton E. S., White D. W., Cathelyn J. S., et al. // Nature : journal. вАФ 2007. вАФ Vol. 447 , no. 7142 . вАФ P. 326вАФ329 . вАФ DOI :10.1038/nature05762 PMID 17507983 .вЖС Bertoletti A., Gehring A. // Hepatol. Res. : journal. вАФ 2007. вАФ Vol. 37 Suppl 3 . вАФ P. S331вАФ8 . вАФ DOI :10.1111/j.1872-034X.2007.00221.x PMID 17931183 .вЖС Rodrigues C., Deshmukh M., Jacob T., Nukala R., Menon S., Mehta A. // Indian journal of medical microbiology : journal. вАФ 2001. вАФ Vol. 19 , no. 3 . вАФ P. 141вАФ144 . вАФ PMID 17664817 .вЖС Nguyen V. T., McLaws M. L., Dore G. J. // Journal of Gastroenterology and Hepatology : journal. вАФ 2007. вАФ Vol. 22 , no. 12 . вАФ P. 2093вАФ2100 . вАФ DOI :10.1111/j.1440-1746.2007.05010.x PMID 17645465 .вЖС Fowler M. G., Lampe M. A., Jamieson D. J., Kourtis A. P., Rogers M. F. // American Journal of Obstetrics and Gynecology [en] Elsevier , 2007. вАФ Vol. 197 , no. 3 Suppl . вАФ P. S3вАФ9 . вАФ DOI :10.1016/j.ajog.2007.06.048 PMID 17825648 .вЖС Sauerbrei A., Wutzler P. // Journal of perinatology : official journal of the California Perinatal Association. вАФ 2000. вАФ –Ґ. 20 , вДЦ 8 Pt 1 . вАФ –°. 548вАФ554 . вАФ PMID 11190597 .вЖС Garnett G. P. // J. Infect. Dis. : journal. вАФ 2005. вАФ P. S97вАФ106 .[–љ–µ–і–Њ—Б—В—Г–њ–љ–µ –њ–Њ—Б–Є–ї–∞–љ–љ—П –Ј –Ш—О–ї—М 2019 ] вЖС Platonov A. E. // Vestn. Akad. Med. Nauk SSSR. вАФ 2006. вАФ вДЦ 2 . вАФ –°. 25вАФ9 .вЖС
Ranlet P. The British, the Indians, and smallpox: what actually happened at Fort Pitt in 1763? // Pa Hist : journal. вАФ 2000. вАФ Vol. 67 , no. 3 . вАФ P. 427вАФ441 . вАФ PMID 17216901 . –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 2008-09-16.Van Rijn K. "Lo! The poor Indian!" colonial responses to the 1862вАУ63 smallpox epidemic in British Columbia and Vancouver Island // Can Bull Med Hist : journal. вАФ 2006. вАФ Vol. 23 , no. 2 . вАФ P. 541вАФ560 . вАФ PMID 17214129 . –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 2008-09-16.Patterson K. B., Runge T. Smallpox and the Native American // Am. J. Med. Sci.. вАФ 2002. вАФ –Ґ. 323 , вДЦ 4 . вАФ –°. 216вАФ222 . вАФ DOI :10.1097/00000441-200204000-00009 PMID 12003378 .Sessa R., Palagiano C., Scifoni M. G., di Pietro M., Del Piano M. The major epidemic infections: a gift from the Old World to the New? // Panminerva Med : journal. вАФ 1999. вАФ Vol. 41 , no. 1 . вАФ P. 78вАФ84 . вАФ PMID 10230264 .Bianchine P. J., Russo T. A. The role of epidemic infectious diseases in the discovery of America // Allergy Proc : journal. вАФ 1992. вАФ Vol. 13 , no. 5 . вАФ P. 225вАФ232 . вАФ DOI :10.2500/108854192778817040 PMID 1483570 . –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 2008-09-16.Hauptman L. M. Smallpox and American Indian; Depopulation in Colonial New York // N Y State J Med : journal. вАФ 1979. вАФ Vol. 79 , no. 12 . вАФ P. 1945вАФ1949 . вАФ PMID 390434 .Fortuine R. Smallpox decimates the Tlingit (1787) // Alaska Med. вАФ 1988. вАФ –Ґ. 30 , вДЦ 3 . вАФ –°. 109 . вАФ PMID 3041871 . –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 2008-09-16. вЖС Patterson K. D., Pyle G. F. // Bull Hist Med. : journal. вАФ 1991. вАФ No. 1 . вАФ P. 4вАФ21 .вЖС Johnson N. P., Mueller J. // Bull Hist Med : journal. вАФ 2002. вАФ No. 1 . вАФ P. 105вАФ115 .вЖС Gao F., Bailes E., Robertson D. L., et al. // Nature : journal. вАФ 1999. вАФ No. 6718 . вАФ P. 436вАФ441 . [{{{archiveurl}}} –Р—А—Е—Ц–≤–Њ–≤–∞–љ–Њ] –Ј –і–ґ–µ—А–µ–ї–∞ 23 –ї—О—В–Њ–≥–Њ 2005.вЖС Status of the global HIV epidemic (PDF) . UNAIDS. 2008. –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г (PDF) –Ј–∞ 9 –±–µ—А–µ–Ј–љ—П 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 15 –≤–µ—А–µ—Б–љ—П 2008 .вЖС Towner J. S., Khristova M. L., Sealy T. K., et al. // J. Virol. : journal. вАФ 2006. вАФ No. 13 . вАФ P. 6497вАФ6516 .вЖС Einstein M. H., Schiller J. T., Viscidi R. P., Strickler H. D., Coursaget P., Tan T., Halsey N., Jenkins D. // The Lancet : journal. вАФ Elsevier , 2009. вАФ Vol. 9 , no. 6 . вАФ P. 347вАФ356 . вАФ DOI :10.1016/S1473-3099(09)70108-2 PMID 19467474 .вЖС Shuda M., Feng H., Kwun H. J., Rosen S. T., Gjoerup O., Moore P. S., Chang Y. // Proceedings of the National Academy of Sciences : journal. вАФ United States National Academy of Sciences , 2008. вАФ Vol. 105 , no. 42 . вАФ P. 16272вАФ16277 . вАФ DOI :10.1073/pnas.0806526105 PMID 18812503 .вЖС Pulitzer M. P., Amin B. D., Busam K. J. // Advances in Anatomic Pathology. вАФ 2009. вАФ –Ґ. 16 , вДЦ 3 . вАФ –°. 135вАФ144 . вАФ DOI :10.1097/PAP.0b013e3181a12f5a PMID 19395876 .вЖС Koike K. // J. Gastroenterol. Hepatol. : journal. вАФ 2007. вАФ Vol. 22 Suppl 1 . вАФ P. S108вАФ11 . вАФ DOI :10.1111/j.1440-1746.2006.04669.x PMID 17567457 .вЖС Hu J., Ludgate L. // Cancer Treat. Res. : journal. вАФ 2007. вАФ Vol. 133 . вАФ P. 241вАФ252 . вАФ DOI :10.1007/978-0-387-46816-7_9 PMID 17672044 .вЖС Bellon M., Nicot C. // Cancer genomics & proteomics : journal. вАФ 2007. вАФ Vol. 4 , no. 1 . вАФ P. 21вАФ5 . вАФ PMID 17726237 .вЖС Schiffman M., Castle P. E., Jeronimo J., Rodriguez A. C., Wacholder S. // The Lancet . вАФ Elsevier , 2007. вАФ Vol. 370 , no. 9590 . вАФ P. 890вАФ907 . вАФ DOI :10.1016/S0140-6736(07)61416-0 PMID 17826171 .вЖС Klein E., Kis L. L., Klein G. // Oncogene : journal. вАФ 2007. вАФ Vol. 26 , no. 9 . вАФ P. 1297вАФ1305 . вАФ DOI :10.1038/sj.onc.1210240 PMID 17322915 .вЖС zur Hausen H. // International Journal of Cancer. Journal International Du Cancer : journal. вАФ 2008. вАФ Vol. 123 , no. 2 . вАФ P. 247вАФ250 . вАФ DOI :10.1002/ijc.23620 PMID 18449881 .вЖС Alberts, Bruce; Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walters . {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ New York and London : Garland Science [en] ISBN 0-8153-3218-1 .вЖС Ding S. W., Voinnet O. // Cell . вАФ Cell Press , 2007. вАФ Vol. 130 , no. 3 . вАФ P. 413вАФ426 . вАФ DOI :10.1016/j.cell.2007.07.039 PMID 17693253 .вЖС Patton J. T., Vasquez-Del Carpio R., Spencer E. // Curr. Pharm. Des. : journal. вАФ 2004. вАФ Vol. 10 , no. 30 . вАФ P. 3769вАФ3777 . вАФ DOI :10.2174/1381612043382620 PMID 15579070 .вЖС Jayaram H., Estes M. K., Prasad B. V. // Virus Res. : journal. вАФ 2004. вАФ Vol. 101 , no. 1 . вАФ P. 67вАФ81 . вАФ DOI :10.1016/j.virusres.2003.12.007 PMID 15010218 .вЖС Greer S., Alexander G. J. // Baillieres Clin. Gastroenterol.. вАФ 1995. вАФ вДЦ 4 . вАФ –°. 689вАФ721 .вЖС Matter L., Kogelschatz K., Germann D. // J. Infect. Dis. : journal. вАФ 1997. вАФ No. 4 . вАФ P. 749вАФ755 .вЖС Mallery D. L., McEwan W. A., Bidgood S. R., Towers G. J., Johnson C. M., James L. C. // Proceedings of the National Academy of Sciences : journal. вАФ United States National Academy of Sciences , 2010. вАФ No. 46 (11). вАФ P. 19985вАФ19990 .вЖС Cascalho M., Platt J. L. Novel functions of B cells // Crit. Rev. Immunol.. вАФ 2007. вАФ вДЦ 2 (18 December). вАФ –°. 141вАФ151 .вЖС Le Page C., G√©nin P., Baines M. G., Hiscott J. Interferon activation and innate immunity // Rev Immunogenet. вАФ 2000. вАФ вДЦ 3 (18 December). вАФ –°. 374вАФ386 .вЖС Maurice R. Hilleman. Strategies and mechanisms for host and pathogen survival in acute and persistent viral infections // Proceedings of the National Academy of Sciences . вАФ National Academy of Sciences , 2004-10-05. вАФ Iss. suppl 2 . вАФ P. 14560вАФ14566 .вЖС Asaria P., MacMahon E. Measles in the United Kingdom: can we eradicate it by 2010? // BMJ : journal. вАФ 2006. вАФ No. 7574 . вАФ P. 890вАФ895 . –Р—А—Е—Ц–≤–Њ–≤–∞–љ–Њ –Ј –і–ґ–µ—А–µ–ї–∞ 7 –±–µ—А–µ–Ј–љ—П 2016. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020.вЖС Lane J. M. Mass vaccination and surveillance/containment in the eradication of smallpox // Curr. Top. Microbiol. Immunol. : journal. вАФ 2006. вАФ P. 17вАФ29 .вЖС Arvin A. M., Greenberg H. B. New viral vaccines // Virology. вАФ 2006. вАФ вДЦ 1 . вАФ –°. 240вАФ249 .вЖС Pastoret P. P., Schudel A. A., Lombard M. ConclusionsвАФfuture trends in veterinary vaccinology // Rev. вАУ Off. Int. Epizoot. : journal. вАФ 2007. вАФ No. 2 . вАФ P. 489вАФ494 .вЖС Palese P. Making better influenza virus vaccines? // Emerging Infect. Dis.. вАФ 2006. вАФ вДЦ 1 . вАФ –°. 61вАФ5 . –Р—А—Е—Ц–≤–Њ–≤–∞–љ–Њ –Ј –і–ґ–µ—А–µ–ї–∞ 2 –ґ–Њ–≤—В–љ—П 2012. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020.вЖС Thomssen R. Live attenuated versus killed virus vaccines // Monographs in allergy. вАФ 1975. вАФ –°. 155вАФ176 .вЖС McLean A. A. Development of vaccines against hepatitis A and hepatitis B // Rev. Infect. Dis. : journal. вАФ 1986. вАФ No. 4 . вАФ P. 591вАФ598 .вЖС Casswall T. H., Fischler B. Vaccination of the immunocompromised child // Expert review of vaccines. вАФ 2005. вАФ вДЦ 5 . вАФ –°. 725вАФ738 .вЖС Barnett E. D., Wilder-Smith A., Wilson M. E. Yellow fever vaccines and international travelers // Expert Rev Vaccines. вАФ 2008. вАФ вДЦ 5 . вАФ –°. 579вАФ587 .вЖС Magden J., K√§√§ri√§inen L., Ahola T. // Appl. Microbiol. Biotechnol. : journal. вАФ 2005. вАФ No. 6 . вАФ P. 612вАФ621 .вЖС Mindel A., Sutherland S. // J. Antimicrob. Chemother. : journal. вАФ 1983. вАФ P. 51вАФ9 .вЖС Witth√ґft T., M√ґller B., Wiedmann K. H., et al. // J. Viral Hepat. : journal. вАФ 2007. вАФ Vol. 14 , no. 11 . вАФ P. 788вАФ796 . вАФ DOI :10.1111/j.1365-2893.2007.00871.x PMID 17927615 .вЖС Rudin D., Shah S. M., Kiss A., Wetz R. V., Sottile V. M. // Liver Int. : journal. вАФ 2007. вАФ Vol. 27 , no. 9 . вАФ P. 1185вАФ1193 . вАФ DOI :10.1111/j.1478-3231.2007.01580.x PMID 17919229 .вЖС Goris N., Vandenbussche F., De Clercq K. // Antiviral Res. : journal. вАФ 2008. вАФ No. 1 . вАФ P. 170вАФ178 .вЖС Carmichael L. // J. Vet. Med. B Infect. Dis. Vet. Public Health : journal. вАФ 2005. вАФ No. 7вАФ8 . вАФ P. 303вАФ311 .вЖС Tinsley T. W., Harrap K. A. Viruses of Invertebrates (–∞–љ–≥–ї.) . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 7 —З–µ—А–≤–љ—П 2018. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 27 –ї—О—В–Њ–≥–Њ 2013 . вЖС Invertebrate iridescent viruses (Iridoviridae) (–∞–љ–≥–ї.) . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 13 –≤–µ—А–µ—Б–љ—П 2019. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 27 –ї—О—В–Њ–≥–Њ 2013 .вЖС –Т–Є—А—Г—Б—Л –±–µ—Б–њ–Њ–Ј–≤–Њ–љ–Њ—З–љ—Л—Е (—А–Њ—Б.) . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 24 –ї—О—В–Њ–≥–Њ 2020. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 27 –ї—О—В–Њ–≥–Њ 2013 .вЖС Chen Y. P., Zhao Y., Hammond J., Hsu H., Evans J. D., Feldlaufer M. F. Multiple virus infections in the honey bee and genome divergence of honey bee viruses // Journal of Invertebrate Pathology : journal. вАФ No. 2вАФ3 . вАФ P. 84вАФ93 .вЖС Rybicki EP (2015) ¬ЂA Top Ten list for economically important plant viruses¬ї, Archives of Virology 160:17-20
вЖС Dinesh-Kumar S. P., Tham Wai-Hong, Baker B. J. // Proceedings of the National Academy of Sciences : journal. вАФ National Academy of Sciences , 2000. вАФ No. 26 . вАФ P. 14789вАФ14794 .вЖС Soosaar J. L., Burch-Smith T. M., Dinesh-Kumar S. P. // Nat. Rev. Microbiol. вАФ 2005. вАФ вДЦ 10 . вАФ –°. 789вАФ798 .вЖС Lomonossoff G. P. Virus Particles and the Uses of Such Particles in Bio- and Nanotechnology // {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Caister Academic Press [en] ISBN 978-1-904455-75-2 .вЖС –∞ –± –Т–Є—А—Г—Б—Л –≥—А–Є–±–Њ–≤ (—А–Њ—Б.) . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 5 –≤–µ—А–µ—Б–љ—П 2019. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 27 –ї—О—В–Њ–≥–Њ 2013 .вЖС Mycophages: Are they ideal antifungal agents? . The Phage - Exploring the virus of microbes (–±—А–Є—В.) . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 9 –±–µ—А–µ–Ј–љ—П 2022. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 9 –±–µ—А–µ–Ј–љ—П 2022 .вЖС McGraw-Hill Science & Technology Encyclopedia: Fungal virus (–∞–љ–≥–ї.) . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 4 –±–µ—А–µ–Ј–љ—П 2016. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 27 –ї—О—В–Њ–≥–Њ 2013 .вЖС –Ф—М—П–Ї–Њ–≤ –Ѓ. –Ґ., –®–љ—Л—А–µ–≤–∞ –Р. –Т., –°–µ—А–≥–µ–µ–≤ –Р. –Ѓ. {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ –Ь. : –Є–Ј–і. —Ж–µ–љ—В—А ¬Ђ–Р–Ї–∞–і–µ–Љ–Є—П¬ї, 2005. вАФ –°. 57вАФ58. вАФ ISBN 5-7695-2174-0 .вЖС –С–µ–ї—П–Ї–Њ–≤–∞ –У. –Р., –Ф—М—П–Ї–Њ–≤ –Ѓ. –Ґ., –Ґ–∞—А–∞—Б–Њ–≤ –Ъ. –Ы. {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ –Ь. : –Є–Ј–і. —Ж–µ–љ—В—А ¬Ђ–Р–Ї–∞–і–µ–Љ–Є—П¬ї, 2006. вАФ –°. 73. вАФ ISBN 5-7695-2731-5 .вЖС International Society for Viruses of Microorganisms: Protist Viruses (–∞–љ–≥–ї.) . –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 28 –ї—О—В–Њ–≥–Њ 2013 .[–љ–µ–і–Њ—Б—В—Г–њ–љ–µ –њ–Њ—Б–Є–ї–∞–љ–љ—П –Ј –Т–µ—А–µ—Б–µ–љ—М 2018 ] вЖС Philippe Colson, Gregory Gimenez, Micka√Ђl Boyer, Ghislain Fournous, Didier Raoult. .вЖС Wommack K. E., Colwell R. R. // Microbiol. Mol. Biol. Rev.. вАФ 2000. вАФ вДЦ 1 . вАФ –°. 69вАФ114 .вЖС Bergh O., B√Єrsheim K. Y., Bratbak G., Heldal M. // Nature : journal. вАФ 1989. вАФ No. 6233 . вАФ P. 467вАФ468 .вЖС Bickle T. A., Kr√Љger D. H. // Microbiology and Molecular Biology Reviews [en] American Society for Microbiology [en] Vol. 57 , no. 2 , P. 434вАФ450 . вАФ PMID 8336674 .вЖС Barrangou R., Fremaux C., Deveau H. et al. // Science. вАФ 2007. вАФ Vol. 315 , no. 5819 . вАФ P. 1709вАФ1712 . вАФ PMID 17379808 .вЖС Brouns S. J., Jore M. M., Lundgren M., et al. // Science. вАФ 2008. вАФ Vol. 321 , no. 5891 . вАФ P. 960вАФ964 . вАФ PMID 18703739 .вЖС –Т. –Ь. –Ц–і–∞–љ–Њ–≤ .–Э–∞—Г–Ї–∞ –Є —З–µ–ї–Њ–≤–µ—З–µ—Б—В–≤–Њ , 1984. вАФ –Ь. : –Ч–љ–∞–љ–Є–µ . вАФ –°. 44вАФ55 .вЖС Xiang X., Chen L., Huang X., Luo Y., She Q., Huang L. // J. Virol. : journal. вАФ 2005. вАФ Vol. 79 , no. 14 . вАФ P. 8677вАФ8686 . вАФ DOI :10.1128/JVI.79.14.8677-8686.2005 PMID 15994761 .вЖС Robb F., Antranikian G., Grogan D., Driessen A. (Editors) (2007) ¬ЂThermophiles: Biology and Technology at High Temperatures¬ї, CRC Press, ISBN 978-0849392146 , pp. 231вАФ232
вЖС Krupovic M. , Bamford D. , Emmanuelle R J Quemin Unification of the globally distributed spindle-shaped viruses of the Archaea // J. Virol. вАФ ASM , 2013. вАФ Vol. 88, Iss. 4. вАФ P. 2354вАУ2358. вАФ ISSN 0022-538X ; 1098-5514 ; 1070-6321 вАФ doi:10.1128/JVI.02941-13 вЖС C. Martin Lawrence Large Tailed Spindle Viruses of Archaea: a New Way of Doing Viral Business // J. Virol. вАФ ASM , 2015. вАФ Vol. 89, Iss. 18. вАФ P. 9146вАУ9. вАФ ISSN 0022-538X ; 1098-5514 ; 1070-6321 вАФ doi:10.1128/JVI.00612-15 вЖС ¬ЂUneven Distribution of Viruses Suggests Surprising Evolutionary Power¬ї, Scientific American
вЖС Prangishvili D., Forterre P., Garrett R. A. // Nat. Rev. Microbiol.. вАФ 2006. вАФ –Ґ. 4 , вДЦ 11 . вАФ –°. 837вАФ848 . вАФ DOI :10.1038/nrmicro1527 PMID 17041631 .вЖС Prangishvili D., Garrett R.A. // Biochem. Soc. Trans. : journal. вАФ 2004. вАФ Vol. 32 , no. Pt 2 . вАФ P. 204вАФ208 . вАФ DOI :10.1042/BST0320204 PMID 15046572 .[–љ–µ–і–Њ—Б—В—Г–њ–љ–µ –њ–Њ—Б–Є–ї–∞–љ–љ—П –Ј –Т–µ—А–µ—Б–µ–љ—М 2018 ] вЖС Mojica F. J., D√≠ez-Villase√±or C., Garc√≠a-Mart√≠nez J., Soria E. // J. Mol. Evol. : journal. вАФ 2005. вАФ Vol. 60 , no. 2 . вАФ P. 174вАФ182 . вАФ DOI :10.1007/s00239-004-0046-3 PMID 15791728 .вЖС Makarova K. S., Grishin N. V., Shabalina S. A., Wolf Y. I., Koonin E. V. // Biol. Direct : journal. вАФ 2006. вАФ Vol. 1 . вАФ P. 7 . вАФ DOI :10.1186/1745-6150-1-7 PMID 16545108 .вЖС La Scola B., Desnues C., Pagnier I., Robert C., Barrassi L., Fournous G., Merchat M., Suzan-Monti M., Forterre P., Koonin E., Raoult D. // Nature. вАФ 2008. вАФ Iss. 7209 . вАФ P. 100вАФ104 .вЖС Helen Pearson (2008). 'Virophage' suggests viruses are alive . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 10 –ї—О—В–Њ–≥–Њ 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 2 –ї—О—В–Њ–≥–Њ 2013 . вЖС –Р–ї–µ–Ї—Б–∞–љ–і—А –Ь–∞—А–Ї–Њ–≤ (8 –≤–µ—А–µ—Б–љ—П 2008). –Т–Є—А—Г—Б—Л —В–Њ–ґ–µ –±–Њ–ї–µ—О—В –≤–Є—А—Г—Б–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 10 –ї—О—В–Њ–≥–Њ 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 2 –ї—О—В–Њ–≥–Њ 2013 . вЖС Desnues C., Boyer M., Raoult D. // Adv Virus Res. вАФ 2012. вАФ –°. 63вАФ89 .вЖС Claverie J. M., Abergel C. // Annu Rev Genet. вАФ 2009. вАФ –°. 49вАФ66 .вЖС PMID 23408616 (PMID 23408616 )–С—Ц–±–ї—Ц–Њ–≥—А–∞—Д—Ц—З–љ–Є–є –Њ–њ–Є—Б –Ј'—П–≤–Є—В—М—Б—П –∞–≤—В–Њ–Љ–∞—В–Є—З–љ–Њ —З–µ—А–µ–Ј –і–µ—П–Ї–Є–є —З–∞—Б. –Т–Є –Љ–Њ–ґ–µ—В–µ –њ—Ц–і—Б—В–∞–≤–Є—В–Є —Ж–Є—В–∞—В—Г –≤–ї–∞—Б–љ–Њ—А—Г—З –∞–±–Њ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—З–Є –±–Њ—В–∞ . вЖС PMID 23091035 (PMID 23091035 )–С—Ц–±–ї—Ц–Њ–≥—А–∞—Д—Ц—З–љ–Є–є –Њ–њ–Є—Б –Ј'—П–≤–Є—В—М—Б—П –∞–≤—В–Њ–Љ–∞—В–Є—З–љ–Њ —З–µ—А–µ–Ј –і–µ—П–Ї–Є–є —З–∞—Б. –Т–Є –Љ–Њ–ґ–µ—В–µ –њ—Ц–і—Б—В–∞–≤–Є—В–Є —Ж–Є—В–∞—В—Г –≤–ї–∞—Б–љ–Њ—А—Г—З –∞–±–Њ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—З–Є –±–Њ—В–∞ . вЖС La Scola B., Campocasso A., N'Dong R., Fournous G., Barrassi L., Flaudrops C., Raoult D. // Intervirology. вАФ 2010. вАФ –Т–Є–њ. 5 . вАФ –°. 344вАФ353 .вЖС PMID 27886075 (PMID 27886075 )–С—Ц–±–ї—Ц–Њ–≥—А–∞—Д—Ц—З–љ–Є–є –Њ–њ–Є—Б –Ј'—П–≤–Є—В—М—Б—П –∞–≤—В–Њ–Љ–∞—В–Є—З–љ–Њ —З–µ—А–µ–Ј –і–µ—П–Ї–Є–є —З–∞—Б. –Т–Є –Љ–Њ–ґ–µ—В–µ –њ—Ц–і—Б—В–∞–≤–Є—В–Є —Ж–Є—В–∞—В—Г –≤–ї–∞—Б–љ–Њ—А—Г—З –∞–±–Њ –≤–Є–Ї–Њ—А–Є—Б—В–Њ–≤—Г—О—З–Є –±–Њ—В–∞ . вЖС ScienceNow вАФ ¬ЂAncient Virus Gave Wasps Their Sting¬ї . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 15 –Ї–≤—Ц—В–љ—П 2011. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 26 –±–µ—А–µ–Ј–љ—П 2011 .вЖС –≠–ї–µ–Љ–µ–љ—В—Л вАФ –љ–Њ–≤–Њ—Б—В–Є –љ–∞—Г–Ї–Є: –Э–∞–µ–Ј–і–љ–Є–Ї–Є –њ–Њ–і–∞–≤–ї—П—О—В –Є–Љ–Љ—Г–љ–љ—Г—О –Ј–∞—Й–Є—В—Г —Б–≤–Њ–Є—Е –ґ–µ—А—В–≤ –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –њ—А–Є—А—Г—З–µ–љ–љ—Л—Е –≤–Є—А—Г—Б–Њ–≤ . –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 17 –ї–Є—Б—В–Њ–њ–∞–і–∞ 2016. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 22 –±–µ—А–µ–Ј–љ—П 2020 .вЖС Breitbart M. // Annual Review of Marine Science. вАФ 2012. вАФ –°. 425вАФ448 .вЖС Suttle C. A. // Nature. вАФ 2005. вАФ No. 7057 . вАФ P. 356вАФ361 .[–љ–µ–і–Њ—Б—В—Г–њ–љ–µ –њ–Њ—Б–Є–ї–∞–љ–љ—П –Ј –Т–µ—А–µ—Б–µ–љ—М 2018 ] вЖС National Center for Environmental Health (24 –ї–Є–њ–љ—П 2012). Harmful Algal Blooms (–∞–љ–≥–ї.) . Centers for disease control and prevention. –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 21 –±–µ—А–µ–Ј–љ—П 2013. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 8 –±–µ—А–µ–Ј–љ—П 2013 . вЖС –∞ –± –≤ Suttle C. A. // Nature Reviews. Microbiology : journal. вАФ 2007. вАФ Vol. 5 , no. 10 . вАФ P. 801вАФ812 . вАФ DOI :10.1038/nrmicro1750 PMID 17853907 .вЖС Hall, A. J., Jepson, P. D., Goodman, S. J. & Harkonen, T. ¬ЂPhocine distemper virus in the North and European Seas вАФ data and models, nature and nurture¬ї. Biol. Conserv. 131, 221вАФ229 (2006).
вЖС Suttle C. A. Marine virusesвАФmajor players in the global ecosystem // Nature Reviews. Microbiology : journal. вАФ 2007. вАФ No. 10 (18 December). вАФ P. 801вАФ812 .вЖС Canchaya C., Fournous G., Chibani-Chennoufi S., Dillmann M. L., Br√Љssow H. Phage as agents of lateral gene transfer // Curr. Opin. Microbiol.. вАФ 2003. вАФ вДЦ 4 (18 December). вАФ –°. 417вАФ424 .вЖС Forterre P., Philippe H. The last universal common ancestor (LUCA), simple or complex? // The Biological Bulletin : journal. вАФ 1999. вАФ No. 3 (18 December). вАФ P. 373вАФ375 .вЖС Lodish, Harvey; Berk, Arnold; Zipursky, S. Lawrence; Matsudaira, Paul; Baltimore, David; Darnell, James. Viruses: Structure, Function, and Uses Retrieved on September 16, 2008
вЖС Matsuzaki S., Rashel M., Uchiyama J., Sakurai S., Ujihara T., Kuroda M., Ikeuchi M., Tani T., Fujieda M., Wakiguchi H., Imai S. // Journal of Infection and Chemotherapy : Official Journal of the Japan Society of Chemotherapy : journal. вАФ 2005. вАФ Vol. 11 , no. 5 (10). вАФ P. 211вАФ219 . вАФ DOI :10.1007/s10156-005-0408-9 PMID 16258815 .вЖС Gleba, Y. Y.; Giritch, A. Plant Viral Vectors for Protein Expression // {{{–Ч–∞–≥–Њ–ї–Њ–≤–Њ–Ї}}}. вАФ Caister Academic Press [en] ISBN 978-1-904455-75-2 .вЖС Fischlechner M., Donath E. // Angewandte Chemie International Edition : journal. вАФ 2007. вАФ No. 18 . вАФ P. 3184вАФ3193 .вЖС Soto C. M., Blum A. S., Vora G. J., et al. // J. Am. Chem. Soc. : journal. вАФ 2006. вАФ Vol. 128 , no. 15 . вАФ P. 5184вАФ5189 . вАФ DOI :10.1021/ja058574x PMID 16608355 .вЖС Blum A. S., Soto C. M., Wilson C. D. et al. // Small : journal. вАФ 2005. вАФ Vol. 7 . вАФ P. 702 . вАФ DOI :10.1002/smll.200500021 PMID 17193509 .вЖС Coleman J. R., Papamichail D., Skiena S., Futcher B., Wimmer E., Mueller S. // Science : journal. вАФ 2008. вАФ No. 5884 . вАФ P. 1784вАФ1787 .вЖС Genomes. NIH viral genome database . Ncbi.nlm.nih.gov. –Р—А—Е—Ц–≤ –Њ—А–Є–≥—Ц–љ–∞–ї—Г –Ј–∞ 14 –ї—О—В–Њ–≥–Њ 2014. –Я—А–Њ—Ж–Є—В–Њ–≤–∞–љ–Њ 7 —В—А–∞–≤–љ—П 2012 . вЖС Artenstein A. W., Grabenstein J. D. // Expert Review of Vaccines : journal. вАФ 2008. вАФ No. 8 . вАФ P. 1225вАФ1237 .вЖС Arag√≥n T. J., Ulrich S., Fernyak S., Rutherford G. W. // BMC public health : journal. вАФ 2003. вАФ P. 26 .вЖС Weiss M. M., Weiss P. D., Mathisen G., Guze P. // Clin. Infect. Dis.. вАФ 2004. вАФ вДЦ 11 . вАФ –°. 1668вАФ1673 .вЖС –∞ –± –≤ –≥ Georgios Pappas, Savvas Seitaridis, Nikolaos Akritidis, Epaminondas Tsianos. // Clinical Infectious Diseases : oxford Journals. вАФ 2003. вАФ Vol. 37 , no. 7 . вАФ P. 939вАФ942 . вАФ DOI :10.1086/377740
–Р–≤—В–Њ—А—Б—М–Ї–Є–є –Ї–Њ–ї–µ–Ї—В–Є–≤, –Ј–∞ —А–µ–і. –Т.–Я. –®–Є—А–Њ–±–Њ–Ї–Њ–≤–∞ . –Ь–µ–і–Є—З–љ–∞ –Љ—Ц–Ї—А–Њ–±—Ц–Њ–ї–Њ–≥—Ц—П, –≤—Ц—А—Г—Б–Њ–ї–Њ–≥—Ц—П —В–∞ —Ц–Љ—Г–љ–Њ–ї–Њ–≥—Ц—П. вАФ –Т—Ц–љ–љ–Є—Ж—П : –Э–Њ–≤–∞ –Ъ–љ–Є–≥–∞, 2011. вАФ 952 —Б. вАФ 2000 –њ—А–Є–Љ. вАФ ISBN 978-966-382-325-6 .–У—Г–і–Ј—М –°. –Я., –Я–µ—А–µ—В—П—В–Ї–Њ –Ґ. –С., –Я–∞–≤–ї–Њ–≤–∞ –Ѓ. –Ю. –Ч–∞–≥–∞–ї—М–љ–∞ –≤—Ц—А—Г—Б–Њ–ї–Њ–≥—Ц—П. –Э–∞–≤—З–∞–ї—М–љ–Є–є –њ–Њ—Б—Ц–±–љ–Є–Ї. вАФ –Ы—М–≤—Ц–≤: –Т–Є–і–∞–≤–љ–Є—З–Є–є —Ж–µ–љ—В—А –Ы–Э–£ —Ц–Љ. –Ж–≤–∞–љ–∞ –§—А–∞–љ–Ї–∞, 2010. вАФ 264 —Б. ISBN 9789666137534
–Ґ–∞—И—Г—В–∞ –°. –У. –Ч–∞–≥–∞–ї—М–љ–∞ –≤—Ц—А—Г—Б–Њ–ї–Њ–≥—Ц—П: –Я–Њ—Б—Ц–±–љ–Є–Ї. вАФ –Ъ–Є—Ч–≤:, 2004. вАФ 458 —Б.
–Т—Ц—А—Г—Б–Њ—Б—Д–µ—А–∞: –≤—Ц–і –Ј–∞—Б—В—Г–і–Є –і–Њ COVID вАФ –љ–∞–≤—Ц—Й–Њ –ї—О–і—Б—В–≤—Г –≤—Ц—А—Г—Б–Є / –§. –†–∞—П–љ ; [–њ–µ—А. –Ј –∞–љ–≥–ї.: –Э. –Я–∞–ї—Ц–є, –†. –°–≤—П—В–Њ]. вАФ –Ъ–Є—Ч–≤: Yakaboo Publishing, 2020. вАФ 304 —Б. ISBN 978-617-7544-70-7
Fields Virology: Emerging Viruses. Howley, Peter M.; Knipe, David M.; Whelan, Sean/ Lippincott Williams & Wilkins (LWW), 2020.- 1256 p. ISBN 978-1-97-511254-7 Mayo M. A., Pringle C. R. Virus taxonomy вАФ 1997 // Journal of General Virology [en] Microbiology Society [en] No. 79 . вАФ P. 649вАФ657 . –Р—А—Е—Ц–≤–Њ–≤–∞–љ–Њ –Ј –і–ґ–µ—А–µ–ї–∞ 29 –≤–µ—А–µ—Б–љ—П 2007.Collier, Leslie; Balows, Albert; Sussman, Max. Topley and WilsonвАЩs Microbiology and Microbial Infections / Mahy, Brian and Collier, Leslie. Arnold. вАФ ninth edition. вАФ Virology, 1998. вАФ –Ґ. 1. вАФ ISBN 0-340-66316-2 .Dimmock, N.J.; Easton, Andrew J.; Leppard, Keith. Introduction to Modern Virology. вАФ sixth edition. вАФ Blackwell Publishing, 2007. вАФ ISBN 1-4051-3645-6 .Knipe, David M.; Howley, Peter M.; Griffin, Diane E.; Lamb, Robert A.; Martin, Malcolm A.; Roizman, Bernard; Straus Stephen E. Fields Virology. вАФ Lippincott Williams & Wilkins, 2007. вАФ ISBN 0-7817-6060-7 .Shors, Teri. Understanding Viruses. вАФ Jones and Bartlett Publishers, 2008. вАФ ISBN 0-7637-2932-9 .–С—Г–Ї—А–Є–љ—Б–Ї–∞—П –Р. –У. –Т–Є—А—Г—Б–Њ–ї–Њ–≥–Є—П. вАФ –Ь–µ–і–Є—Ж–Є–љ–∞, 1986. вАФ 336 —Б.
–С–∞–Ј–Є –і–∞–љ–Є—Е —В–∞–Ї—Б–Њ–љ—Ц–≤