| Rezorcin
|
![]()
Rezorcin |

3 dimenziós
szerkezet
|
| IUPAC-név |
Benzol-1,3-diol
|
| Más nevek |
1,3-dihidroxibenzol, m-dihidroxibenzol
|
| Kémiai azonosítók
|
| CAS-szám |
108-46-3
|
| ATC kód |
D10AX02, S01AX06
|
| Gyógyszer szabadnév |
resorcinol
|
| Gyógyszerkönyvi név |
Resorcinolum
|
|
|
|
|
| Kémiai és fizikai tulajdonságok
|
| Kémiai képlet |
C6H4(OH)2
|
| Moláris tömeg |
110,11 g/mol
|
| Megjelenés |
színtelen, kristályos
|
| Sűrűség |
1,28 g/cm³ (20 °C)[1]
|
| Olvadáspont |
111 °C[1]
|
| Forráspont |
277 °C[1]
|
| Oldhatóság (vízben) |
Jól oldódik
840 g/l (0 °C)
1400 g/l (20 °C)
2650 g/l (40 °C)
5000 g/l (80 °C)[1]
|
| Gőznyomás |
1 Pa (20 °C)[1]
|
| Veszélyek
|
| EU osztályozás |
Ártalmas (Xn)
Veszélyes a környezetre (N)[1]
|
| R mondatok |
R22, R36/38, R50[1]
|
| S mondatok |
(S2), S26, S61[1]
|
| Lobbanáspont |
127 °C[1]
|
| Öngyulladási hőmérséklet |
605 °C[1]
|
| LD50 |
301 mg/kg (patkány, szájon át)
3360 mg/kg (házinyúl, bőrön keresztül)[2]
|
| Rokon vegyületek
|
| Rokon kétértékű fenolok |
Pirokatechin
Hidrokinon
|
| Az infoboxban SI-mértékegységek szerepelnek. Ahol lehetséges, az adatok standardállapotra (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. Az ezektől való eltérést egyértelműen jelezzük.
|
A rezorcin egy szerves vegyület, kétértékű fenol. A molekula benzolgyűrűt tartalmaz, ehhez két hidroxilcsoport kapcsolódik meta-helyzetben. Neve a latin resina (mézga, fagyanta) és az olasz oricello (zuzmókból nyert ibolyaszínű festék) összetételéből származik.[3]
Két izomerje van, ezek a pirokatechin és a hidrokinon. Színtelen, kristályos vegyület. Édes íze van. Vízben, alkoholban és éterben igen jól, kloroformban rosszabbul oldódik. A bőrgyógyászatban antiszeptikumként (fertőtlenítésre), illetve festékek és műanyagok gyártására használják.
Bőrizgató hatású vegyület, a bőrön kiütéseket okozhat.
Kémiai tulajdonságai
A rezorcin redukáló tulajdonságú vegyület. Könnyen oxidálódik, különösen lúgos kémhatású oldatban. Ekkor a színe sötétebb lesz. Ibolya színreakciót ad a vas(III)-ionokkal, még nagy hígítás esetén is. A rezorcin hajlamos szubsztitúciós reakciókra, ez a hajlam hidroxilcsoportok m-helyzetével magyarázható. A szubsztitúciós reakciók 2-es és 4-es helyzetben mennek végbe a legkönnyebben.
A vegyület elméleti szempontból jelentős reakciója, hogy nátriumamalgám hatására ciklohexán-1,3-dionná alakul. Ez arra utal, hogy a vegyületnek van egy tautomer, diketon alakja. Ebben a reakcióban a vegyületnek ez az alakja vesz részt. A reakció igen könnyen végbemegy.
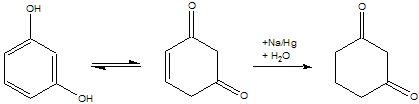
Előállítása
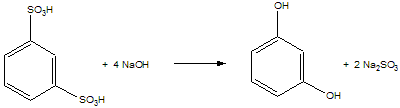
A rezorcint benzol-1,3-diszulfonsav alkáliömlesztésével állítható elő. A benzol-1,3-diszulfonsav legegyszerűbben benzolból nyerhető. Az alkáliömlesztést nátrium-hidroxiddal vagy kálium-hidroxiddal végzik.
Felhasználása
A rezorcint a bőrgyógyászatban fertőtlenítésre (antiszeptikumként) használják, ugyanis kevésbé mérgező, mint a fenol és kevésbé izgatja a bőrt. Emellett számos jelentős anyagot rezorcinból állítanak elő. Kiindulási anyag többféle festék előállításánál, ilyenek például a fluoreszcein és az eozin. Emellett felhasználják a műanyagiparban és egyes gyógyszerek gyártására. Adalékanyagként használják a gumigyártásban. Szintetikus ragasztók készítésére is használják.
Jegyzetek
Források
- Erdey-Grúz Tibor: Vegyszerismeret
- Bruckner Győző: Szerves kémia, II/1-es kötet
- Bot György: A szerves kémia alapjai
|
|---|
| Alkoholok | Egyértékű alkoholok | |
|---|
Többértékű alkoholok | |
|---|
|
|---|
| Enolok | |
|---|
| Fenolok | Egyértékű fenolok | |
|---|
Többértékű fenolok | |
|---|
|
|---|