ซีนอนเฮกซะฟลูออโรแพลทิเนต
![]()
|
| ชื่อ
|
| ชื่ออื่น
Xenon(I) hexafluoroplatinate
|
| เลขทะเบียน
|
|
|
|
|
|
|
F[Xe+].F[Pt-1](F)(F)(F)(F)F F[Xe+].F[Pt-1](F)(F)(F)(F)(F)Pt(F)(F)(F)(F)F
|
| คุณสมบัติ
|
|
|
Xe+[PtF6]−
|
| มวลโมเลกุล
|
440.367
|
| ลักษณะทางกายภาพ
|
ของแข็งสีส้ม
|
|
|
Chemical compound
ซีนอนเฮกซะฟลูออโรแพลทิเนต เป็นชื่อของสารประกอบที่เกิดจากการรวมตัวกันของก๊าซซีนอนและแพลทินัมเฮกซะฟลูออไรด์ ในการทดลองเพื่อพิสูจน์ความสามารถในการทำปฏิกิริยาทางเคมีของแก๊สมีสกุล โดยนีล บาร์เลตต์จากมหาวิทยาลัยบริติชโคลัมเบียได้ให้สูตรของสารประกอบนี้ว่า "Xe+[PtF6]−" แม้ว่างานวิจัยในระยะเวลาต่อมาจะชี้ให้เห็นว่าสารประกอบที่ได้เป็นของผสมของสารประกอบหลายชนิด ไม่ใช่เป็นสารบริสุทธิ์[1]
การเตรียม
สามารถเตรียมได้จากซีนอนและแพลทินัมเฮกซะฟลูออไรด์ (PtF6) ซึ่งละลายใน SF6 สารตั้งต้นจะผสมรวมกันที่ 77 เคลวิน และอุณหภูมิจะค่อยๆ เพิ่มสูงขึ้นอย่างช้า ๆ
โครงสร้าง
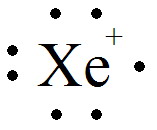 ไอออน Xe+
ไอออน Xe+
โครงสร้างของสารประกอบนี้ไม่ได้เป็นอย่างที่บาร์เลตต์คาดไว้ เนื่องจากไอออนบวกที่บาร์เลตต์เสนอไว้คือ "Xe+" นั้นมีอิเล็กตรอนเดี่ยว ดังภาพด้านขวา จะเห็นว่าอิเล็กตรอนวงนอกสุดนั้นยังไม่ครบแปดตัว จึงสามารถเกิดพันธะกับอะตอมหนึ่งของฟลูออรีนเกิดเป็น XeF+ ดังนั้นบาร์เลตต์จึงสรุปว่าซีนอนได้เข้าทำปฏิกิริยาด้วย แต่ทว่าความเป็นธรรมชาติและความบริสุทธิ์ของผลิตภัณฑ์สีเหลืองมัสตาร์ดยังไม่เป็นที่แน่ชัด[2] เนื่องจากงานวิจัยชิ้นถัดมาบ่งชี้ว่า สารผลิตภัณฑ์ที่บาร์เลตต์เตรียมได้นั้นอาจเป็นสารผสมระหว่าง [XeF]+[PtF5]−, [XeF]+[Pt2F11]− และ [Xe2F3]+[PtF6]−[3] ซึ่งสารประกอบเหล่านี้เป็นเกลือซึ่งมีไอออนบวกมีซีนอนเป็นองค์ประกอบ และมีแพลทินัมเป็นองค์ประกอบของไอออน[4]
ประวัติ
เมื่อ ค.ศ. 1962 นีล บาร์เลตต์ค้นพบว่าสารผสมของแพลทินัมเฮกซะฟลูออไรด์กับก๊าซออกซิเจนเกิดปฏิกิริยากันได้ของแข็งสีแดง[5][6] พบว่าของแข็งสีแดงที่ได้นั้นคือไดออกซิเจนิล เฮกซะฟลูออโรแพลทิเนต (O+
2[PtF6]−) และเขาก็ทราบว่าค่าพลังงานไอออไนเซชันของโมเลกุลออกซิเจนและอะตอมซีนอนมีค่าใกล้เคียงกัน เขาจึงขอให้เพื่อนร่วมงานนำซีนอนส่วนหนึ่งมาเพื่อทดสอบการทำปฏิกิริยา[7] ซึ่งเขาพบว่าซีนอนก็ทำปฏิกิริยาจริง ๆ แม้ว่าสารผลิตภัณฑ์ที่ได้จะไม่บริสุทธิ์เท่าไรนัก แต่งานของเขาก็สามารถพิสูจน์ได้ว่าเราสามารถเตรียมสารประกอบจากแก๊สมีสกุลได้ การค้นพบของเขาเป็นตัวอย่างของการค้นพบสารประกอบของธาตุเหล่านี้ และได้มีการค้นพบสารประกอบประเภทฟลูออไรด์ของซีนอนในระยะเวลาต่อมา[3]
ดูเพิ่ม
อ้างอิง
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth–Heinemann. ISBN 0080379419.
- ↑ Graham, Lionell; Graudejus, Oliver; Jha, Narendra K.; Bartlett, Neil (2000). "Concerning the nature of XePtF6". Coordination Chemistry Reviews. 197 (1): 321–334. doi:10.1016/S0010-8545(99)00190-3.
- ↑ 3.0 3.1 Holleman, Arnold Frederick; Wiberg, Egon (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 0-12-352651-5.
- ↑ Sampson, Mark T. (May 23, 2006). Neil Bartlett and the Reactive Noble Gases (PDF). National Historic Chemical Landmarks. American Chemical Society. เก็บ (PDF)จากแหล่งเดิมเมื่อ April 18, 2016. สืบค้นเมื่อ June 12, 2017.
- ↑ Bartlett, Neil (1962). "Xenon hexafluoroplatinate(V) Xe+[PtF6]−". Proceedings of the Chemical Society. 1962 (6): 197–236. doi:10.1039/PS9620000197.
- ↑ Bartlett, Neil; Lohmann, D. H. (1962). "Dioxygenyl hexafluoroplatinate(V), O+
2[PtF6]−". Proceedings of the Chemical Society. 1962 (3): 97–132. doi:10.1039/PS9620000097.
- ↑ Clugston, Michael; Flemming, Rosalind (2000). Advanced Chemistry. Oxford University Press. p. 355. ISBN 978-0199146338.