![]() เธเนเธณเนเธเธทเธญเธเธเธตเนเธญเธธเธเธซเธ เธนเธกเธด 99.3 ยฐC (210.8 ยฐF) เธเธตเนเธเธงเธฒเธกเธชเธนเธ 215 เนเธกเธเธฃ (705 เธเธธเธ)
เธเนเธณเนเธเธทเธญเธเธเธตเนเธญเธธเธเธซเธ เธนเธกเธด 99.3 ยฐC (210.8 ยฐF) เธเธตเนเธเธงเธฒเธกเธชเธนเธ 215 เนเธกเธเธฃ (705 เธเธธเธ)
เธเธธเธเนเธเธทเธญเธเธเธญเธเธชเธฒเธฃเนเธเนเธเธญเธธเธเธซเธ เธนเธกเธดเธเธตเนเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธงเนเธเนเธฒเธเธฑเธเธเธงเธฒเธกเธเธฑเธเนเธเธขเธฃเธญเธเธเธญเธเธเธญเธเนเธซเธฅเธง เนเธฅเธฐเธเธญเธเนเธซเธฅเธงเธเธฐเนเธเธฅเธตเนเธขเธเธชเธเธฒเธเธฐเนเธเนเธเนเธญ
เธเธธเธเนเธเธทเธญเธเธเธญเธเธเธญเธเนเธซเธฅเธงเธเธฐเนเธเธฅเธตเนเธขเธเนเธเธฅเธเนเธเธเธฒเธกเธเธงเธฒเธกเธเธฑเธเนเธงเธเธฅเนเธญเธกเธเธตเนเนเธเธเธเนเธฒเธเธเธฑเธ เธเธญเธเนเธซเธฅเธงเนเธเธชเธธเธเธเธฒเธเธฒเธจเธเธฒเธเธชเนเธงเธ เนเธเนเธ เธ เธฒเธขเนเธเนเธเธงเธฒเธกเธเธฑเธเธเธตเนเธเนเธณเธเธงเนเธฒเธเธฐเธกเธตเธเธธเธเนเธเธทเธญเธเธเนเธณเธเธงเนเธฒเธเธญเธเธเธตเนเธเธญเธเนเธซเธฅเธงเธเธฑเนเธเธญเธขเธนเนเธเธตเนเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจ เนเธเธทเนเธญเธเธเธฒเธเนเธซเธเธธเธเธตเน เธเนเธณเธเธฐเนเธเธทเธญเธเธเธตเน 100ยฐC (เธซเธฃเธทเธญเนเธกเนเธเธขเธณเธเธฒเธเธงเธดเธเธขเธฒเธจเธฒเธชเธเธฃเน: 99.97ยฐC) เธ เธฒเธขเนเธเนเธเธงเธฒเธกเธเธฑเธเธกเธฒเธเธฃเธเธฒเธเธเธตเนเธฃเธฐเธเธฑเธเธเนเธณเธเธฐเนเธฅ เนเธเนเธเธฐเนเธเธทเธญเธเธเธตเน 93.4ยฐC เธเธตเนเธเธงเธฒเธกเธชเธนเธ 1905 เนเธกเธเธฃ
เธเธธเธเนเธเธทเธญเธเธเธเธเธด (เธซเธฃเธทเธญเธเธตเนเนเธฃเธตเธขเธเธงเนเธฒเธเธธเธเนเธเธทเธญเธเธเธตเนเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจ) เธเธญเธเธเธญเธเนเธซเธฅเธงเธเธทเธญเธเธฃเธเธตเธเธดเนเธจเธฉเธเธตเนเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธงเนเธเนเธฒเธเธฑเธเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจเธเธตเนเธเธณเธซเธเธเนเธงเนเธเธตเนเธฃเธฐเธเธฑเธเธเนเธณเธเธฐเนเธฅ เธเธถเนเธเธเธทเธญ 1 เธเธฃเธฃเธขเธฒเธเธฒเธจ เธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเธเธฑเนเธ เธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธงเธเธฐเนเธเธตเธขเธเธเธญเธเธตเนเธเธฐเนเธญเธฒเธเธเธฐเนเธฃเธเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจเนเธฅเธฐเธเธณเนเธซเนเนเธเธดเธเธเธญเธเนเธญเธ เธฒเธขเนเธเธเธญเธเนเธซเธฅเธง
เธเธงเธฒเธกเธฃเนเธญเธเธเธญเธเธเธฒเธฃเธฃเธฐเนเธซเธขเนเธเนเธเธเธฅเธฑเธเธเธฒเธเธเธตเนเธเนเธญเธเนเธเนเนเธเธเธฒเธฃเนเธเธฅเธตเนเธขเธเธเธฃเธดเธกเธฒเธเธชเธฒเธฃเธซเธเธถเนเธ (เนเธเนเธ เนเธกเธฅ เธเธดเนเธฅเธเธฃเธฑเธก เธเธญเธเธเน เธฏเธฅเธฏ) เธเธฒเธเธชเธเธฒเธเธฐเธเธญเธเนเธซเธฅเธงเนเธเนเธเธชเธเธฒเธเธฐเนเธเนเธชเธ เธฒเธขเนเธเนเธเธงเธฒเธกเธเธฑเธเธเธตเนเธเธณเธซเธเธ (เธกเธฑเธเธเธฐเนเธเนเธเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจ)
เธเธญเธเนเธซเธฅเธงเธญเธฒเธเนเธเธฅเธตเนเธขเธเธชเธเธฒเธเธฐเนเธเนเธเนเธญเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเธเนเธณเธเธงเนเธฒเธเธธเธเนเธเธทเธญเธเธเนเธฒเธเธเธฃเธฐเธเธงเธเธเธฒเธฃเธฃเธฐเนเธซเธข เธเธฒเธฃเธฃเธฐเนเธซเธขเนเธเนเธเธเธฃเธฒเธเธเธเธฒเธฃเธเนเธเธตเนเนเธเธดเธเธเธถเนเธเธเธตเนเธเธดเธงเธเธญเธเธเธญเธเนเธซเธฅเธง เธเธถเนเธเนเธกเนเธฅเธเธธเธฅเธเธตเนเธญเธขเธนเนเนเธเธฅเนเธเธญเธเธเธญเธเนเธซเธฅเธงเนเธกเนเธกเธตเธเธงเธฒเธกเธเธฑเธเธเธญเธเนเธซเธฅเธงเนเธเธตเธขเธเธเธญเธเธตเนเธเธฐเธเธฑเธเนเธเนเธเนเธงเน เธเธณเนเธซเนเธชเธฒเธกเธฒเธฃเธเธซเธฅเธธเธเธญเธญเธเนเธเนเธเธชเธ เธฒเธเนเธงเธเธฅเนเธญเธกเธฃเธญเธเธเนเธฒเธเนเธเธฃเธนเธเนเธเธเธเธญเธเนเธญ เนเธเธเธฒเธเธเธฃเธเธเธฑเธเธเนเธฒเธก เธเธฒเธฃเนเธเธทเธญเธเนเธเนเธเธเธฃเธฐเธเธงเธเธเธฒเธฃเธเธตเนเนเธกเนเธฅเธเธธเธฅเนเธเธเธญเธเนเธซเธฅเธงเธชเธฒเธกเธฒเธฃเธเธซเธฅเธธเธเธญเธญเธเนเธเน เธเธณเนเธซเนเนเธเธดเธเธเธญเธเนเธญเธ เธฒเธขเนเธเธเธญเธเนเธซเธฅเธง[1][2][3][4][5][6]
เธญเธธเธเธซเธ เธนเธกเธดเนเธฅเธฐเธเธงเธฒเธกเธเธฑเธเธญเธดเนเธกเธเธฑเธง
เธเธฒเธฃเธชเธฒเธเธดเธเธเธฒเธฃเนเธเธทเธญเธเธเธญเธเธเนเธณเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเธเนเธณเธฅเธเนเธกเธทเนเธญเธญเธขเธนเนเนเธเธเธงเธฒเธกเธเธฑเธเธเนเธณ เนเธเธขเนเธเนเธเธฑเนเธกเธชเธธเธเธเธฒเธเธฒเธจ
เธเธญเธเนเธซเธฅเธงเธญเธดเนเธกเธเธฑเธงเธซเธกเธฒเธขเธเธถเธเธเธญเธเนเธซเธฅเธงเธเธตเนเธกเธตเธเธฅเธฑเธเธเธฒเธเธเธงเธฒเธกเธฃเนเธญเธเธกเธฒเธเธเธตเนเธชเธธเธเนเธเนเธฒเธเธตเนเธเธฐเธกเธตเนเธเนเนเธเธขเนเธกเนเนเธเธดเธเธเธฒเธฃเนเธเธทเธญเธ (เธซเธฃเธทเธญเนเธเธเธฒเธเธเธฃเธเธเธฑเธเธเนเธฒเธก เนเธญเธญเธดเนเธกเธเธฑเธงเธซเธกเธฒเธขเธเธถเธเนเธญเธเธตเนเธกเธตเธเธฅเธฑเธเธเธฒเธเธเธงเธฒเธกเธฃเนเธญเธเธเนเธญเธขเธเธตเนเธชเธธเธเนเธเนเธฒเธเธตเนเธเธฐเธกเธตเนเธเนเนเธเธขเนเธกเนเนเธเธดเธเธเธฒเธฃเธเธงเธเนเธเนเธ)
เธญเธธเธเธซเธ เธนเธกเธดเธญเธดเนเธกเธเธฑเธง เธซเธกเธฒเธขเธเธถเธ เธเธธเธเนเธเธทเธญเธ เธญเธธเธเธซเธ เธนเธกเธดเธญเธดเนเธกเธเธฑเธงเธเธทเธญเธญเธธเธเธซเธ เธนเธกเธดเธชเธณเธซเธฃเธฑเธเธเธงเธฒเธกเธเธฑเธเธญเธดเนเธกเธเธฑเธงเธเธตเนเธชเธญเธเธเธฅเนเธญเธเธเธฑเธ เธเธถเนเธเธเธญเธเนเธซเธฅเธงเธเธฐเนเธเธทเธญเธเธเธฅเธฒเธขเนเธเนเธเนเธญเธชเธฒเธกเธฒเธฃเธเธเธฅเนเธฒเธงเนเธเนเธงเนเธฒเธเธญเธเนเธซเธฅเธงเธเธฑเนเธเธญเธดเนเธกเธเธฑเธงเธเนเธงเธขเธเธฅเธฑเธเธเธฒเธเธเธงเธฒเธกเธฃเนเธญเธ เธเธฒเธฃเนเธเธดเนเธกเธเธฅเธฑเธเธเธฒเธเธเธงเธฒเธกเธฃเนเธญเธเนเธ เน เธเธฐเธชเนเธเธเธฅเนเธซเนเนเธเธดเธเธเธฒเธฃเนเธเธฅเธตเนเธขเธเนเธเธฅเธเธชเธเธฒเธเธฐ
เธซเธฒเธเธเธงเธฒเธกเธเธฑเธเนเธเธฃเธฐเธเธเธเธเธเธตเน (เธเธฃเธฐเธเธงเธเธเธฒเธฃเธญเธตเนเธเธเธฒเธฃเธดเธ) เนเธญเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเธญเธดเนเธกเธเธฑเธงเธเธฐเนเธฃเธดเนเธกเธเธงเธเนเธเนเธเธเธฅเธฒเธขเนเธเนเธเธเธญเธเนเธซเธฅเธงเนเธกเธทเนเธญเธกเธตเธเธฒเธฃเธเธณเธเธฑเธเธเธฅเธฑเธเธเธฒเธเธเธงเธฒเธกเธฃเนเธญเธ (เธเธงเธฒเธกเธฃเนเธญเธ) เนเธเธเธณเธเธญเธเนเธเธตเธขเธงเธเธฑเธ เธเธญเธเนเธซเธฅเธงเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเนเธฅเธฐเธเธงเธฒเธกเธเธฑเธเธญเธดเนเธกเธเธฑเธงเธเธฐเนเธเธทเธญเธเธเธฅเธฒเธขเนเธเนเธเนเธญเนเธกเธทเนเธญเธกเธตเธเธฒเธฃเนเธเธดเนเธกเธเธฅเธฑเธเธเธฒเธเธเธงเธฒเธกเธฃเนเธญเธเนเธเธดเนเธกเนเธเธดเธก
เธเธธเธเนเธเธทเธญเธเธชเธญเธเธเธฅเนเธญเธเธเธฑเธเธญเธธเธเธซเธ เธนเธกเธดเธเธตเนเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธงเนเธเนเธฒเธเธฑเธเธเธงเธฒเธกเธเธฑเธเนเธเธขเธฃเธญเธ เธเธฑเธเธเธฑเนเธเธเธธเธเนเธเธทเธญเธเธเธถเธเธเธถเนเธเธญเธขเธนเนเธเธฑเธเธเธงเธฒเธกเธเธฑเธ เธเธธเธเนเธเธทเธญเธเธญเธฒเธเธเธนเธเนเธเธขเนเธเธฃเนเนเธเธขเธญเนเธฒเธเธญเธดเธเธเธฑเธNIST, USA เธเธงเธฒเธกเธเธฑเธเธกเธฒเธเธฃเธเธฒเธเธเธตเน 101.325 เธเธดเนเธฅเธเธฒเธชเธเธฒเธฅ (เธซเธฃเธทเธญ 1 เธเธฃเธฃเธขเธฒเธเธฒเธจ) เธซเธฃเธทเธญเธเธงเธฒเธกเธเธฑเธเธกเธฒเธเธฃเธเธฒเธเธเธญเธเธชเธซเธ เธฒเธเนเธเธกเธตเธเธฃเธดเธชเธธเธเธเธดเนเนเธฅเธฐเนเธเธกเธตเธเธฃเธฐเธขเธธเธเธเนเธฃเธฐเธซเธงเนเธฒเธเธเธฃเธฐเนเธเธจ (IUPAC)เธเธตเน 100.000 เธเธดเนเธฅเธเธฒเธชเธเธฒเธฅ เธเธตเนเธฃเธฐเธเธฑเธเธเธงเธฒเธกเธชเธนเธเธเธตเนเธชเธนเธเธเธถเนเธ เธเธถเนเธเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจเธเนเธณเธเธงเนเธฒเธกเธฒเธ เธเธธเธเนเธเธทเธญเธเธเธฐเธเนเธณเธฅเธเธเนเธงเธขเนเธเนเธเธเธฑเธ เธเธธเธเนเธเธทเธญเธเธเธฐเนเธเธดเนเธกเธเธถเนเธเนเธกเธทเนเธญเธเธงเธฒเธกเธเธฑเธเนเธเธดเนเธกเธเธถเนเธเธเธเธเธถเธเธเธธเธเธงเธดเธเธคเธ เธเธถเนเธเธเธธเธเธชเธกเธเธฑเธเธดเธเธญเธเนเธญเนเธฅเธฐเธเธญเธเนเธซเธฅเธงเธเธฐเนเธซเธกเธทเธญเธเธเธฑเธ เธเธธเธเนเธเธทเธญเธเนเธกเนเธชเธฒเธกเธฒเธฃเธเนเธเธดเนเธกเธเธถเนเธเนเธเธดเธเธเธงเนเธฒเธเธธเธเธงเธดเธเธคเธเนเธเนเนเธเนเธเธเธฑเธ เนเธเธเธณเธเธญเธเนเธเธตเธขเธงเธเธฑเธ เธเธธเธเนเธเธทเธญเธเธเธฐเธฅเธเธฅเธเนเธกเธทเนเธญเธเธงเธฒเธกเธเธฑเธเธฅเธเธฅเธเธเธเธเธถเธเธเธธเธเธชเธฒเธกเธชเธเธฒเธเธฐ เธเธธเธเนเธเธทเธญเธเนเธกเนเธชเธฒเธกเธฒเธฃเธเธฅเธเธฅเธเธเนเธณเธเธงเนเธฒเธเธธเธเธชเธฒเธกเธชเธเธฒเธเธฐเนเธเน
เธซเธฒเธเธเธฃเธฒเธเธเธงเธฒเธกเธฃเนเธญเธเธเธญเธเธเธฒเธฃเธฃเธฐเนเธซเธขเนเธฅเธฐเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธงเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเธซเธเธถเนเธ เธเธธเธเนเธเธทเธญเธเธชเธฒเธกเธฒเธฃเธเธเธณเธเธงเธเนเธเนเนเธเธขเนเธเนเธชเธกเธเธฒเธฃเธเธฅเธญเนเธเธตเธขเธชโเนเธเธฅเนเธเธฃเธขเนเธฃเธญเธ เธเธฑเธเธเธตเน:

เนเธเธขเธเธตเน:
 เธเธทเธญเธเธธเธเนเธเธทเธญเธเธเธตเนเธเธงเธฒเธกเธเธฑเธเธเธตเนเธชเธเนเธ,
เธเธทเธญเธเธธเธเนเธเธทเธญเธเธเธตเนเธเธงเธฒเธกเธเธฑเธเธเธตเนเธชเธเนเธ, เธเธทเธญเธเนเธฒเธเธเธเธตเนเนเธเนเธชเธญเธธเธเธกเธเธเธด,
เธเธทเธญเธเนเธฒเธเธเธเธตเนเนเธเนเธชเธญเธธเธเธกเธเธเธด, เธเธทเธญเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธง,
เธเธทเธญเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธง, เธเธทเธญเธเธงเธฒเธกเธเธฑเธเธเธฒเธเธเนเธฒเธเธตเนเธเธฃเธฒเธเธเนเธฒ
เธเธทเธญเธเธงเธฒเธกเธเธฑเธเธเธฒเธเธเนเธฒเธเธตเนเธเธฃเธฒเธเธเนเธฒ  เธเธตเนเธชเธญเธเธเธฅเนเธญเธเธเธฑเธ (เธเธเธเธดเธเนเธญเธกเธนเธฅเธเธตเนเธเธฐเธกเธตเธญเธขเธนเนเธเธตเน 1 atm เธซเธฃเธทเธญ 100 kPa),
เธเธตเนเธชเธญเธเธเธฅเนเธญเธเธเธฑเธ (เธเธเธเธดเธเนเธญเธกเธนเธฅเธเธตเนเธเธฐเธกเธตเธญเธขเธนเนเธเธตเน 1 atm เธซเธฃเธทเธญ 100 kPa), เธเธทเธญเธเธงเธฒเธกเธฃเนเธญเธเธเธญเธเธเธฒเธฃเธฃเธฐเนเธซเธขเธเธญเธเธเธญเธเนเธซเธฅเธง,
เธเธทเธญเธเธงเธฒเธกเธฃเนเธญเธเธเธญเธเธเธฒเธฃเธฃเธฐเนเธซเธขเธเธญเธเธเธญเธเนเธซเธฅเธง, เธเธทเธญเธญเธธเธเธซเธ เธนเธกเธดเนเธเธทเธญเธ,
เธเธทเธญเธญเธธเธเธซเธ เธนเธกเธดเนเธเธทเธญเธ, เธเธทเธญเธฅเธญเธเธฒเธฃเธดเธเธถเธกเธเธฃเธฃเธกเธเธฒเธเธด.
เธเธทเธญเธฅเธญเธเธฒเธฃเธดเธเธถเธกเธเธฃเธฃเธกเธเธฒเธเธด.
เธเธงเธฒเธกเธเธฑเธเธญเธดเนเธกเธเธฑเธง เธเธทเธญเธเธงเธฒเธกเธเธฑเธเธชเธณเธซเธฃเธฑเธเธญเธธเธเธซเธ เธนเธกเธดเธญเธดเนเธกเธเธฑเธงเธเธตเนเธชเธญเธเธเธฅเนเธญเธเธเธฑเธ เธเธถเนเธเธเธญเธเนเธซเธฅเธงเธเธฐเนเธเธทเธญเธเธเธฅเธฒเธขเนเธเนเธเนเธญ เธเธงเธฒเธกเธเธฑเธเธญเธดเนเธกเธเธฑเธงเนเธฅเธฐเธญเธธเธเธซเธ เธนเธกเธดเธญเธดเนเธกเธเธฑเธงเธกเธตเธเธงเธฒเธกเธชเธฑเธกเธเธฑเธเธเนเนเธเธขเธเธฃเธ: เนเธกเธทเนเธญเธเธงเธฒเธกเธเธฑเธเธญเธดเนเธกเธเธฑเธงเนเธเธดเนเธกเธเธถเนเธ เธญเธธเธเธซเธ เธนเธกเธดเธญเธดเนเธกเธเธฑเธงเธเนเธเธฐเนเธเธดเนเธกเธเธถเนเธเธเนเธงเธข
เธซเธฒเธเธญเธธเธเธซเธ เธนเธกเธดเนเธเธฃเธฐเธเธเธเธเธเธตเน (เธฃเธฐเธเธเธญเธธเธเธซเธ เธนเธกเธดเธเธเธเธตเน) เนเธญเธเธตเนเธเธงเธฒเธกเธเธฑเธเนเธฅเธฐเธญเธธเธเธซเธ เธนเธกเธดเธญเธดเนเธกเธเธฑเธงเธเธฐเนเธฃเธดเนเธกเธเธงเธเนเธเนเธเธเธฅเธฒเธขเนเธเนเธเธเธญเธเนเธซเธฅเธงเนเธกเธทเนเธญเธเธงเธฒเธกเธเธฑเธเธฃเธฐเธเธเนเธเธดเนเธกเธเธถเนเธ เนเธเธเธณเธเธญเธเนเธเธตเธขเธงเธเธฑเธ เธเธญเธเนเธซเธฅเธงเธเธตเนเธเธงเธฒเธกเธเธฑเธเนเธฅเธฐเธญเธธเธเธซเธ เธนเธกเธดเธญเธดเนเธกเธเธฑเธงเธเธฐเธกเธตเนเธเธงเนเธเนเธกเธเธตเนเธเธฐเธฃเธฐเนเธซเธขเธญเธขเนเธฒเธเธฃเธงเธเนเธฃเนเธงเธเธฅเธฒเธขเนเธเนเธเนเธญเนเธกเธทเนเธญเธเธงเธฒเธกเธเธฑเธเธฃเธฐเธเธเธฅเธเธฅเธ
เธกเธตเธชเธญเธเนเธเธงเธเธฒเธเนเธเธตเนเธขเธงเธเธฑเธ เธเธธเธเนเธเธทเธญเธเธกเธฒเธเธฃเธเธฒเธเธเธญเธเธเนเธณ: เธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธทเธญ 99.97 เธญเธเธจเธฒเนเธเธฅเนเธเธตเธขเธช (211.9 เธญเธเธจเธฒเธเธฒเนเธฃเธเนเธฎเธเน) เธเธตเนเธเธงเธฒเธกเธเธฑเธ 1 atm (เธเธทเธญ 101.325 kPa) IUPACเนเธเธฐเธเธณ เธเธธเธเนเธเธทเธญเธเธกเธฒเธเธฃเธเธฒเธเธเธญเธเธเนเธณเธเธตเนเธเธงเธฒเธกเธเธฑเธเธกเธฒเธเธฃเธเธฒเธ 100 kPa (1 เธเธฒเธฃเน)[7] เธเธทเธญ 99.61 เธญเธเธจเธฒเนเธเธฅเนเธเธตเธขเธช (211.3 เธญเธเธจเธฒเธเธฒเนเธฃเธเนเธฎเธเน).[6][8] เนเธเธทเนเธญเนเธเธฃเธตเธขเธเนเธเธตเธขเธ เธเธตเนเธขเธญเธ เธ เธนเนเธเธฒเนเธญเนเธงเธญเนเธฃเธชเธเน, เธเธตเนเธเธงเธฒเธกเธชเธนเธ 8,848 m (29,029 ft) เธเธงเธฒเธกเธเธฑเธเธญเธขเธนเนเธเธตเนเธเธฃเธฐเธกเธฒเธ 34 kPa (255 Torr)[9] เนเธฅเธฐเธเธธเธเนเธเธทเธญเธเธเธญเธเธเนเธณเธเธทเธญ 71 เธญเธเธจเธฒเนเธเธฅเนเธเธตเธขเธช (160 เธญเธเธจเธฒเธเธฒเนเธฃเธเนเธฎเธเน)เธกเธฒเธเธฃเธฒเธชเนเธงเธเธญเธธเธเธซเธ เธนเธกเธดเนเธเธฅเนเธเธตเธขเธชเธเธนเธเธเธณเธซเธเธเธเธเธเธถเธเธเธต 1954 เนเธเธขเธชเธญเธเธเธธเธ: 0 ยฐC เธเธนเธเธเธณเธซเธเธเนเธเธขเธเธธเธเนเธขเธทเธญเธเนเธเนเธเธเธญเธเธเนเธณ เนเธฅเธฐ 100 ยฐC เธเธนเธเธเธณเธซเธเธเนเธเธขเธเธธเธเนเธเธทเธญเธเธเธญเธเธเนเธณเธเธตเนเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจเธกเธฒเธเธฃเธเธฒเธ
เธเธงเธฒเธกเธชเธฑเธกเธเธฑเธเธเนเธฃเธฐเธซเธงเนเธฒเธเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธฑเธเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธง
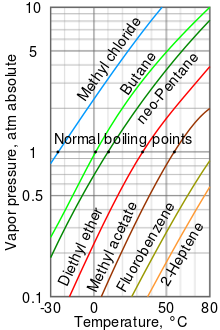 เธเธฃเธฒเธเธเธงเธฒเธกเธเธฑเธเนเธญเนเธเธเธฅเนเธญเธ-เธฅเธดเธ (log-lin) เธชเธณเธซเธฃเธฑเธเธเธญเธเนเธซเธฅเธงเธซเธฅเธฒเธขเธเธเธดเธ
เธเธฃเธฒเธเธเธงเธฒเธกเธเธฑเธเนเธญเนเธเธเธฅเนเธญเธ-เธฅเธดเธ (log-lin) เธชเธณเธซเธฃเธฑเธเธเธญเธเนเธซเธฅเธงเธซเธฅเธฒเธขเธเธเธดเธ
เธขเธดเนเธเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเธญเธเนเธซเธฅเธงเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเนเธ เน เธชเธนเธเธเธถเนเธเนเธเนเธฒเนเธ เธเธธเธเนเธเธทเธญเธเธเธเธเธด (เธเธทเธญ เธเธธเธเนเธเธทเธญเธเธเธตเนเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจ) เธเธญเธเธเธญเธเนเธซเธฅเธงเธเธฐเธขเธดเนเธเธเนเธณเธฅเธ
เธเธฃเธฒเธเธเธงเธฒเธกเธเธฑเธเนเธญเธเธตเนเธญเธขเธนเนเธเธฒเธเธเธงเธฒเธกเธตเธเธฃเธฒเธเนเธชเธเธเธเธงเธฒเธกเธชเธฑเธกเธเธฑเธเธเนเธฃเธฐเธซเธงเนเธฒเธเธเธงเธฒเธกเธเธฑเธเนเธญเธเธฑเธเธญเธธเธเธซเธ เธนเธกเธดเธชเธณเธซเธฃเธฑเธเธเธญเธเนเธซเธฅเธงเธซเธฅเธฒเธเธซเธฅเธฒเธขเธเธเธดเธ[10] เธเธฒเธเธเธฃเธฒเธเธเธฐเนเธซเนเธเนเธเนเธงเนเธฒเธเธญเธเนเธซเธฅเธงเธเธตเนเธกเธตเธเธงเธฒเธกเธเธฑเธเนเธญเธชเธนเธเธเธตเนเธชเธธเธเธเธฐเธกเธตเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเนเธณเธเธตเนเธชเธธเธ
เธเธฑเธงเธญเธขเนเธฒเธเนเธเนเธ เธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเนเธ เน เธเนเธเธฒเธก เนเธกเธเธดเธฅเธเธฅเธญเนเธฃเธเนเธกเธตเธเธงเธฒเธกเธเธฑเธเนเธญเธชเธนเธเธเธตเนเธชเธธเธเนเธเธเธฃเธฃเธเธฒเธเธญเธเนเธซเธฅเธงเนเธเธเธฃเธฒเธเธเธตเน เนเธฅเธฐเธกเธตเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธตเนเธเนเธณเธเธตเนเธชเธธเธ (-24.2 ยฐC) เธเธถเนเธเนเธเนเธเธเธธเธเธเธตเนเธเธฃเธฒเธเธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเนเธกเธเธดเธฅเธเธฅเธญเนเธฃเธเน (เนเธชเนเธเธชเธตเธเนเธณเนเธเธดเธ) เธเธฑเธเธเธฑเธเนเธชเนเธเธเธงเธฒเธกเธเธฑเธเนเธเธงเธเธญเธเธเธตเนเธซเธเธถเนเธเธเธฃเธฃเธขเธฒเธเธฒเธจ (atm) เธเธญเธเธเธงเธฒเธกเธเธฑเธเนเธญเธชเธฑเธกเธเธนเธฃเธเน
เธเธธเธเธงเธดเธเธคเธเธเธญเธเธเธญเธเนเธซเธฅเธงเธเธทเธญเธญเธธเธเธซเธ เธนเธกเธด (เนเธฅเธฐเธเธงเธฒเธกเธเธฑเธ) เธชเธนเธเธชเธธเธเธเธตเนเธเธญเธเนเธซเธฅเธงเธเธฐเนเธเธทเธญเธเนเธเน
เธเธนเนเธเธดเนเธกเนเธเธดเธกเธเธตเน เธเธงเธฒเธกเธเธฑเธเนเธญเธเธญเธเธเนเธณ
เธเธธเธเนเธเธทเธญเธเธเธญเธเธเธฒเธเธธเนเธเธกเธต
เธเธฒเธเธธเธเธตเนเธกเธตเธเธธเธเนเธเธทเธญเธเธเนเธณเธเธตเนเธชเธธเธเธเธทเธญ เธฎเธตเนเธฅเธตเธขเธก เธเธเธฐเธเธตเนเธเธธเธเนเธเธทเธญเธเธเธญเธ เนเธฃเนเธเธตเธขเธก เนเธฅเธฐ เธเธฑเธเธชเนเธเธ เนเธเธดเธ 5000 K เธเธตเน เธเธงเธฒเธกเธเธฑเธเธกเธฒเธเธฃเธเธฒเธ; เนเธเธทเนเธญเธเธเธฒเธเธเธฒเธฃเธงเธฑเธเธญเธธเธเธซเธ เธนเธกเธดเธเธตเนเธชเธนเธเธกเธฒเธเธญเธฒเธเธกเธตเธเธงเธฒเธกเธเธฅเธฒเธเนเธเธฅเธทเนเธญเธ, เธเนเธญเธกเธนเธฅเนเธเธตเนเธขเธงเธเธฑเธเธเธธเธเนเธเธทเธญเธเธเธตเนเธชเธนเธเธเธญเธเธเธฑเนเธเธชเธญเธเธเธฒเธเธธเธเธถเธเธกเธตเธเธฒเธฃเธเธฅเนเธฒเธงเธเธถเธเนเธเธงเธฃเธฃเธเธเธฃเธฃเธกเธงเนเธฒเนเธเนเธเธเธธเธเนเธเธทเธญเธเธเธตเนเธชเธนเธเธเธงเนเธฒเธเธตเน[11]
เธเธธเธเนเธเธทเธญเธเนเธเธเธฒเธเธฐเธเธธเธเธชเธกเธเธฑเธเธดเธญเนเธฒเธเธญเธดเธเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฃเธดเธชเธธเธเธเธดเน
เธเธฒเธเธเธฃเธฒเธเธเนเธฒเธเธเธเธเธญเธเธฅเธญเธเธฒเธฃเธดเธเธถเธกเธเธญเธเธเธงเธฒเธกเธเธฑเธเนเธญเนเธเธตเธขเธเธเธฑเธเธญเธธเธเธซเธ เธนเธกเธดเธชเธณเธซเธฃเธฑเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเนเธเธกเธตเธเธฃเธดเธชเธธเธเธเธดเนเธเธตเนเธเธณเธซเธเธ เธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเนเธเธชเธฒเธกเธฒเธฃเธเนเธเนเนเธเนเธเธเธฑเธงเธเนเธเธเธตเนเธเธถเธเธเธงเธฒเธกเธฃเธฐเนเธซเธขเนเธเธขเธฃเธงเธกเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเนเธ เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฃเธดเธชเธธเธเธเธดเนเธเธตเนเธเธณเธซเธเธเธเธฐเธกเธตเนเธเธตเธขเธเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธซเธเธถเนเธเธเธธเธเนเธเนเธฒเธเธฑเนเธ (เธซเธฒเธเธกเธต) เนเธฅเธฐเธเธธเธเนเธเธทเธญเธเธเธเธเธดเนเธฅเธฐเธเธธเธเธซเธฅเธญเธกเนเธซเธฅเธงเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธชเธฒเธกเธฒเธฃเธเนเธเนเนเธเนเธเธเธธเธเธชเธกเธเธฑเธเธดเธชเธกเธเธฑเธเธดเธเธฒเธเธเธฒเธขเธ เธฒเธเธฅเธฑเธเธฉเธเธฐเนเธเธเธฒเธฐเธชเธณเธซเธฃเธฑเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเนเธ เน เธเธถเนเธเธเธฐเธกเธตเธเธฒเธฃเธฃเธฐเธเธธเนเธงเนเนเธเธซเธเธฑเธเธชเธทเธญเธญเนเธฒเธเธญเธดเธ เธขเธดเนเธเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธชเธนเธเนเธเนเธฒเนเธฃ เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเนเธเธเนเธเธฐเธกเธตเธเธงเธฒเธกเธฃเธฐเนเธซเธขเธเนเธญเธขเธฅเธเนเธเนเธฒเธเธฑเนเธ เนเธฅเธฐเนเธเธเธฒเธเธเธฅเธฑเธเธเธฑเธ เธขเธดเนเธเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเนเธณเธฅเธ เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเนเธเธเนเธเธฐเธกเธตเธเธงเธฒเธกเธฃเธฐเนเธซเธขเธกเธฒเธเธเธถเนเธ เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฒเธเธเธเธดเธเธเธฐเธชเธฅเธฒเธขเธเธฑเธงเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเธชเธนเธเธเนเธญเธเธเธตเนเธเธฐเธเธถเธเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธซเธฃเธทเธญเธเธฒเธเธเธฃเธฑเนเธเนเธกเนเธเธฃเธฐเธเธฑเนเธเธเธธเธเธซเธฅเธญเธกเนเธซเธฅเธง เธชเธณเธซเธฃเธฑเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธตเนเนเธชเธเธตเธขเธฃ เธเธธเธเนเธเธทเธญเธเธญเธขเธนเนเนเธเธเนเธงเธเธเธฑเนเธเนเธเนเธเธธเธเธชเธฒเธกเธชเธเธฒเธเธฐเนเธเธเธเธเธถเธเธเธธเธเธงเธดเธเธคเธ เธเธถเนเธเธญเธขเธนเนเธเธฑเธเธเธงเธฒเธกเธเธฑเธเธ เธฒเธขเธเธญเธ เธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฐเธชเธนเธเธเธงเนเธฒเธเธธเธเธซเธฅเธญเธกเนเธซเธฅเธง (เธเนเธฒเธกเธต) เนเธกเธทเนเธญเธญเธขเธนเนเนเธซเธเธทเธญเธเธธเธเธชเธฒเธกเธชเธเธฒเธเธฐ เธซเธฅเธฑเธเธเธฒเธเธเธธเธเธงเธดเธเธคเธเนเธฅเนเธง เธชเธเธฒเธเธฐเธเธญเธเนเธซเธฅเธงเนเธฅเธฐเนเธญเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฐเธฃเธงเธกเนเธเนเธฒเธเนเธงเธขเธเธฑเธเนเธเนเธเธซเธเธถเนเธเธชเธเธฒเธเธฐ เธเธถเนเธเธญเธฒเธเนเธฃเธตเธขเธเธงเนเธฒเนเธเนเธชเธฃเนเธญเธเธขเธงเธเธขเธดเนเธ เนเธกเธทเนเธญเธญเธธเธเธซเธ เธนเธกเธดเนเธ เน เธเนเธเธฒเธก เธเนเธฒเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเนเธณเธเธงเนเธฒ เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเนเธเนเธเธขเธเธฑเนเธงเนเธเธเธฐเธญเธขเธนเนเนเธเธฃเธนเธเธเธญเธเนเธเนเธชเธเธตเนเธเธงเธฒเธกเธเธฑเธเธ เธฒเธขเธเธญเธเธเธฃเธฃเธขเธฒเธเธฒเธจ เธเนเธฒเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธชเธนเธเธเธงเนเธฒ เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเนเธเธชเธฒเธกเธฒเธฃเธเธญเธขเธนเนเนเธเธฃเธนเธเธเธญเธเนเธซเธฅเธงเธซเธฃเธทเธญเธเธญเธเนเธเนเธเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเนเธ เน เธเนเธเธฒเธกเธเธตเนเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจเธ เธฒเธขเธเธญเธ เนเธฅเธฐเธเธฐเธญเธขเธนเนเนเธเธชเธกเธเธธเธฅเธเธฑเธเนเธญ (เธซเธฒเธเธกเธตเธเธงเธฒเธกเธฃเธฐเนเธซเธข) เธซเธฒเธเนเธญเธเธนเธเนเธเนเธเธฃเธฑเธเธฉเธฒเนเธงเน เธซเธฒเธเนเธญเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเนเธกเนเนเธเนเธเธนเธเนเธเนเธเธฃเธฑเธเธฉเธฒเนเธงเน เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฒเธเธเธเธดเธเธเธตเนเธฃเธฐเนเธซเธขเนเธเนเนเธเธเธตเนเธชเธธเธเธเธฐเธฃเธฐเนเธซเธขเธซเธฒเธขเนเธ เนเธกเนเธงเนเธฒเธเธฐเธกเธตเธเธธเธเนเธเธทเธญเธเธเธตเนเธชเธนเธเธเธถเนเธเธเนเธเธฒเธก
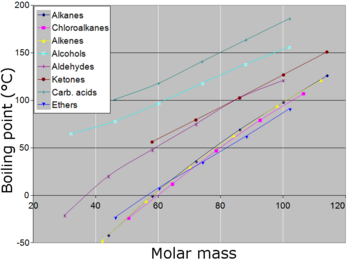 เธเธฃเธฒเธเนเธชเธเธเธเธธเธเนเธเธทเธญเธเธเธญเธเนเธญเธฅเนเธเธ, เนเธญเธฅเธเธตเธ, เธญเธตเนเธเธญเธฃเน, เธฎเธฒเนเธฅเธเธตเนเธเนเธญเธฅเนเธเธ, เนเธญเธฅเธเธตเนเธฎเธเน, เธเธตเนเธเธ, เนเธญเธฅเธเธญเธฎเธญเธฅเน เนเธฅเธฐเธเธฃเธเธเธฒเธฃเนเธเธญเธเธเธดเธฅเธดเธ เนเธกเธทเนเธญเนเธเธตเธขเธเธเธฑเธเธกเธงเธฅเนเธกเธฅเธฒเธฃเน
เธเธฃเธฒเธเนเธชเธเธเธเธธเธเนเธเธทเธญเธเธเธญเธเนเธญเธฅเนเธเธ, เนเธญเธฅเธเธตเธ, เธญเธตเนเธเธญเธฃเน, เธฎเธฒเนเธฅเธเธตเนเธเนเธญเธฅเนเธเธ, เนเธญเธฅเธเธตเนเธฎเธเน, เธเธตเนเธเธ, เนเธญเธฅเธเธญเธฎเธญเธฅเน เนเธฅเธฐเธเธฃเธเธเธฒเธฃเนเธเธญเธเธเธดเธฅเธดเธ เนเธกเธทเนเธญเนเธเธตเธขเธเธเธฑเธเธกเธงเธฅเนเธกเธฅเธฒเธฃเน
เนเธเธขเธเธฑเนเธงเนเธ เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธตเนเธกเธตเธเธฑเธเธเธฐเนเธญเธญเธญเธเธดเธเธเธฐเธกเธตเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธตเนเธชเธนเธ เธซเธฒเธเนเธกเนเธชเธฅเธฒเธขเธเธฑเธงเธเนเธญเธเธเธตเนเธเธฐเธเธถเธเธญเธธเธเธซเธ เธนเธกเธดเธชเธนเธเธเธฑเธเธเธฅเนเธฒเธง เนเธฅเธซเธฐเธซเธฅเธฒเธขเธเธเธดเธเธกเธตเธเธธเธเนเธเธทเธญเธเธชเธนเธ เนเธเนเนเธกเนเนเธเนเธเธฑเนเธเธซเธกเธ เนเธเธขเธเธฑเนเธงเนเธเนเธฅเนเธงเนเธกเธทเนเธญเธเธฑเธเธเธฑเธขเธญเธทเนเธ เน เนเธเนเธฒเธเธฑเธ เนเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธตเนเธกเธตเธเธฑเธเธเธฐเนเธเธงเธฒเนเธฅเธเธเน เนเธกเธทเนเธญเธเธเธฒเธเธเธญเธเนเธกเนเธฅเธเธธเธฅ (เธซเธฃเธทเธญเธกเธงเธฅเนเธกเนเธฅเธเธธเธฅ) เนเธเธดเนเธกเธเธถเนเธ เธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธฐเนเธเธดเนเธกเธเธถเนเธ เนเธกเธทเนเธญเธเธเธฒเธเธเธญเธเนเธกเนเธฅเธเธธเธฅเนเธเธดเนเธกเธเธถเนเธเธเธเธเธฅเธฒเธขเนเธเนเธเธกเธฒเธเธฃเนเธกเนเธฅเธเธธเธฅ, เนเธเธฅเธตเนเธกเธญเธฃเน เธซเธฃเธทเธญเธกเธตเธเธเธฒเธเนเธซเธเนเธกเธฒเธ เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธกเธฑเธเธเธฐเธชเธฅเธฒเธขเธเธฑเธงเธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเธชเธนเธเธเนเธญเธเธเธตเนเธเธฐเธเธถเธเธเธธเธเนเธเธทเธญเธ เธญเธตเธเธเธฑเธเธเธฑเธขเธซเธเธถเนเธเธเธตเนเธชเนเธเธเธฅเธเนเธญเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธทเธญเธเธฑเนเธงเธเธญเธเนเธกเนเธฅเธเธธเธฅเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเนเธ เนเธกเธทเนเธญเธเธฑเนเธงเธเธญเธเนเธกเนเธฅเธเธธเธฅเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเนเธเธดเนเธกเธเธถเนเธ เธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเนเธเธฐเนเธเธดเนเธกเธเธถเนเธเนเธเนเธเธเธฑเธเนเธกเธทเนเธญเธเธฑเธเธเธฑเธขเธญเธทเนเธ เน เนเธเนเธฒเธเธฑเธ เธชเธดเนเธเธเธตเนเนเธเธตเนเธขเธงเธเนเธญเธเธญเธขเนเธฒเธเนเธเธฅเนเธเธดเธเธเธทเธญเธเธงเธฒเธกเธชเธฒเธกเธฒเธฃเธเธเธญเธเนเธกเนเธฅเธเธธเธฅเนเธเธเธฒเธฃเธชเธฃเนเธฒเธเธเธฑเธเธเธฐเนเธฎเนเธเธฃเนเธเธ (เนเธเธชเธเธฒเธเธฐเธเธญเธเนเธซเธฅเธง) เธเธถเนเธเธเธณเนเธซเนเนเธกเนเธฅเธเธธเธฅเธขเธฒเธเธเธตเนเธเธฐเธญเธญเธเธเธฒเธเธชเธเธฒเธเธฐเธเธญเธเนเธซเธฅเธง เนเธฅเธฐเธเธณเนเธซเนเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธชเธนเธเธเธถเนเธ เธเธฃเธเธเธฒเธฃเนเธเธญเธเธเธดเธฅเธดเธเธเธเธดเธเธเนเธฒเธข เน เธเธฐเนเธเธดเธเธเธฒเธฃเธฃเธงเธกเธเธฑเธงเธเธฑเธเนเธเนเธเธเธนเนเธเนเธฒเธเธเธฒเธฃเธชเธฃเนเธฒเธเธเธฑเธเธเธฐเนเธฎเนเธเธฃเนเธเธเธฃเธฐเธซเธงเนเธฒเธเนเธกเนเธฅเธเธธเธฅ เธเธฑเธเธเธฑเธขเนเธฅเนเธเธเนเธญเธขเธเธตเนเธชเนเธเธเธฅเธเนเธญเธเธธเธเนเธเธทเธญเธเธเธทเธญเธฃเธนเธเธฃเนเธฒเธเธเธญเธเนเธกเนเธฅเธเธธเธฅ เธเธฒเธฃเธเธณเนเธซเนเธฃเธนเธเธฃเนเธฒเธเธเธญเธเนเธกเนเธฅเธเธธเธฅเธกเธตเธเธงเธฒเธกเธเธฐเธเธฑเธเธฃเธฑเธเธกเธฒเธเธเธถเนเธเธเธฐเธเธณเนเธซเนเธเธธเธเนเธเธทเธญเธเธเธเธเธดเธฅเธเธฅเธเนเธฅเนเธเธเนเธญเธขเนเธกเธทเนเธญเนเธเธตเธขเธเธเธฑเธเนเธกเนเธฅเธเธธเธฅเธเธตเนเธกเธตเธเธทเนเธเธเธดเธงเธชเธฑเธกเธเธฑเธชเธกเธฒเธเธเธงเนเธฒ
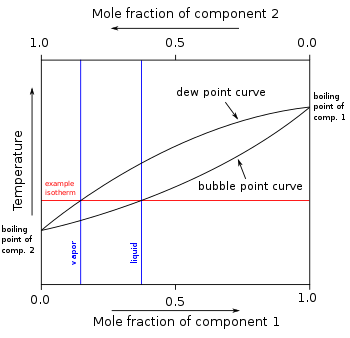 เนเธเธญเธฐเนเธเธฃเธกเธเธธเธเนเธเธทเธญเธเนเธเธเธฒเธฃเธตเธเธญเธเธชเนเธงเธเธเธฃเธฐเธเธญเธเธชเธญเธเธชเนเธงเธเธชเธกเธกเธธเธเธดเธเธตเนเธกเธตเธเธเธดเธเธดเธฃเธดเธขเธฒเนเธเนเธเธญเธเธเธฑเธเนเธเธตเธขเธเนเธฅเนเธเธเนเธญเธขเนเธเธขเนเธกเนเธกเธตเธญเธฐเธเธตเนเธญเธเธฃเธญเธ
เนเธเธญเธฐเนเธเธฃเธกเธเธธเธเนเธเธทเธญเธเนเธเธเธฒเธฃเธตเธเธญเธเธชเนเธงเธเธเธฃเธฐเธเธญเธเธชเธญเธเธชเนเธงเธเธชเธกเธกเธธเธเธดเธเธตเนเธกเธตเธเธเธดเธเธดเธฃเธดเธขเธฒเนเธเนเธเธญเธเธเธฑเธเนเธเธตเธขเธเนเธฅเนเธเธเนเธญเธขเนเธเธขเนเธกเนเธกเธตเธญเธฐเธเธตเนเธญเธเธฃเธญเธ
เธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธตเนเธฃเธฐเนเธซเธขเนเธเนเธกเธฒเธเธเธตเนเธชเธธเธ (เธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเนเธเธฅเนเนเธเธตเธขเธเธเธฑเธเธญเธธเธเธซเธ เธนเธกเธดเนเธงเธเธฅเนเธญเธก) เธกเธฑเธเธเธฐเธเนเธฒเธเธชเธเธฒเธเธฐเธเธญเธเนเธซเธฅเธงเธฃเธฐเธซเธงเนเธฒเธเธเธฒเธฃเธญเธธเนเธเธเธฒเธเธชเธเธฒเธเธฐเธเธญเธเนเธเนเธเนเธเธทเนเธญเนเธเธฅเธตเนเธขเธเนเธเนเธเนเธญ เนเธเธเธฒเธฃเนเธเธฃเธตเธขเธเนเธเธตเธขเธเธเธฑเธเธเธฒเธฃเนเธเธทเธญเธเธเธฒเธฃเธฃเธฐเนเธซเธดเธเนเธเนเธเธเธฒเธฃเนเธเธฅเธตเนเธขเธเนเธเธฅเธเธเธฒเธเธเธฒเธขเธ เธฒเธเธเธตเนเธชเธเธฒเธเธฐเธเธญเธเนเธเนเธเนเธเธฅเธตเนเธขเธเนเธเนเธเนเธญเนเธเธขเธเธฃเธ เธเธถเนเธเนเธเธดเธเธเธถเนเธเนเธเธเธฒเธเธเธฃเธเธต เนเธเนเธเธเธฒเธฃเนเธเธญเธเนเธเธญเธญเธเนเธเธเนเธเธตเนเธเธงเธฒเธกเธเธฑเธเธเธฃเธฃเธขเธฒเธเธฒเธจ เธชเธณเธซเธฃเธฑเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฑเธเธเธฅเนเธฒเธงเธเธธเธเธฃเธฐเนเธซเธดเธเธเธทเธญเธญเธธเธเธซเธ เธนเธกเธดเธเธตเนเธชเธเธฒเธเธฐเธเธญเธเนเธเนเธเนเธเธฅเธตเนเธขเธเนเธเนเธเนเธญเนเธเธขเธเธฃเธเธกเธตเธเธงเธฒเธกเธเธฑเธเนเธญเนเธเนเธฒเธเธฑเธเธเธงเธฒเธกเธเธฑเธเธ เธฒเธขเธเธญเธ
เธชเธดเนเธเนเธเธทเธญเธเธเนเธฅเธฐเธชเธฒเธฃเธเธชเธก
เนเธเธชเนเธงเธเธเนเธญเธเธซเธเนเธฒเธเธตเน เนเธเนเธเธฃเธญเธเธเธฅเธธเธกเธเธธเธเนเธเธทเธญเธเธเธญเธเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธฃเธดเธชเธธเธเธเธดเน เธเธงเธฒเธกเธเธฑเธเนเธญเนเธฅเธฐเธเธธเธเนเธเธทเธญเธเธเธญเธเธชเธฒเธฃเธชเธฒเธกเธฒเธฃเธเนเธเนเธฃเธฑเธเธเธฅเธเธฃเธฐเธเธเธเธฒเธเธเธฒเธฃเธกเธตเธญเธขเธนเนเธเธญเธเธชเธดเนเธเนเธเธทเธญเธเธเธเธตเนเธฅเธฐเธฅเธฒเธขเธญเธขเธนเน (เธชเธฒเธฃเธฅเธฐเธฅเธฒเธข) เธซเธฃเธทเธญเธชเธฒเธฃเธญเธทเนเธ เน เธเธตเนเธเธชเธกเนเธเนเธฒเธเธฑเธเนเธเน เธฃเธฐเธเธฑเธเธเธญเธเธเธฅเธเธฃเธฐเธเธเธเธถเนเธเธญเธขเธนเนเธเธฑเธเธเธงเธฒเธกเนเธเนเธกเธเนเธเธเธญเธเธชเธดเนเธเนเธเธทเธญเธเธเธซเธฃเธทเธญเธชเธฒเธฃเธญเธทเนเธ เน เธเธฒเธฃเธกเธตเธญเธขเธนเนเธเธญเธเธชเธดเนเธเนเธเธทเธญเธเธเธเธตเนเนเธกเนเธฃเธฐเนเธซเธข เนเธเนเธ เนเธเธฅเธทเธญ เธซเธฃเธทเธญเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธเธตเนเธกเธตเธเธงเธฒเธกเธฃเธฐเนเธซเธขเธเนเธณเธเธงเนเธฒเธชเธฒเธฃเธเธฃเธฐเธเธญเธเธซเธฅเธฑเธเธกเธฒเธ เธเธฐเธเธณเนเธซเนเนเธจเธฉเธชเนเธงเธเนเธกเธฅเนเธฅเธฐเธชเธฒเธฃเธฅเธฐเธฅเธฒเธขเธกเธตเธเธงเธฒเธกเธฃเธฐเนเธซเธขเธเนเธญเธขเธฅเธ เนเธฅเธฐเธเธณเนเธซเนเธเธธเธเนเธเธทเธญเธเธเธเธเธดเนเธเธดเนเธกเธเธถเนเธเธเธฒเธกเธชเธฑเธเธชเนเธงเธเธเธญเธเธเธงเธฒเธกเนเธเนเธกเธเนเธเธเธญเธเธชเธฒเธฃเธฅเธฐเธฅเธฒเธขเธเธตเนเธกเธตเธชเธดเนเธเนเธเธทเธญเธเธ เธเธฅเธเธฃเธฐเธเธเธเธตเนเนเธฃเธตเธขเธเธงเนเธฒ เธเธฒเธฃเนเธเธดเนเธกเธเธถเนเธเธเธญเธเธเธธเธเนเธเธทเธญเธ เธเธฑเธงเธญเธขเนเธฒเธเธเธฑเนเธงเนเธเนเธเนเธ เธเนเธณเนเธเธฅเธทเธญ เธเธตเนเธกเธตเธเธธเธเนเธเธทเธญเธเธชเธนเธเธเธงเนเธฒเธเนเธณเธเธฃเธดเธชเธธเธเธเธดเน
เนเธเธชเธฒเธฃเธเธชเธกเธญเธทเนเธ เน เธเธญเธเธชเธฒเธฃเธเธตเนเธชเธฒเธกเธฒเธฃเธเธเธชเธกเธเธฑเธเนเธเน (เธชเนเธงเธเธเธฃเธฐเธเธญเธ) เธญเธฒเธเธกเธตเธชเธญเธเธชเนเธงเธเธเธฃเธฐเธเธญเธเธซเธฃเธทเธญเธกเธฒเธเธเธงเนเธฒเธเธฑเนเธเธเธตเนเธกเธตเธเธงเธฒเธกเธฃเธฐเนเธซเธขเธเนเธฒเธเธเธฑเธ เนเธเธขเนเธเนเธฅเธฐเธชเนเธงเธเธเธฃเธฐเธเธญเธเธเธฐเธกเธตเธเธธเธเนเธเธทเธญเธเธเธญเธเธชเธฒเธฃเธเธฃเธดเธชเธธเธเธเธดเนเธเธญเธเธเธฑเธงเนเธญเธเธเธตเนเธเธงเธฒเธกเธเธฑเธเนเธ เน เธเนเธเธฒเธก เธเธฒเธฃเธกเธตเธญเธขเธนเนเธเธญเธเธชเนเธงเธเธเธฃเธฐเธเธญเธเธเธตเนเธฃเธฐเนเธซเธขเนเธเนเธญเธทเนเธ เน เนเธเธชเธฒเธฃเธเธชเธกเธกเธตเธเธฅเธเธฃเธฐเธเธเธเนเธญเธเธงเธฒเธกเธเธฑเธเนเธญ เนเธฅเธฐเธเธฑเธเธเธฑเนเธเธเธถเธเธชเนเธเธเธฅเธเนเธญเธเธธเธเนเธเธทเธญเธเนเธฅเธฐเธเธธเธเธเนเธณเธเนเธฒเธเธเธญเธเธชเนเธงเธเธเธฃเธฐเธเธญเธเธเธฑเนเธเธซเธกเธเนเธเธชเธฒเธฃเธเธชเธก เธเธธเธเธเนเธณเธเนเธฒเธเธเธทเธญเธญเธธเธเธซเธ เธนเธกเธดเธเธตเนเนเธญเธเธงเธเนเธเนเธเนเธเนเธเธเธญเธเนเธซเธฅเธง เธเธญเธเธเธฒเธเธเธตเน เธเธตเนเธญเธธเธเธซเธ เธนเธกเธดเนเธ เน เธเนเธเธฒเธก เธญเธเธเนเธเธฃเธฐเธเธญเธเธเธญเธเนเธญเธกเธฑเธเธเธฐเนเธเธเธเนเธฒเธเธเธฒเธเธญเธเธเนเธเธฃเธฐเธเธญเธเธเธญเธเธเธญเธเนเธซเธฅเธงเนเธเธเธฃเธเธตเธชเนเธงเธเนเธซเธเน เนเธเธทเนเธญเนเธชเธเธเธเธฅเธเธฃเธฐเธเธเนเธซเธฅเนเธฒเธเธตเนเธฃเธฐเธซเธงเนเธฒเธเธชเนเธงเธเธเธฃเธฐเธเธญเธเธเธตเนเธฃเธฐเนเธซเธขเนเธเนเนเธเธชเธฒเธฃเธเธชเธก เนเธเธขเธเธฑเนเธงเนเธเธเธฐเนเธเน เนเธเธญเธฐเนเธเธฃเธกเธเธธเธเนเธเธทเธญเธ เธเธฒเธฃเธเธฅเธฑเนเธ เนเธเนเธเธเธฃเธฐเธเธงเธเธเธฒเธฃเธเธญเธเธเธฒเธฃเนเธเธทเธญเธเนเธฅเธฐ [เนเธเธขเธเธเธเธดเนเธฅเนเธง] เธเธฒเธฃเธเธงเธเนเธเนเธ เธเธถเนเธเนเธเนเธเธฃเธฐเนเธขเธเธเนเธเธฒเธเธเธงเธฒเธกเนเธเธเธเนเธฒเธเธเธญเธเธญเธเธเนเธเธฃเธฐเธเธญเธเธฃเธฐเธซเธงเนเธฒเธเนเธเธชเธเธญเธเนเธซเธฅเธงเนเธฅเธฐเนเธญ
เธเธฒเธฃเธฒเธ
|
|
| Group โ
|
1
|
2
|
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
12
|
13
|
14
|
15
|
16
|
17
|
18
|
| โ Period
|
|
| 1
|
H2 20.271 K
(โ252.879 ยฐC)
|
|
He4.222 K
(โ268.928 ยฐC)
|
| 2
|
Li1603 K
(1330 ยฐC)
|
Be2742 K
(2469 ยฐC)
|
|
B 4200 K
(3927 ยฐC)
|
C 3915 K (subl.)
(3642 ยฐC)
|
N2 77.355 K
(โ195.795 ยฐC)
|
O2 90.188 K
(โ182.962 ยฐC)
|
F2 85.03 K
(โ188.11 ยฐC)
|
Ne27.104 K
(โ246.046 ยฐC)
|
| 3
|
Na1156.090 K
(882.940 ยฐC)
|
Mg1363 K
(1091 ยฐC)
|
|
Al2743 K
(2470 ยฐC)
|
Si3538 K
(3265 ยฐC)
|
P 553.7 K
(280.5 ยฐC)
|
S 717.8 K
(444.6 ยฐC)
|
Cl2239.11 K
(โ34.04 ยฐC)
|
Ar87.302 K
(โ185.848 ยฐC)
|
| 4
|
K 1032 K
(759 ยฐC)
|
Ca1757 K
(1484 ยฐC)
|
|
Sc3109 K
(2836 ยฐC)
|
Ti3560 K
(3287 ยฐC)
|
V 3680 K
(3407 ยฐC)
|
Cr2945.15 K
(2672.0 ยฐC)
|
Mn2334 K
(2061 ยฐC)
|
Fe3134 K
(2861 ยฐC)
|
Co3200 K
(2927 ยฐC)
|
Ni3003 K
(2730 ยฐC)
|
Cu2835 K
(2562 ยฐC)
|
Zn1180 K
(907 ยฐC)
|
Ga2673 K
(2400 ยฐC)
|
Ge3106 K
(2833 ยฐC)
|
As887 K (subl.)
(615 ยฐC)
|
Se958 K
(685 ยฐC)
|
Br2332.0 K
(58.8 ยฐC)
|
Kr119.735 K
(โ153.415 ยฐC)
|
| 5
|
Rb961 K
(688 ยฐC)
|
Sr1650 K
(1377 ยฐC)
|
|
Y 3203 K
(2930 ยฐC)
|
Zr4650 K
(4377 ยฐC)
|
Nb5017 K
(4744 ยฐC)
|
Mo4912 K
(4639 ยฐC)
|
Tc4538 K
(4265 ยฐC)
|
Ru4423 K
(4150 ยฐC)
|
Rh3968 K
(3695 ยฐC)
|
Pd3236 K
(2963 ยฐC)
|
Ag2483 K
(2210 ยฐC)
|
Cd1040 K
(767 ยฐC)
|
In2345 K
(2072 ยฐC)
|
Sn2875 K
(2602 ยฐC)
|
Sb1908 K
(1635 ยฐC)
|
Te1261 K
(988 ยฐC)
|
I2 457.4 K
(184.3 ยฐC)
|
Xe165.051 K
(โ108.099 ยฐC)
|
| 6
|
Cs944 K
(671 ยฐC)
|
Ba2118 K
(1845 ยฐC)
|

|
Lu3675 K
(3402 ยฐC)
|
Hf4876 K
(4603 ยฐC)
|
Ta5731 K
(5458 ยฐC)
|
W 6203 K
(5930 ยฐC)
|
Re5900.15 K
(5627.0 ยฐC)
|
Os5285 K
(5012 ยฐC)
|
Ir4403 K
(4130 ยฐC)
|
Pt4098 K
(3825 ยฐC)
|
Au3243 K
(2970 ยฐC)
|
Hg629.88 K
(356.73 ยฐC)
|
Tl1746 K
(1473 ยฐC)
|
Pb2022 K
(1749 ยฐC)
|
Bi1837 K
(1564 ยฐC)
|
Po1235 K
(962 ยฐC)
|
At2503ยฑ3 K
(230ยฑ3 ยฐC)
|
Rn211.5 K
(โ61.7 ยฐC)
|
| 7
|
Fr950 K
(677 ยฐC)
|
Ra2010 K
(1737 ยฐC)
|

|
Lr
|
Rf5800 K
(5500 ยฐC)
|
Db
|
Sg
|
Bh
|
Hs
|
Mt
|
Ds
|
Rg
|
Cn340ยฑ10 K
(67ยฑ10 ยฐC)
|
Nh1430 K
(1130 ยฐC)
|
Fl380 K
(107 ยฐC)
|
Mc~1400 K
(~1100 ยฐC)
|
Lv1035โ1135 K
(762โ862 ยฐC)
|
Ts883 K
(610 ยฐC)
|
Og450ยฑ10 K
(177ยฑ10 ยฐC)
|
|

|
La3737 K
(3464 ยฐC)
|
Ce3716 K
(3443 ยฐC)6
|
Pr3403 K
(3130 ยฐC)
|
Nd3347 K
(3074 ยฐC)
|
Pm3273 K
(3000 ยฐC)
|
Sm2173 K
(1900 ยฐC)
|
Eu1802 K
(1529 ยฐC)
|
Gd3546 K
(3273 ยฐC)
|
Tb3396 K
(3123 ยฐC)
|
Dy2840 K
(2567 ยฐC)
|
Ho2873 K
(2600 ยฐC)
|
Er3141 K
(2868 ยฐC)
|
Tm2223 K
(1950 ยฐC)
|
Yb1469 K
(1196 ยฐC)
|

|
Ac3471 K
(3198 ยฐC)
|
Th5061 K
(4788 ยฐC)
|
Pa4300? K
(4027 ยฐC)
|
U 4404 K
(4131 ยฐC)
|
Np4175.15 K
(3902.0 ยฐC)
|
Pu3508.15 K
(3235.0 ยฐC)
|
Am2880 K
(2607 ยฐC)
|
Cm3383 K
(3110 ยฐC)
|
Bk2900 K
(2627 ยฐC)
|
Cf1743 K
(1470 ยฐC)
|
Es1269
(996 ยฐC)
|
Fm
|
Md
|
No
|
| Legend
|
| Values are in kelvin K and degrees Celsius ยฐC, rounded
|
| For the equivalent in degrees Fahrenheit ยฐF, see: Boiling points of the elements (data page)
|
| Some values are predictions
|
|
|
เธญเนเธฒเธเธญเธดเธ
- โ Goldberg, David E. (1988). 3,000 Solved Problems in Chemistry (1st ed.). McGraw-Hill. section 17.43, p. 321. ISBN 0-07-023684-4.
- โ Theodore, Louis; Dupont, R. Ryan; Ganesan, Kumar, เธ.เธ. (1999). Pollution Prevention: The Waste Management Approach to the 21st Century. CRC Press. section 27, p. 15. ISBN 1-56670-495-2.
- โ "Boiling Point of Water and Altitude". www.engineeringtoolbox.com.
- โ General Chemistry Glossary Purdue University website page
- โ Reel, Kevin R.; Fikar, R. M.; Dumas, P. E.; Templin, Jay M. & Van Arnum, Patricia (2006). AP Chemistry (REA) โ The Best Test Prep for the Advanced Placement Exam (9th ed.). Research & Education Association. section 71, p. 224. ISBN 0-7386-0221-3.
- โ 6.0 6.1 Cox, J. D. (1982). "Notation for states and processes, significance of the word standard in chemical thermodynamics, and remarks on commonly tabulated forms of thermodynamic functions". Pure and Applied Chemistry. 54 (6): 1239โ1250. doi:10.1351/pac198254061239.
- โ เธเธงเธฒเธกเธเธฑเธเธกเธฒเธเธฃเธเธฒเธ IUPAC เธเธณเธซเธเธเธงเนเธฒ "เธเธงเธฒเธกเธเธฑเธเธกเธฒเธเธฃเธเธฒเธ" เนเธเนเธฒเธเธฑเธ 105 Pa (เธเธถเนเธเนเธเนเธฒเธเธฑเธ 1 เธเธฒเธฃเน).
- โ เธ เธฒเธเธเธเธงเธ 1: เธเธฒเธฃเธฒเธเธเธธเธเธชเธกเธเธฑเธเธดเนเธฅเธฐเธเธฃเธฒเธ (เธซเธเนเธงเธข SI), เนเธฅเธทเนเธญเธเนเธเธเธตเนเธเธฒเธฃเธฒเธ A-5 เนเธฅเธฐเธญเนเธฒเธเธเนเธฒเธเธญเธ 99.61 ยฐC เธเธตเนเธเธงเธฒเธกเธเธฑเธ 100 kPa (1 เธเธฒเธฃเน). เธเนเธญเธกเธนเธฅเธเธฒเธเนเธงเนเธเนเธเธเน Higher Education เธเธญเธ McGraw-Hill.
- โ West, J. B. (1999). "Barometric pressures on Mt. Everest: New data and physiological significance". Journal of Applied Physiology. 86 (3): 1062โ6. doi:10.1152/jappl.1999.86.3.1062. PMID 10066724. S2CID 27875962.
- โ Perry, R.H.; Green, D.W., เธ.เธ. (1997). Chemical Engineering Handbook Perry (7th ed.). McGraw-Hill. ISBN 0-07-049841-5.
- โ DeVoe, Howard (2000). Thermodynamics and Chemistry (1st ed.). Prentice-Hall. ISBN 0-02-328741-1.
เนเธซเธฅเนเธเธเนเธญเธกเธนเธฅเธญเธทเนเธ