En química, os epímeros son diastereoisómeros que só difiren entre si na configuración nun centro estereoxénico. Os disatereoisómeros son unha clase de estereoisómeros que non son superpoñibles, polo que non son imaxes especulares un do outro.[1][2]
Na nomenclatura química, nun dos epímeros do par leva o prefixo epi; por exemplo, a quinina e a epiquinina. Cando o par é de enantiómeros, o prefixo que se utiliza é ent.
Exemplos
O azucre α-D-glicosa e β-D-glicosa son epímeros. Na α-D-glicosa, o grupo OH do primeiro carbono (anomérico) está na posición oposta ao grupo unido ao carbono 6 (en posición axial). Na β-D-glicosa, o grupo OH está orientado na mesma dirección ca o grupo unido ao carbono 6 (en posición ecuatorial).[3] Estas dúas moléculas son ambas as dúas epímeras e á vez anómeras.
![]() |

|
| α-D-glicopiranosa |
β-D-glicopiranosa
|
A β-D-glicopiranosa e a β-D-manopiranosa son epímeros porque difiren só na estereoquímica do carbono 2. O grupo hidroxilo da β-D-glicopiranosa é ecuatorial (situado no "plano" do anel), e na β-D-manopiranosa o grupo hidroxilo en C-2 é axial (por riba do "plano" do anel). Estas dúas moléculas son epímeros pero non anómeros.
A doxorrubicina e a epirrubicina son dúas substancias relacionadas que son epímeros entre si.

|
| Comparación doxorrubicina–epirrubicina
|
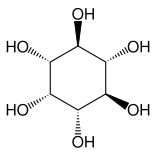
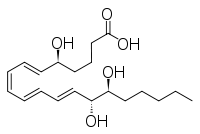
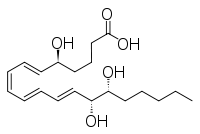
Outros compostos moi relacionados son o epiinositol e o inositol, e a lipoxina e a epilipoxina.
 |
 |
 |
|
| Epiinositol
|
Inositol
|
Lipoxina
|
Epilipoxina
|
Epimerización
A epimerización é un proceso químico onde un epímero se transforma no seu isómero quiral alternativo. Pode acontecer nas reaccións de despolimerización de taninos condensados. A epimerización pode ser espontánea (xeralmente é un proceso moi lento), ou ser catalizada por encimas; por exemplo, a epimerización entre os azucres N-acetilglicosamina e N-acetilmanosamina, que está catalizado pola proteína de unión á renina.
Notas