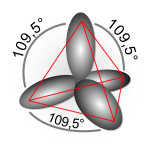
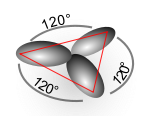
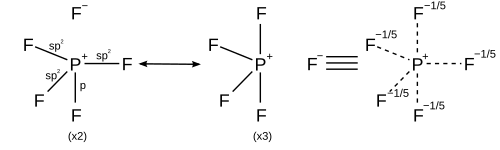
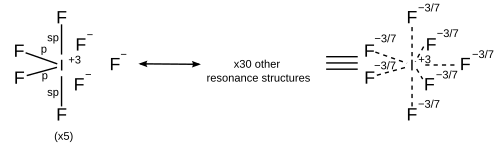
Hibridisasi orbital
| |||||||||||||||||||||||||||||||||||||
Read other articles:

English director and film editor This article has multiple issues. Please help improve it or discuss these issues on the talk page. (Learn how and when to remove these template messages) This biography of a living person relies on a single source. You can help by adding reliable sources to this article. Contentious material about living people that is unsourced or poorly sourced must be removed immediately. (January 2014) (Learn how and when to remove this template message)Some of this articl...

تشيفاز ريغالChivas Regal (بالإنجليزية) معلومات عامةالمنشأ اسكتلندابلد المطبخ سكوتش اسكتلنديالمبتكر شركة الأخوين تشيفاز ، تشيفاز بروذرزتاريخ الابتكار 1801 القيمة الغذائيةنسبة الكحول 40%تعديل - تعديل مصدري - تعديل ويكي بيانات تشيفاز ريغال (بالإنجليزية: Chivas Regal) ويسكي سكوتش مخلوط �...

Ministry of agriculture in Somalia Ministry of Agriculture and IrrigationWasaaradda Beeraha iyo WaraabkaCoat of arms of SomaliaAgency overviewFormedSeptember 1960JurisdictionSomaliaHeadquartersMogadishuAgency executiveDr. Said Hussein Iid, Minister of Agriculture and Irrigation of SomaliaParent agencyCabinet of Somalia The Ministry of Agriculture and Irrigation of Somalia (MOAIOS) (Somali: Wasaaradda Beeraha iyo Waraabka ee Soomaaliya) is a ministry responsible for Agriculture in Somalia. The...

This article needs additional citations for verification. Please help improve this article by adding citations to reliable sources. Unsourced material may be challenged and removed.Find sources: Kittatinny Valley State Park – news · newspapers · books · scholar · JSTOR (October 2018) (Learn how and when to remove this template message) Kittatinny Valley State ParkKayakers on Lake AeroflexShow map of Sussex County, New JerseyShow map of New JerseyShow m...

Artikel ini sebatang kara, artinya tidak ada artikel lain yang memiliki pranala balik ke halaman ini.Bantulah menambah pranala ke artikel ini dari artikel yang berhubungan atau coba peralatan pencari pranala.Tag ini diberikan pada Desember 2022. Gabing merupakan batang kelapa muda yang dimasak menjadi sayur dengan kuah santan. Mirip dengan sayur gori (nangka muda) di Jawa.[1] Resep Gabing Khas Lampung. Gabing merupakan salah masakan khas Lampung yang ada di daerah lainya. Gabing sendi...

Nanatsuiro DropsSampul depan novel visual orisinal Nanatsuiro Dropsななついろ★ドロップスGenreFantasi · Perempuan pesulap · Romansa PermainanPengembangUNiSONSHIFTPenerbitUNiSONSHIFT (Windows)MediaWorks (PS2)ASCII Media Works (DS)GenreEroge · Novel visualPlatformWindows · PS2 · DSRilis21 April 2006 Novel ringanPengarangTamaki IchikawaIlustratorNoizi ItoPenerbitEnterbrainDemografiMaleTerbit30 Juni 2006 MangaPengarangUNiSONSHIFTIl...

Herzog Ernst im Kreis seiner Räte (Zeichnung von R. A. Jaumann, entstanden 1899) Ernst von Bayern-München (* 1373; † 2. Juli 1438 in München) aus dem Haus Wittelsbach war von 1397 bis 1438 Herzog von Bayern-München. Nach dem Erlöschen der wittelsbachischen Linie Bayern-Straubing erhielt Bayern-München durch den Preßburger Schiedsspruch von 1429 den größten Teil des Straubinger Erbes zugesprochen. Der Nachwelt bekannt ist Ernst vor allem durch seine Rolle beim Tod der Agnes Bernauer...

Dutch ocean liner built in Ireland & chartered to Sweden For other ships with the same name, see List of ships named Noordam and List of ships named Kungsholm. Noordam picking up a pilot in 1903. History Name 1902: Noordam 1923: Kungsholm 1925: Noordam OwnerHolland America Line Operator1923: Swedish American Line Port of registry 1902: Rotterdam 1923: Gothenburg 1925: Rotterdam Route 1902: Rotterdam – New York 1923: Gothenburg – New York 1926: Rotterdam – New York BuilderHarland &am...

Religion in Ghana Religion in Ghana (2021 census)[1] Christianity (71.3%) Islam (20%) Traditional faiths (3.2%) None (1.1%) Others/No answer (4.5%) Holy Trinity Anglican Cathedral in the capital Accra Ahmadiyya Central Mosque in Tamale, Northern region Christianity is the largest religion in Ghana, with 71.3% of the population being member of various Christian denominations as of 2021 census.[2] Islam is practised by 20% ...

Slovak footballer Albert Rusnák Rusnák with Real Salt Lake in 2021Personal informationFull name Albert Rusnák[1]Date of birth (1994-07-07) 7 July 1994 (age 29)Place of birth Vyškov, Czech Republic[2]Height 1.75 m (5 ft 9 in)Position(s) Attacking midfielderTeam informationCurrent team Seattle Sounders FCNumber 11Youth career KAC Košice[2]1997–2010 Košice2010–2013 Manchester CitySenior career*Years Team Apps (Gls)2013–2015 Manchester City ...

1986 Burkinabé filmSarraouniaDirected byMed HondoWritten byMed HondoAbdoulaye MamaniProduced byMed HondoStarringAï KeïtaCinematographyGuy FamechonEdited byMarie-Thérèse BoichéMusic byPierre AkendenguéAbdoulaye CisséIssouf CompaoreProductioncompanyLes Films Soleil ORelease date 26 November 1986 (1986-11-26) (France) Running time120 minutesCountriesBurkina FasoMauritaniaFranceLanguagesDioula, Fula, FrenchBudget$3,000,000 Sarraounia is a 1986 historical drama film writ...

CPU Sony Emotion Engine Emotion Engine dalam papan induk PS2 Emotion Engine adalah unit pemrosesan pusat yang dikembangkan dan diproduksi oleh Sony Computer Entertainment dan Toshiba untuk digunakan di konsol permainan PlayStation 2. Prosesor ini juga digunakan pada model PlayStation 3 awal yang dijual di Jepang dan Amerika Utara (Nomor Model CECHAxx & CECHBxx) untuk memberikan dukungan permainan PlayStation 2. Produksi massal Emotion Engine dimulai pada 1999 dan berakhir pada akhir 2012 ...

City in Georgia, United StatesDemorest, GeorgiaCityLocation in Habersham County and the state of GeorgiaCoordinates: 34°33′54″N 83°32′33″W / 34.56500°N 83.54250°W / 34.56500; -83.54250CountryUnited StatesStateGeorgiaCountyHabershamFoundedNovember 13, 1889[1]Government • TypeCouncil - Manager • MayorJerry Harkness • City ManagerMark MusselwhiteArea[2] • Total2.27 sq mi (5.88 km2)&...

造王者King Maker类型古裝恩仇编剧薛家華、何永年、陳寶燕、黎雅倫、沈立強、區嘉慧编导羅鎮岳、陳志江、林鳳玲、朱禮和、廖晉碩助理编导張永輝、唐子洋、馬澤鋒、文家麗、胡家斌、郭家禧、林瑋澄、曹建成主演黎耀祥、鄭則士、敖嘉年、黎諾懿、田蕊妮、唐詩詠、姚子羚、苑瓊丹、郭少芸、李國麟、鄧健泓、郭 峰、石 修、李天翔、胡諾言、楊秀惠旁白陳 欣国家�...

Metallurgical preheating of air Further information: Cowper stoveBlast furnace (left), and three Cowper stoves (right) used to preheat the air blown into the furnace. Hot blast furnace: note the flow of air from the stove in the background to the two blast furnaces, and hot air from the foreground furnace being drawn off to heat the stove. Hot blast refers to the preheating of air blown into a blast furnace or other metallurgical process. As this considerably reduced the fuel consumed, hot bl...

ГородВайтерштадтWeiterstadt Герб 49°54′ с. ш. 8°36′ в. д.HGЯO Страна Германия Земля Гессен Район Дармштадт-Дибург (район) Внутреннее деление 4 городских района Глава Петер Рорбах(ALW) История и география Площадь 34,4 км² Высота центра 105 м Часовой пояс UTC+1:00, летом UTC+2:00 Нас�...

Ver artigo principal: Pandemia de COVID-19 na EuropaMais informações: Pandemia de COVID-19 por país e Pandemia de COVID-19 Pandemia de COVID-19 na Espanha Número de casos confirmados por 100 milhões de habitantes por comunidade autônoma Doença COVID-19 Agente infeccioso SARS-CoV-2 Data de início 31 de janeiro de 2020 Localidade Espanha País Espanha Estatísticas Globais Casos confirmados 13 770 429 (9 março 2023)[1] Mortes 119 479 (9 março 2023)[1] [edite no Wikidata] Parte...

Den här artikeln behöver källhänvisningar för att kunna verifieras. (2010-06) Åtgärda genom att lägga till pålitliga källor (gärna som fotnoter). Uppgifter utan källhänvisning kan ifrågasättas och tas bort utan att det behöver diskuteras på diskussionssidan. Man mognar med åren var Nynningens första skiva och kom ut på MNW 1972. Låtar på albumet Sida A: Man mognar med åren Förbannelse över byråkratismen Den största kärleken Folkets låt Sida B: Lagom till jul Kapte...

Pour les articles homonymes, voir Deux-Novembre. Éphémérides Novembre 1er 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 2 octobre 2 décembre Chronologies thématiques Croisades Ferroviaires Sports Disney Anarchisme Catholicisme Abréviations / Voir aussi (° 1852) = né en 1852 († 1885) = mort en 1885 a.s. = calendrier julien n.s. = calendrier grégorien Calendrier Calendrier perpétuel Liste de calendriers Naissances d...

هذه المقالة بحاجة لصندوق معلومات. فضلًا ساعد في تحسين هذه المقالة بإضافة صندوق معلومات مخصص إليها. المقالة الرئيسة: نظام العد الهندي العربي نظام العد الهندي العربي هو نظام عد عشري يرتكز على فكرة وجود الخانات، ويستعمل هذا النظام رمز الصفر كما في ’’909‘‘.[1] اشتقت رموز هذ...